Clear Sky Science · ru
Стратификация по предписанной дозе улучшает предсказание дозы при VMAT на основе глубокого обучения для местно-распространённого НМРЛ
Почему важны более разумные планы облучения
Когда врачи лечат распространённый рак лёгкого с помощью радиации, им приходится балансировать: подать достаточно энергии, чтобы контролировать опухоль, и одновременно защитить чувствительные соседние органы. Проектирование таких планов медленное, сложное и сильно зависит от мастерства планировщика. В этом исследовании изучают, как искусственный интеллект может предсказывать распределение дозы в грудной клетке и, что важно, показывают, что обучение ИИ с аккуратно сгруппированными уровнями предписанной дозы делает его предсказания более точными и клинически полезными.
Как лечат рак лёгкого сфокусированными лучами
Большинству пациентов с местно-распространённым немелкоклеточным раком лёгкого опухоль нельзя удалить хирургически. Вместо этого им часто назначают химиотерапию вместе с сильно формируемыми лучевыми пучками, которые вращаются вокруг грудной клетки по дугам — техника, известная как VMAT. Цель — подвергнуть опухоль высокой, однородной дозе, ограничивая при этом облучение лёгких, сердца, пищевода и спинного мозга. Достижение этого баланса обычно требует нескольких итераций проб и ошибок, что отнимает время и может задерживать принятие лечебных решений. Если врачи могли бы быстро оценить, какое распределение дозы реально достижимо для конкретного пациента, они могли бы раньше выбрать оптимальную стратегию лечения.
Обучение алгоритма распознавать паттерны дозы
Исследователи обратились к глубокому обучению — разновидности ИИ, которая выявляет закономерности напрямую по изображениям. Они собрали КТ-снимки и законченные планы лечения 72 пациентов с раком лёгкого, лечившихся с помощью VMAT. Для каждого пациента они пересчитали, как та же конфигурация пучков доставляет три различных суммарных дозы: 50, 54 и 60 грей (Gy) — стандартные единицы радиации. Каждый случай был преобразован в трёхмерную сетку, отмечающую опухоль, ключевые органы и исходное КТ-изображение. Эти девять каналов информации подали в 3D U-Net — распространённую архитектуру нейросети, которая может научиться, как доза обычно распределяется по телу в зависимости от анатомии.
Почему имеет значение группировка по предписанной дозе
Ключевой вопрос заключался в том, как учитывать факт, что пациентам назначают разные суммарные дозы. Команда построила четыре по сути идентичных модели ИИ. Три были «одно-предписные» модели, каждая обучена только на планах одного уровня дозы (50, 54 или 60 Gy). Четвёртая модель смешивала случаи с 50 и 60 Gy без указания сети, с какой предписанной дозой она имеет дело. При тестировании на новых пациентах модели, специфичные для предписания, лучше соответствовали истинной дозе в опухоли, сохраняя как покрытие, так и горячие точки близкими к клиническим планам, обычно в пределах нескольких Gy. Напротив, смешанная модель допускала заметно большие ошибки в областях с наибольшей дозой в опухоли и вокруг спинного мозга, где доза должна оставаться ниже строгих предельных значений безопасности.
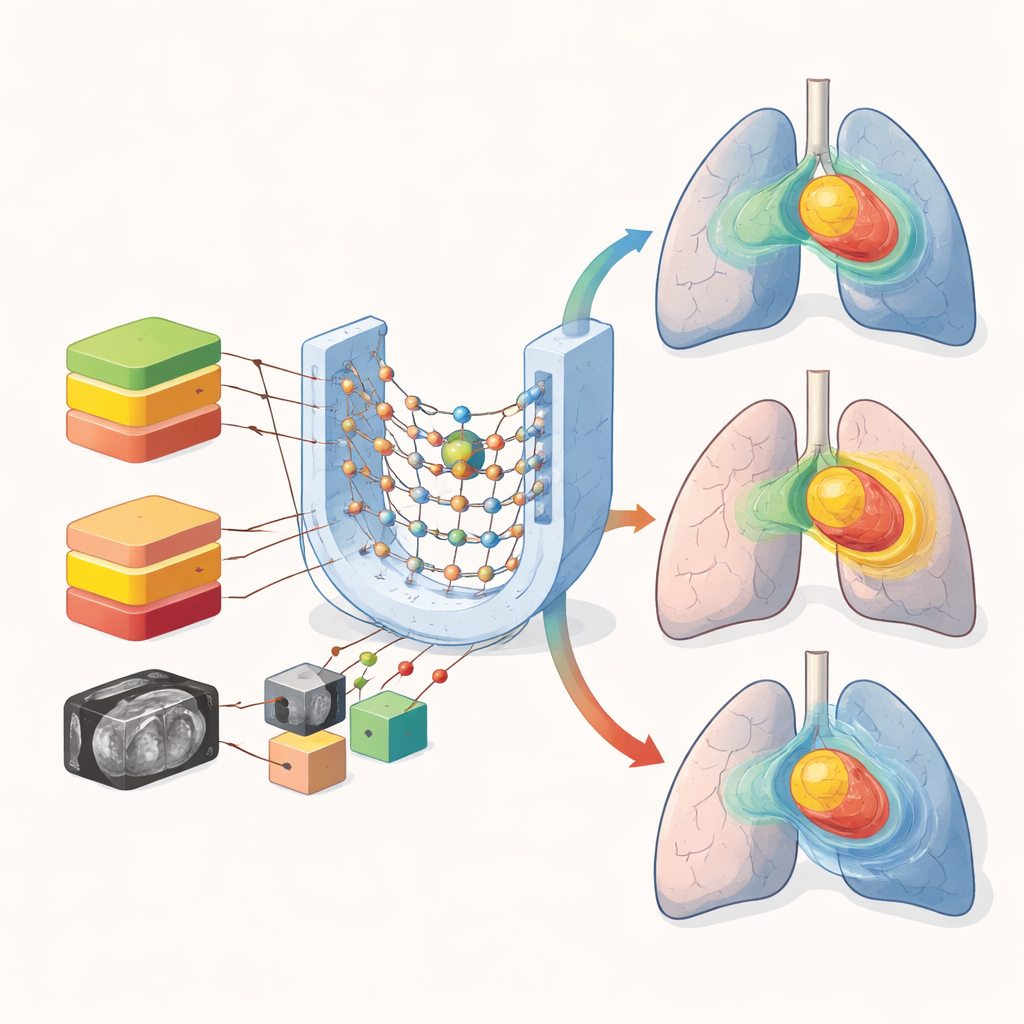
Защита жизненно важных органов при ускорении планирования
Интересно, что для многих органов, таких как лёгкие, сердце и пищевод, смешанная и стратифицированная модели показали схожую работу. Средние ошибки дозы для этих крупных структур оставались умеренными при всех подходах. Основная слабость смешивания предписаний проявлялась в маленьких, чувствительных структурах, таких как спинной мозг, где важен резкий спад дозы. Визуальная проверка предсказанных карт дозы показала, что все модели уловили общую форму зоны высокой дозы в опухоли, но смешивание предписаний приводило к большему размытию в резких градиентах и областях низкой дозы в лёгких. Эти различия, хотя и незначительные в числовом выражении, могут иметь значение, когда врачи решают, безопасно ли назначать более высокую предписанную дозу.
Что это значит для пациентов и клиник
Для пациентов эта работа не заменяет тщательных расчётов доз, которые уже выполняются клиническими системами, но может помочь сосредоточить время и усилия на планах, которые действительно осуществимы и безопасны. Показав, что группировка обучающих данных по предписанной дозе существенно повышает остроту предсказаний ИИ — особенно в части покрытия опухоли и защиты спинного мозга — исследование подчёркивает практический выбор проектирования, который может сделать компьютерную поддержку более надёжной. При дальнейшем тестировании на больших и более разнообразных группах пациентов такие модели могли бы стать повседневными инструментами, дающими врачам быстрый, основанный на анатомии прогноз вероятных радиационных компромиссов и поддерживающими более качественное и последовательное планирование лечения.
Цитирование: Chaipanya, T., Nimjaroen, K., Chamchod, S. et al. Prescription‑dose stratification improves deep learning‑based VMAT dose prediction in locally advanced NSCLC. Sci Rep 16, 8707 (2026). https://doi.org/10.1038/s41598-026-43192-6
Ключевые слова: лучевая терапия рака лёгкого, предсказание дозы с помощью глубокого обучения, планирование VMAT, оптимизация плана лечения, органы риска