Clear Sky Science · ru
Изучение двойной роли внеклеточных везикул в коагуляции и модуляции иммунитета при глиобластоме
Почему тромбы важны при раке мозга
У людей с глиобластомой — самой агрессивной формой рака мозга — часто возникает неожиданная угроза: опасные тромбы в ногах или мозге. Эти сгустки могут сократить продолжительность жизни и осложнить и без того тяжёлое лечение. В этом исследовании поставлен простой, но важный вопрос: что именно в клетках глиобластомы делает окружающую их кровь столь склонной к свертыванию и как крошечные частицы, которые они сбрасывают в кровь, перестраивают иммунные защиты организма?
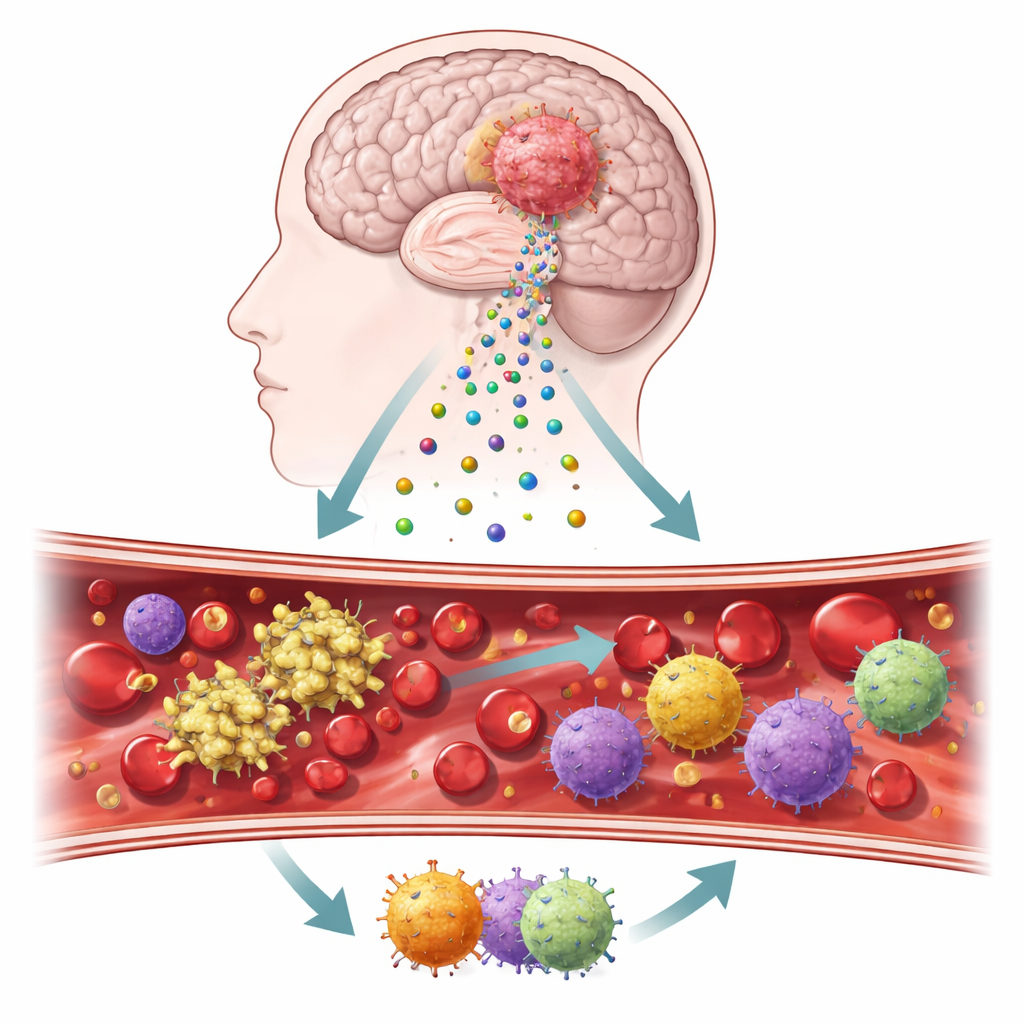
Крошечные посланцы, покидающие опухоль мозга
Исследователи сосредоточились на микроскопических пузырьках — внеклеточных везикулах, которые отщепляются от опухолевых клеток и перемещаются по крови и тканям мозга. На их поверхности находятся два ключевых белка — тканевой фактор и подопланин, — которые известны тем, что запускают образование тромбов и влияют на воспаление. Используя образцы опухолей, кровь, взятую во время операции, и культивированные из опухолей пациентов клеточные линии, команда выстроила пошаговый рабочий процесс, чтобы проследить поведение этих молекул у реальных пациентов и в контролируемых лабораторных тестах. Они также сравнили опухолевую ткань с нормальной тканью мозга, чтобы оценить, насколько активно включены эти сигналы, связанные со свёртыванием.
Тихий кровоток, но подготовленная зона опухоли
Стандартные больничные тесты показали, что до операции кровь многих пациентов выглядела удивительно нормально: общие показатели свертывания и прочности сгустка в основном находились в референсных пределах. Однако при изучении самих опухолей проявилась иная картина. Ткань глиобластомы постоянно демонстрировала высокие уровни тканевого фактора и подопланина и очень низкие уровни природного тормоза — ингибитора пути тканевого фактора. Полученные от пациентов клеточные линии в культуре в целом сохраняли этот профиль, подтверждая, что «способствующая тромбообразованию» подпись является внутренней особенностью раковых клеток. Когда эти клетки или выделяемые ими везикулы смешивали с плазмой в лаборатории, сгустки образовывались быстрее, особенно по так называемому внешнему (экзогенному) пути, который зависит от тканевого фактора.
Разные опухолевые клетки — разные стратегии свертывания
Не все глиобластомы вели себя одинаково. Некоторые клеточные линии, полученные от пациентов, содержали очень много тканевого фактора, у других преобладал подопланин, а у некоторых обоих белков было мало. Клетки с высоким содержанием тканевого фактора наиболее эффективно сокращали время свертывания, тогда как богатые подопланином клетки вносили умеренный вклад через воздействие на тромбоциты. Когда одну такую клеточную линию разделили на подгруппы, экспрессирующие только тканевой фактор, только подопланин, оба белка или ни одного из них, клетки надолго не сохраняли эти статусы. В течение трёх недель они смещались обратно к смешанным профилям, что указывает на высокую степень пластичности. Эта динамическая перестройка сопровождалась изменениями уровня окислительного стресса внутри клеток, намекая на то, что химический стресс в опухоли может склонять клетки к более про-тромботическим состояниям.
Везикулы как формирователи иммунитета мозга и крови
Далее команда подробно изучила, как внеклеточные везикулы опухоли влияют на собственные иммунные клетки мозга — микроглию — а также на циркулирующие лейкоциты и нейтрофилы. Везикулы от высоко про-тромботических клеточных линий активно захватывались микроглией и замедляли её миграцию, одновременно сдвигая её в более воспалительное «M1-подобное» состояние и вызывая признаки клеточного старения. В кровотоке везикулы, богатые тканевым фактором, активировали лейкоциты, усиливали образование реактивных форм кислорода и стимулировали выброс липких сетчатых структур нейтрофилов, известных как внеклеточные ловушки. Везикулы, несущие подопланин, были менее силёнными в провоцировании этих взрывных иммунных реакций, но сильно способствовали запуску программы, похожей на сенесценцию, при которой иммунные клетки прекращают деление и меняют поведение. Даже везикулы, лишённые обоих ключевых белков, могли вызывать некоторую сенесценцию, что указывает на важность других компонентов их содержимого.
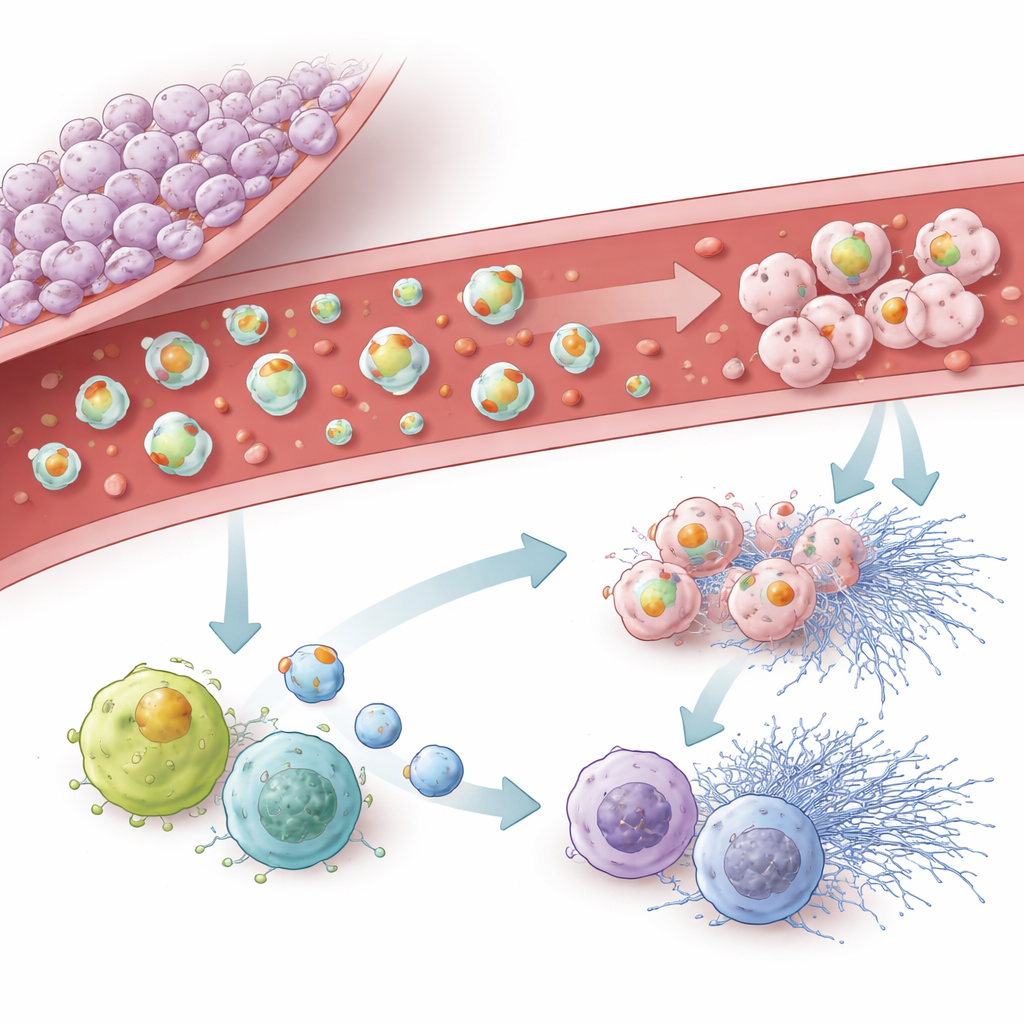
Что это значит для пациентов и будущей терапии
В совокупности результаты показывают, что глиобластома не просто общесистемно сгущает кровь. Скорее, сама опухоль и выделяемые ею везикулы создают локализованную, крайне сложную зону, где свёртывание и воспаление подпитывают друг друга. Тканевой фактор выступает основным мотором формирования тромбов и активации воспаления, тогда как подопланин вносит свой вклад через влияние на тромбоциты, иммунное старение и поведение микроглии. Поскольку эти везикулы циркулируют и отражают состояние опухоли, они могут стать будущими маркёрами в крови для выявления пациентов с особенно высоким риском тромбоза. Они также указывают на возможность более целевых стратегий профилактики, направленных на про-тромботическое оборудование опухоли без широкого разжижения крови.
Цитирование: Wolff, A., Waitz, G., Kaps, P. et al. Exploring the dual role of extracellular vesicles in coagulation and immune modulation in glioblastoma. Sci Rep 16, 9534 (2026). https://doi.org/10.1038/s41598-026-42867-4
Ключевые слова: глиобластома, кровяные тромбы, внеклеточные везикулы, микроокружение опухоли, иммунный ответ