Clear Sky Science · ru
Оценка dodecin-скелета Mycobacterium tuberculosis в качестве платформы мультимеризации для иммуногенности антигенов HPV L2
Почему это исследование важно для будущих вакцин
Вирусы папилломы человека (ВПЧ) вызывают почти все случаи рака шейки матки и всё большую долю других видов рака, однако существующие вакцины сложны в производстве и не покрывают полностью все опасные типы вируса. В этом исследовании рассматривается новый способ создания более простой и более широко защищающей вакцины против ВПЧ, которая могла бы быть дешевле, более стабильной и проще в применении по всему миру, особенно в странах с низким и средним уровнем дохода. Перестраивая способ показа иммунной системе ключевых фрагментов вирусного белка, исследователи стремятся побудить организм вырабатывать мощные антитела одновременно против многих типов ВПЧ.
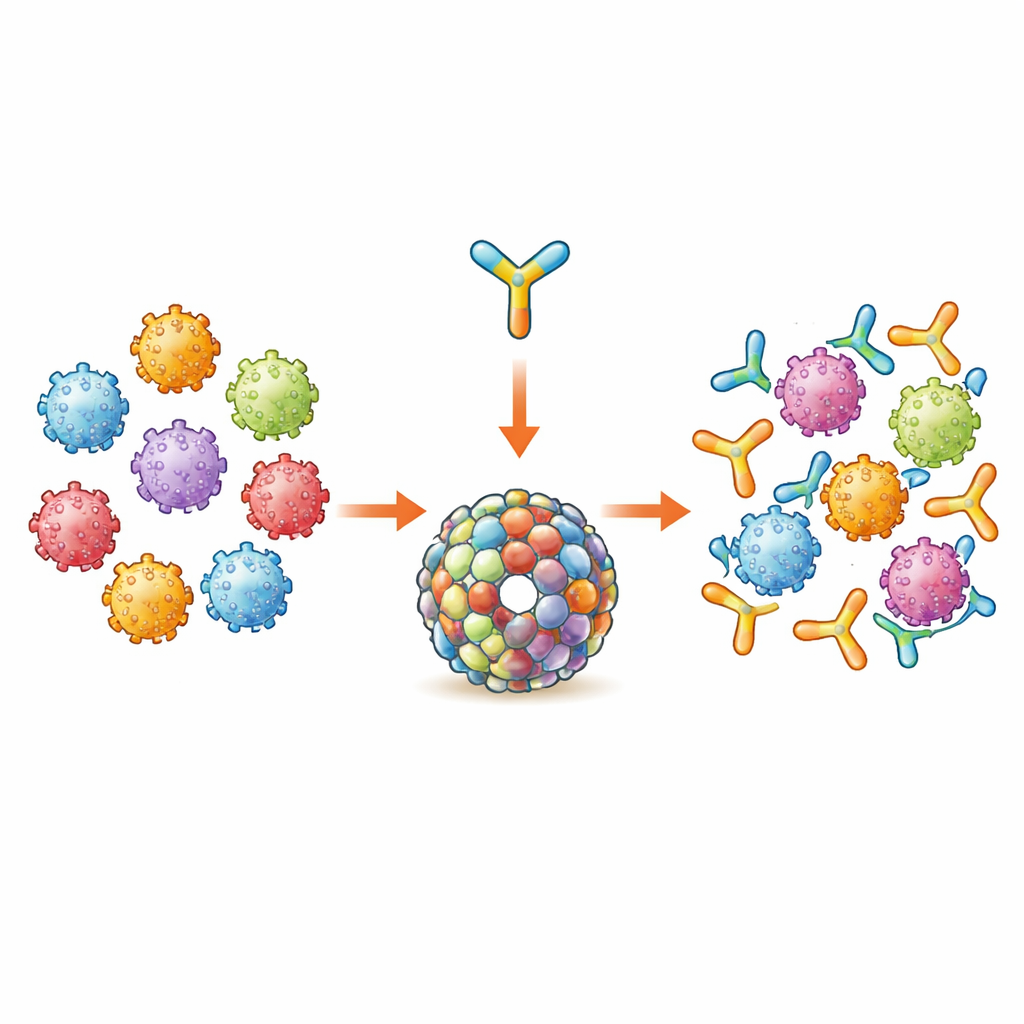
Новая «строительная единица» для защиты от ВПЧ
Современные прививки от ВПЧ опираются на оболочный белок вируса L1, собранный в вирусоподобные частицы, которые сильно стимулируют выработку антител, но в основном против тех немногих типов ВПЧ, которые включены в вакцину. Команда сосредоточилась вместо этого на втором вирусном белке, L2, который содержит короткие участки, схожие у многих типов ВПЧ и, следовательно, может обеспечивать более широкую защиту. Они использовали ранее разработанный антиген Trx-8mer, где небольшие консервативные фрагменты L2 из восьми типов ВПЧ сшиты вместе и представлены на стабильном носителе. Ранее уже показали, что упаковка семи таких единиц Trx-8mer в кольцеобразный комплекс (вакцина PANHPVAX) вызывает сильные перекрестно-защитные антительный ответы и сейчас проходит ранние этапы испытаний на людях.
Превращение бактериального белка в вакцинную платформу
В этом исследовании исследователи попытались выйти за пределы семи копий и уместить ещё больше антигенов L2 в каждой частицы, исходя из предположения, что высоко-повторяющиеся структуры особенно эффективны в активации В-клеток — клеток, производящих антитела. Они выбрали крошечный термостойкий белок из бактерии туберкулёза, называемый dodecin, который естественно собирается в полые шарики из двенадцати идентичных субъединиц. Путём генетического сращения Trx-8mer с dodecin они создали несколько новых кандидатов на вакцину, рассчитанных на самосборку в мультимерные наночастицы, несущие множество копий L2. Эти частицы можно было производить в бактериях, очищать при высокой температуре благодаря их прочности и проверять разными биофизическими методами на формирование задуманной наноструктуры.
Когда прямое сращение недостаточно
Удивительно, но простое прикрепление L2-груза напрямую к dodecin-скелету не превзошло существующую гептамерную референтную вакцину PANHPVAX в экспериментах на мышах. Хотя мультимерные частицы сформировались как задумано и индуцировали нейтрализующие антитела как против вакцинных, так и вне-вакцинных типов ВПЧ, титры в целом были ниже, чем у PANHPVAX. Добавление встроенного эпитопа Т-хелпера, который иногда повышает антительный ответ, также не улучшило показатели. Структурное моделирование и функциональные данные предположили, что объёмные напрямую сращённые единицы Trx-8mer могут мешать друг другу и экранировать критические участки L2 от рецепторов В-клеток, ослабляя иммунный ответ, несмотря на то, что по идее количество копий антигена было больше.
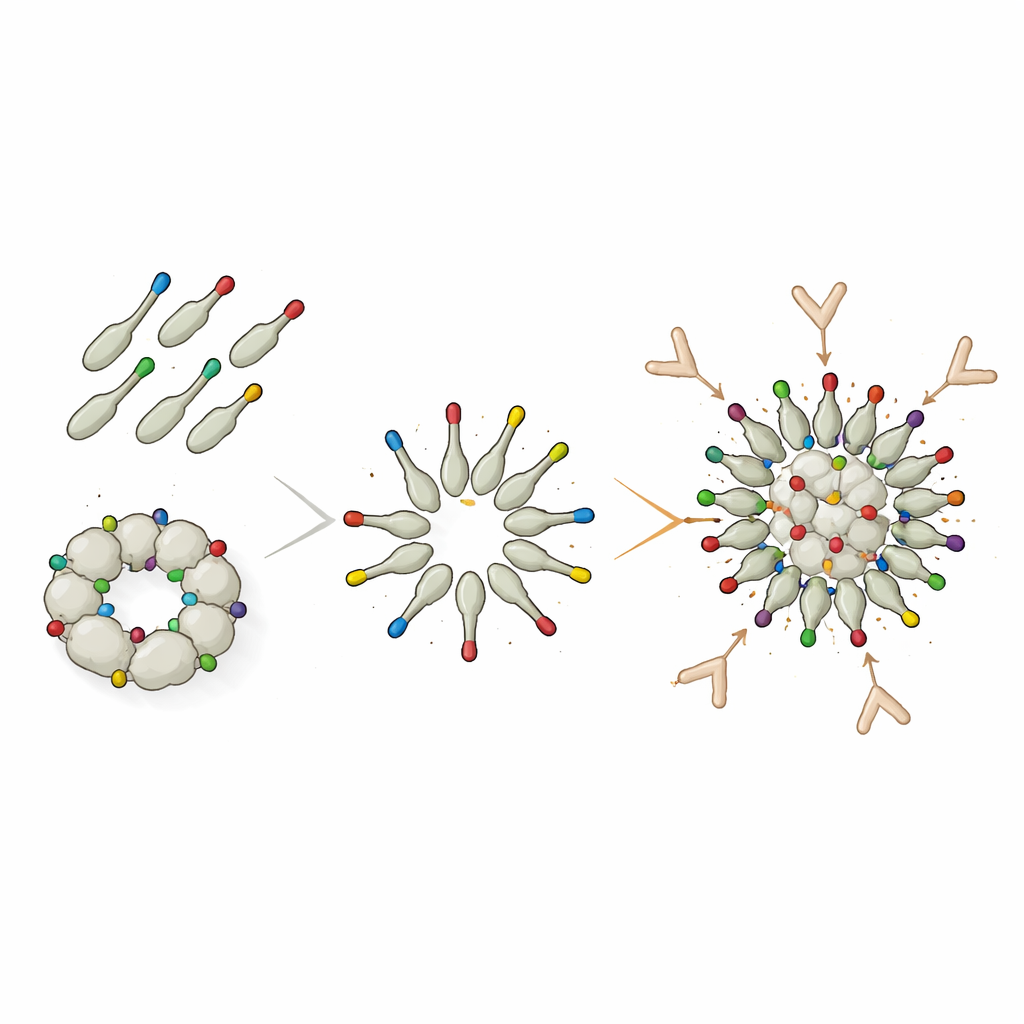
«Прищёлкивание» украшения резко усиливает ответы
Чтобы преодолеть эти структурные ограничения, команда перешла на модульную систему «белкового клея» DogTag/DogCatcher. В этой схеме dodecin сначала производили с лишь крошечным пептидом DogTag на поверхности, что позволяло ему свободно собираться в чистые наночастицы. Отдельно антиген Trx-8mer был сращён с соответствующим партнёром DogCatcher. При смешивании Tag и Catcher «защёлкиваются» через спонтанную ковалентную связь, прикрепляя единицы Trx-8mer с L2 к предварительно сформированным частицам dodecin. Хотя лишь около половины Trx-8mer в итоге прикреплялись к наночастицам, а остальная часть оставалась свободной в растворе, мыши, иммунизированные этим декорированным конструктом, выработали значительно более высокие титры нейтрализующих антител против нескольких онкогенных типов ВПЧ по сравнению с частицами прямого сращения. Для некоторых типов, например HPV16, декорированные частицы даже превосходили PANHPVAX.
Последствия для доступных и широких вакцин против ВПЧ
В целом исследование показывает, что расположение антигенов в пространстве может иметь большее значение, чем просто число копий на бумаге. Предварительная сборка прочного наночастичного скелета с последующим «прищёлкиванием» антигенов обеспечила более благоприятное расстояние и ориентацию фрагментов L2, что привело к более сильным и более широким антительным ответам у мышей. Поскольку частицы на основе dodecin малы, высоко термостабильны и производятся в бактериях, они представляют собой перспективные кандидаты для вакцин следующего поколения против ВПЧ, которые могли бы быть дешевле в производстве и менее зависимы от холодовой цепи. При дальнейшем совершенствовании и испытаниях эта модульная платформа может поддерживать вакцины, защищающие от многих типов ВПЧ в одном доступном уколе, и даже быть адаптирована для сочетания профилактических и терапевтических компонентов в одной наночастице.
Цитирование: Kaplan, E., Mariz, F.C., Zhao, X. et al. Assessment of Mycobacterium tuberculosis dodecin scaffold as a multimerization platform on the immunogenicity of HPV L2 antigens. Sci Rep 16, 9086 (2026). https://doi.org/10.1038/s41598-026-42678-7
Ключевые слова: вакцина против ВПЧ, наночастичный иммуноген, антиген L2, dodecin-скелет, конъюгация белка