Clear Sky Science · ru
Многоцентровое клинико‑патологическое исследование поражений спектра одонтогенной миксомы с использованием количественной патологии
Почему это важно для пациентов и стоматологов
Глубоко в челюстной кости редкие опухоли могут медленно расти месяцы или годы, прежде чем их обнаружат. Эти новообразования, называемые одонтогенной миксомой и миксофибромой, не являются раком, но они могут разрастаться, ослаблять кость и осложнять операцию. Долгое время патологи в основном оценивали их визуально, что приводило к расхождениям в описании и классификации одинаковых поражений в разных больницах. Это исследование внедряет мощные инструменты анализа изображений в работу с препаратами, показывая, как искусственный интеллект (ИИ) может помочь врачам видеть эти опухоли более четко и последовательно.
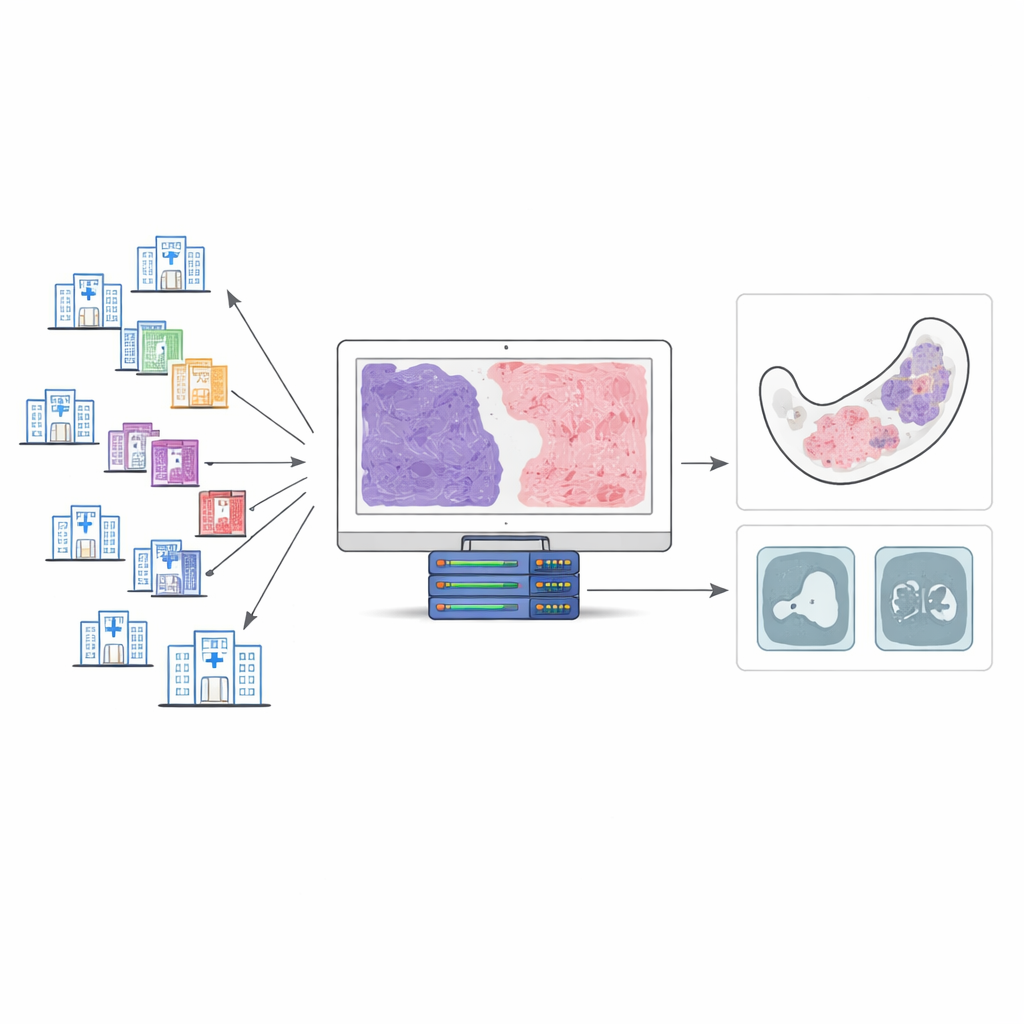
Редкие опухоли челюсти, которые внешне похожи друг на друга
Одонтогенная миксома и одонтогенная миксофиброма развиваются из тканей, участвующих в формировании зуба. Обе представляют собой мягкие, желеобразные образования, расположенные в толще челюстной кости. Под микроскопом они содержат смесь рыхлых миксоидных участков и более плотных фиброзных полос. Традиционно патологи пытались отличить их, оценивая, какая часть опухоли приходится на фиброзную ткань, а какая — на миксоидную. Но эти опухоли редки, и нет общепринятых правил о том, какого процента фиброзной ткани достаточно, чтобы изменить диагноз с одной категории на другую. В результате разные учреждения могут по‑разному называть очень похожие поражения, даже когда у пациентов схожи симптомы и результаты сканирования.
Преобразование препаратов в числа
Команда собрала 143 образца тканей у пациентов, лечившихся в 34 больницах в течение двух десятилетий, и в итоге сосредоточилась на 100 случаях, соответствовавших строгим критериям качества. Все образцы были окрашены специальным красителем (трихром Массона), который по‑разному окрашивает фиброзную ткань и окружающую опухоль. Два опытных челюстно‑лицевых патолога тщательно пересмотрели каждый случай и оценили процент фиброзной ткани с шагом 10%. Эти экспертные оценки послужили эталоном для обучения системы ИИ, которая должна была выполнять ту же задачу автоматически, но в полностью количественной форме.
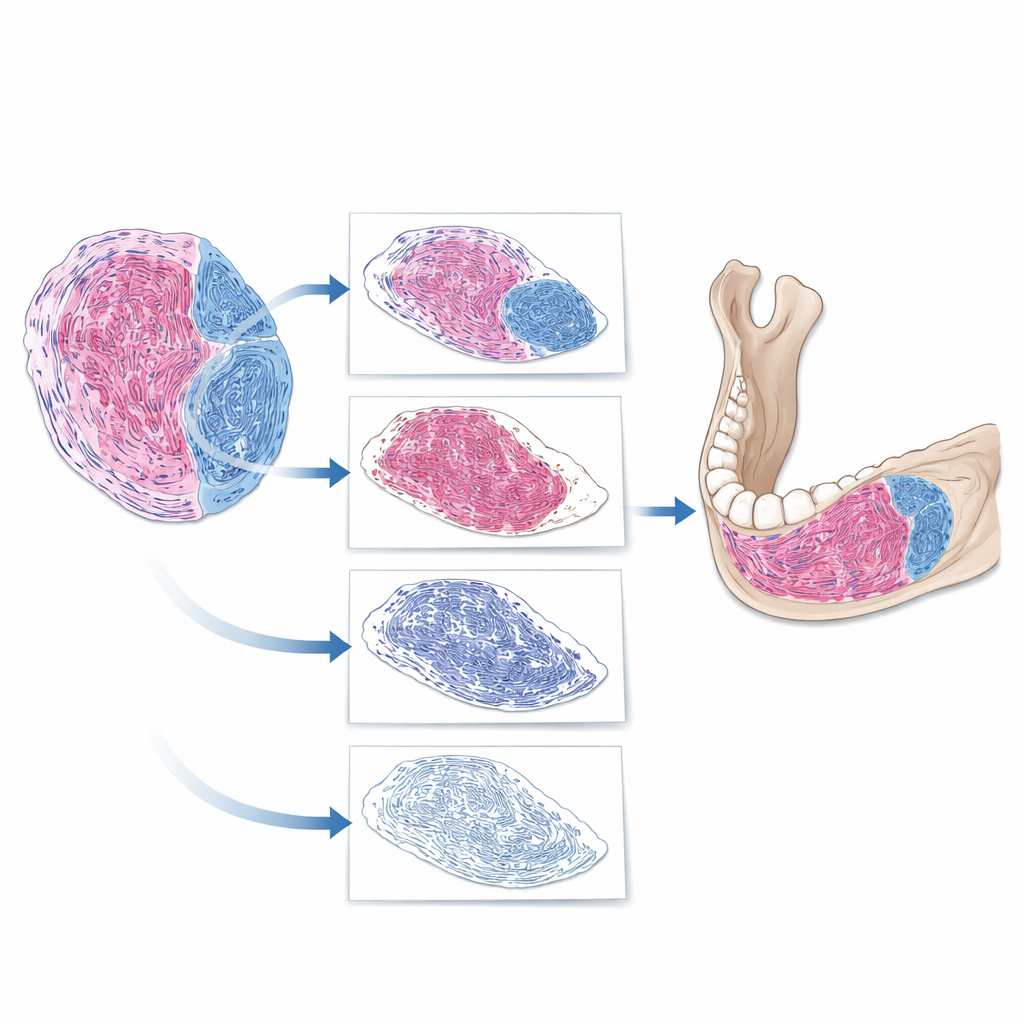
Как ИИ «читает» препарат опухоли
Исследователи построили пошаговый цифровой конвейер для анализа изображений целых срезов. Сначала программное обеспечение отделяло истинную ткань от пустого фона на препарате. Затем оно изолировало опухоль от соседних структур, таких как кость и зубы. Наконец, внутри опухоли система удаляла ядра клеток и фокусировалась на оставшемся матриксе, выявляя области, которые захватывали фиброзное окрашивание. На основе этого ИИ вычислял долю фиброзной ткани: площадь фиброзной ткани, деленная на общую площадь опухоли. При сравнении значений, полученных ИИ, с оценками экспертов согласие оказалось высоким: в большинстве отдельных случаев разброс составлял примерно 10 процентных пунктов. Это свидетельствует о том, что ИИ способен надежно отражать экспертное мнение, при этом выражая его в точных измерениях вместо приблизительных впечатлений.
Что структура фиброзной ткани говорит о внешнем виде опухоли
Имея эти измерения, исследователи изучили, как содержание фиброзной ткани связано с клиническими и радиологическими признаками. Они обнаружили, что доля фиброзной ткани существенно варьирует между учреждениями, что отражает различия в первоначальной маркировке опухолей патологами. При анализе характеристик изображений выделился один паттерн: опухоли, выглядящие на снимках как одиночная полость (унилоулярные поражения), как правило, имели более высокую долю фиброзной ткани, чем образования с несколькими мелкими перегородками (мультиулуярные поражения). Это согласуется с представлением о том, что более фиброзная, плотная ткань может формировать более сплошную, однокамерную массу, тогда как более рыхлая, богатая жидкостью ткань склонна распадаться на несколько полостей.
Что это означает для будущей диагностики и лечения
Исследование не ставит целью переименовать болезни или заменить патологов машинами. Оно показывает, что количественная патология на основе ИИ может обеспечить общую меру для редких опухолей челюсти в разных больницах. Превращая тонкие текстуры опухолевой ткани в воспроизводимые числа, этот подход выявляет, насколько повседневные диагнозы зависят от субъективной оценки, и предлагает способ уменьшить эту вариабельность. Для пациентов более согласованная интерпретация таких поражений может способствовать более четким решениям по лечению и лучшему сравнению исходов между центрами. По мере того как аналогичные методы будут применяться к другим редким опухолям, микроскопия с поддержкой ИИ может незаметно изменить то, как патологи видят болезни — сделав их оценки более сопоставимыми и, в конечном счете, более полезными независимо от места лечения пациента.
Цитирование: Harazono, Y., Fukawa, Y., Iwasaki, T. et al. Multicenter clinicopathological study of odontogenic myxoma spectrum lesions using quantitative pathology. Sci Rep 16, 11221 (2026). https://doi.org/10.1038/s41598-026-42019-8
Ключевые слова: одонтогенная миксома, опухоли челюсти, цифровая патология, искусственный интеллект, доля фиброзной ткани