Clear Sky Science · ru
Мультиэпитопная вакцина против нуклеопротеина и поли-белка оболочки батайского ортобуньявируса с использованием молекулярного докинга и молекулярно-динамических исследований
Почему важен малоизвестный вирус
Батайский ортобуньявирус — не общеизвестное название, но он незаметно распространяется через комаров по Европе, Африке и Азии, заражая людей и сельскохозяйственных животных. У скота он может вызывать выкидыши и пороки развития плодов, а у людей вызывает картины от гриппоподобной лихорадки до, в редких случаях, воспаления мозга и нарушений свертываемости крови. При этом лицензированной вакцины нет, а тестирование очень ограничено. В этом исследовании использованы компьютерные инструменты для проектирования чернового варианта вакцины первого поколения, который после последующих лабораторных работ мог бы помочь защитить людей и животных от этой недооценённой угрозы.
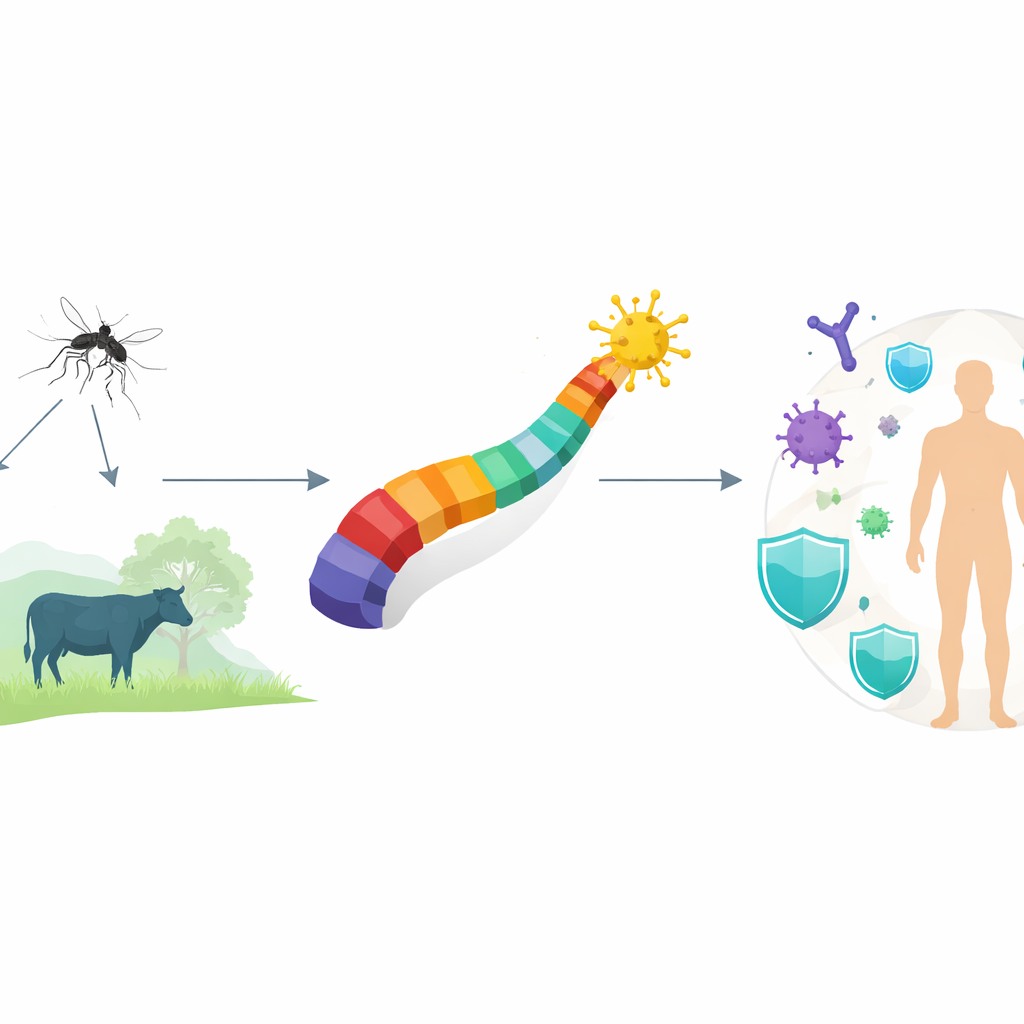
Как вирус распространяется и почему его пропускают
Вирус передаётся в основном обычными комарами, которые также переносят более знакомые инфекции, такие как малярия и денге. Поскольку инфекции Батая часто напоминают обычную лихорадку или простуду, врачи редко заподозривают его, а стандартные диагностические панели обычно на него не тестируют. Наблюдение за комарами и сельскохозяйственными животными ведётся фрагментарно, поэтому вспышки могут тлеть незамеченными. Авторы полагают, что сочетание широкого географического распространения, влияния на размножение скота и недодиагностики делает батайский ортобуньявирус тихой, но значимой проблемой общественного и ветеринарного здравоохранения.
Создание вакцины из модульных фрагментов
Вместо работы с цельным вирусом исследователи сосредоточились на двух его ключевых белках: нуклеопротейне, который участвует в упаковке вирусного генетического материала, и поли-белке оболочки, составляющем часть внешней оболочки вируса. С помощью онлайн-баз данных и серверов предсказания они просканировали эти белки в поисках коротких участков — эпитопов — которые иммунные клетки с наибольшей вероятностью распознают. Отбирали эпитопы, предсказанные как способные вызвать сильный иммунный ответ, избегая при этом участков, способных вызвать аллергию или токсичность. Эти фрагменты затем были цифровым образом сшиты вместе, разделены гибкими «линкерами» и объединены с небольшим иммуноповышающим сегментом — адувантом, образовав единый полипептид из 247 аминокислот, служащий предложенной конструкцией вакцины.
Тестирование конструкции внутри компьютера
Имея последовательность аминокислот, команда проверила, будет ли этот искусственный белок вести себя как реалистичный кандидат в вакцины. Вычислительные инструменты показали, что он должен быть стабильным, гидрофильным и легко воспроизводимым в бактериях, обычно используемых для производства вакцин. Предсказанная трёхмерная структура прошла стандартные проверки качества для белковых моделей. Важное значение имело моделирование взаимодействия конструкции с человеческим рецептором врождённого иммунитета Toll-like receptor 3 — молекулой, помогающей клеткам обнаруживать вирусный материал: моделируемый докинг был тесным и образовал множество стабилизирующих контактов. Молекулярно-динамическое моделирование на 100 наносекунд показало, что комплекс оставался целостным и компактным, что говорит о потенциальной прочности взаимодействия в реальных клетках.
Смогла бы она обеспечить широкую защиту?
Далее авторы спросили, ответит ли на эту конструкцию население по всему миру. Они использовали инструмент оценки охвата популяции, который сопоставляет выбранные эпитопы с распространёнными вариантами генов иммунной системы человека. Анализ показал, что более 97 процентов мирового населения несут по крайней мере один вариант гена, способный распознать участки конструкции, что указывает на широкое теоретическое покрытие. Модель иммунного ответа предсказала сильные волны антител, активацию вспомогательных и цитотоксических Т-клеток, формирование иммунной памяти и вовлечение факторов врождённого иммунитета, таких как естественные киллеры и макрофаги. В виртуальной модели конструкция, по крайней мере, способна вызвать оба плеча иммунного ответа: антителозависимый и клеточно-опосредованный.
Что означает эта работа для дальнейших шагов
Это исследование не даёт готовой вакцины, а представляет собой тщательно спроектированную отправную точку. Все многообещающие результаты — хорошая стабильность, широкое предсказанное покрытие популяции и сильные смоделированные иммунные ответы — получены с помощью компьютерных моделей. Следующие шаги — строго экспериментальные: получение белка в лаборатории, проверка его безопасности и оценка, действительно ли он защищает животных и, в конечном счёте, людей от инфекции Батая. Если будущие работы подтвердят эти прогнозы, описанный здесь мультиэпитопный дизайн может стать основой первой специализированной вакцины против этого забытого вируса, передаваемого комарами.
Цитирование: Naveed, M., Asim, M., Ali, A. et al. Multi-epitope vaccine against nucleoprotein and envelopment polyprotein of Batai orthobunyavirus using molecular docking and molecular dynamics studies. Sci Rep 16, 8973 (2026). https://doi.org/10.1038/s41598-026-41964-8
Ключевые слова: вирус Батай, заболевание, передающееся комарами, вакцина на основе эпитопов, вычислительная вакцинология, мультиэпитопный дизайн