Clear Sky Science · ru
Визуализация злокачественного прогрессирования: пространственный иммунофлуоресцентный анализ in situ на основе CD109 отображает переход папиллярной карциномы щитовидной железы в анапластическую внутри микроокружения опухоли
Почему это исследование рака щитовидной железы важно
Анапластическая карцинома щитовидной железы — один из самых смертоносных видов рака у людей: она способна превратить обычно излечимую опухоль щитовидной железы в быстро летальное состояние. Врачи по-прежнему не полностью понимают, как обычная, медленно растущая папиллярная карцинома может внезапно превратиться в эту агрессивную форму. В этом исследовании авторы проследили такое превращение непосредственно внутри опухоли пациента, применив новый метод визуализации, чтобы наблюдать, как клетки рака и их окружение меняются шаг за шагом. Работа дает более детальную картину того, как местные условия в опухоли могут подтолкнуть клетки к более смертоносному состоянию, указывая на новые подходы к замедлению или предотвращению этого перехода.
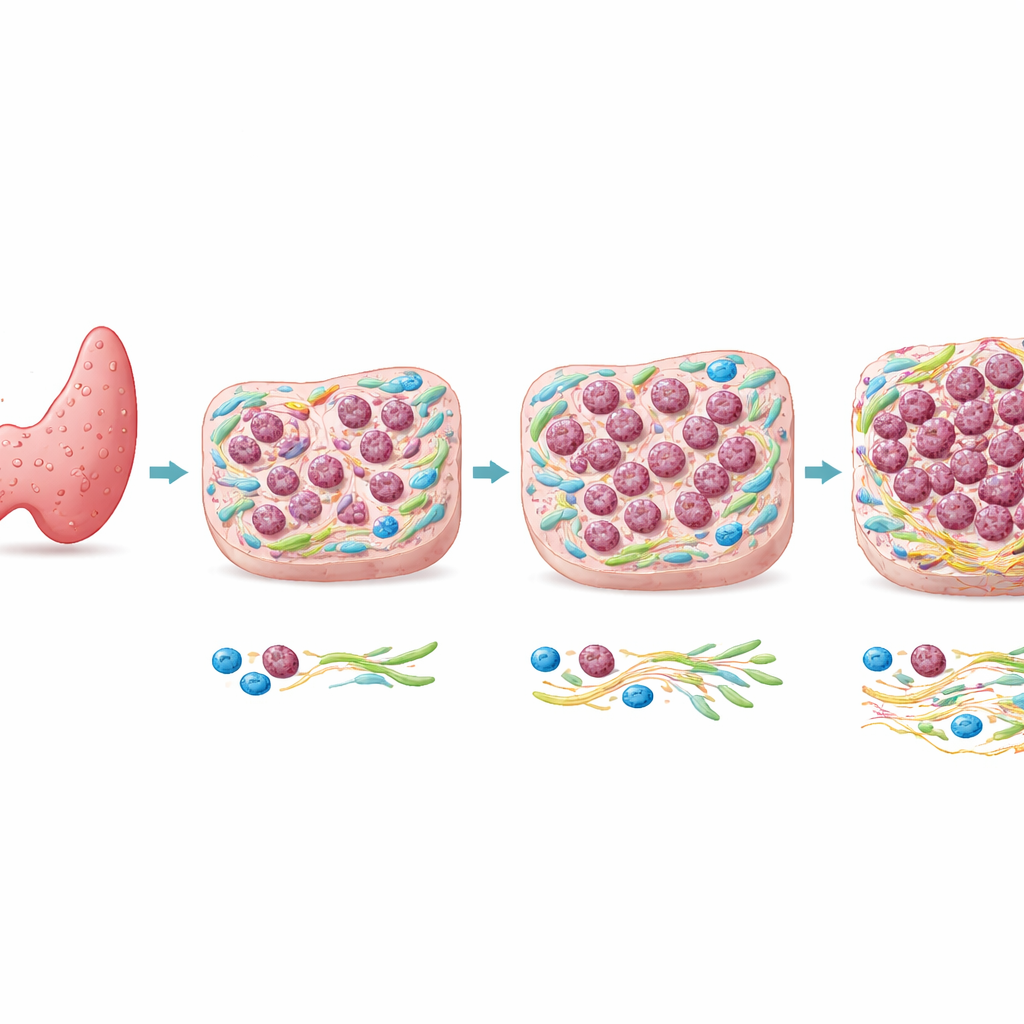
От распространенной опухоли к редкому убийце
Большинство раков щитовидной железы — это папиллярные карциномы (PTC), которые обычно растут медленно и дают отличные прогнозы. Анапластическая карцинома щитовидной железы (ATC), напротив, редка, но часто приводит к смерти в течение нескольких месяцев. Генетические исследования показали, что ATC и прилегающие участки PTC у одного пациента часто имеют множество одинаковых мутаций в ДНК, включая изменения в известных онкогенах. Это сходство указывает на то, что только генетических факторов может быть недостаточно для объяснения того, почему анапластическими становятся лишь некоторые области опухоли. Авторы поэтому сосредоточились на том, что происходит в тканевом окружении клеток — микроокружении опухоли — чтобы выяснить, способствуют ли местные условия этому опасному сдвигу.
Новый способ картирования рака in situ
Исследователи разработали пространственный иммунофлуоресцентный (SPI) анализ — вид многокрасной микроскопии, который измеряет интенсивность конкретных белков в крошечных заданных плитках на поперечном срезе ткани. Они сосредоточили метод на CD109, белке на поверхности, который выявили как маркер злокачественного поведения в ткани щитовидной железы, и на CK8/18, белке, характерном для обычных папиллярных опухолевых клеток. Вычисляя отношение CD109 к CK8/18 в сотнях мелких областей, они создали цветовые карты, которые отделяли явные участки PTC от явных участков ATC и, что важно, показывали промежуточные зоны, где оба маркера пересекались. Вместо резкой границы переход от папиллярной к анапластической форме выглядел как постепенный, пятнистый континуум.
Пять зон на пути изменений
Чтобы лучше понять этот континуум, исследователи разделили ткань на пять регионов — от чистого PTC до полностью сформированной ATC. Затем они исследовали множество дополнительных белков, отражающих идентичность клеток, пролиферацию, подвижность и состояние опорной ткани. По мере продвижения через эти регионы классические эпителиальные признаки, такие как E-кадгерин и CK8/18, постепенно снижались, тогда как маркеры, связанные с подвижностью клеток и изменением формы, например виментин, увеличивались. Белки, указывающие на быстрый клеточный дележ, росли в более анапластических зонах. В то же время окружающие клетки поддержки — фибробласты, ассоциированные с опухолью, и иммунные клетки, особенно определенные макрофаги — становились более многочисленными и более активированными, а белки, которые они продуцировали, также увеличивались.
Когда каркас опухоли становится враждебным
Резкое изменение произошло в «скелете» опухоли — внеклеточном матриксе. В анапластических областях клетки, похожие на фибробласты, откладывали больше коллагенов типов III и VI и матриксного белка TGFBI; эти волокна были толще, более запутанными и ориентированы в разных направлениях, а не в плавных параллельных линиях. Такая перестроенная сеть, вероятно, делает ткань механически более жесткой. В этих более жестких зонах давление-чувствительный сигнальный белок YAP был более активен как в раковых, так и в опорных клетках. Те же области демонстрировали больше признаков повреждения ДНК и формы воспалительной клеточной смерти, вместе с выбросом белков семейства S100, которые могут выступать в роли сигналов опасности и усиливать воспаление. Авторы предполагают, что сочетание компрессии, гибели клеток и хронического воспаления способствует выживанию и распространению уже мутировавших клеток, которые способны выдерживать стресс и переживать процесс, сходный с эпителиально-мезенхимным переходом.
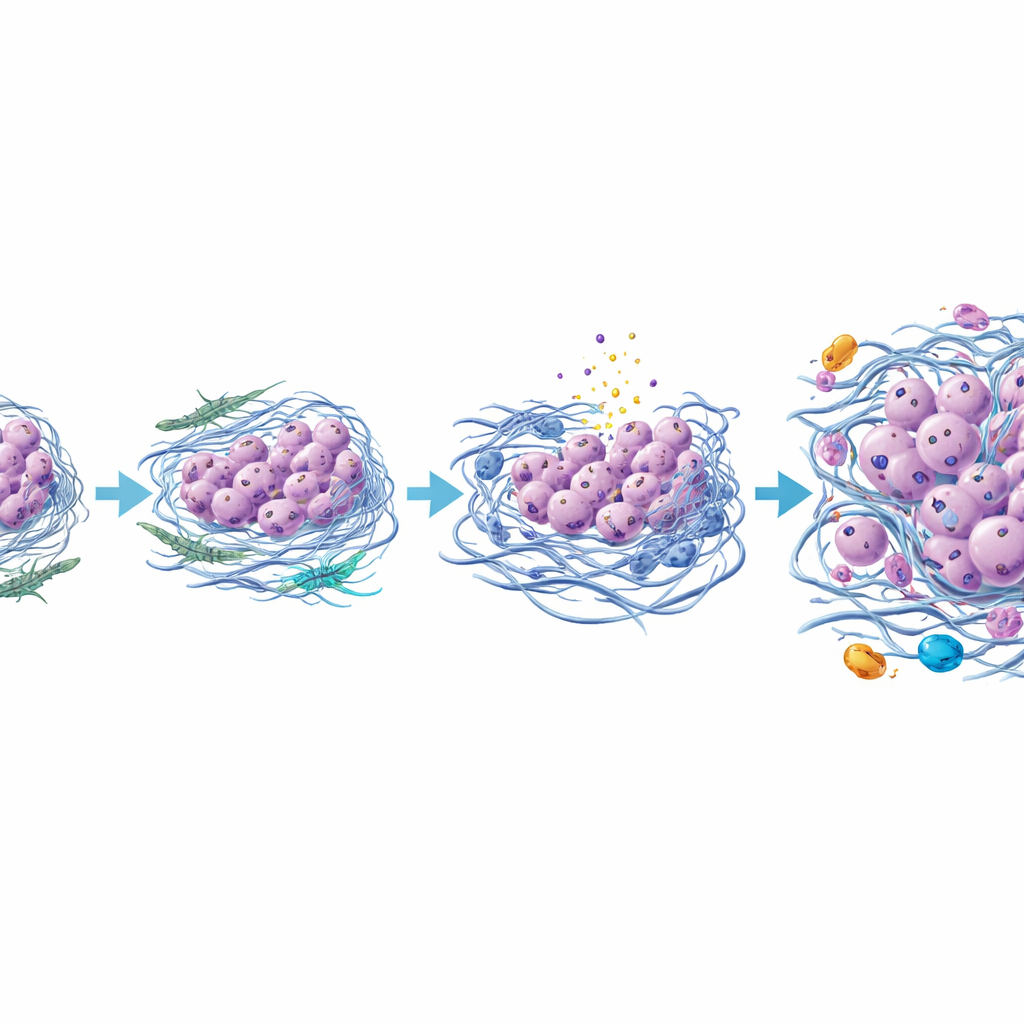
Новая картина превращения опухоли щитовидной железы в летальную
Собрав эти данные вместе, исследование показывает, что анапластическая карцинома щитовидной железы возникает не только из дополнительных генетических мутаций, но и из измененного окружения вокруг опухоли. По мере взаимодействия папиллярных опухолевых клеток и соседних клеток поддержки некоторые фибробласты переходят в более агрессивный тип, утолщая и уплотняя матрикс, сдавливая уязвимые клетки до гибели и привлекая воспалительные иммунные клетки. Выжившие, более устойчивые раковые клетки постепенно теряют свои исходные тиреоидные признаки и приобретают более подвижную, инвазивную идентичность, в конце концов формируя анапластическую опухоль. Хотя работа основана на одном детально изученном случае и требует подтверждения на большем числе пациентов, она вводит мощный инструмент визуализации и подробную модель, в которой нацеливание на клетки поддержки опухоли, матрикс или воспалительные сигналы может помочь предотвратить или отложить один из самых опасных переходов при раке щитовидной железы.
Цитирование: Cohen, T., Suzuki, K., Matsuda, K. et al. Visualizing malignant progression: in situ CD109-based spatial immunofluorescence assay delineates papillary to anaplastic thyroid carcinoma transformation within the tumor microenvironment. Sci Rep 16, 8682 (2026). https://doi.org/10.1038/s41598-026-41927-z
Ключевые слова: анапластическая карцинома щитовидной железы, папиллярная карцинома щитовидной железы, микроокружение опухоли, жесткость внеклеточного матрикса, пространственная иммунофлуоресценция