Clear Sky Science · ru
Сочетание микрoРНК ткани с клиническими моделями риска для прогноза рецидива ГЦК после трансплантации печени: пилотное исследование
Почему это исследование важно для пациентов и их семей
Рак печени — один из самых смертоносных видов рака в мире, и для некоторых пациентов единственный реальный шанс на излечение — получить новую печень. Даже после трансплантации опухоль может вернуться в пересаженном органе, что укорачивает жизнь и расходует дефицитные донорские органы. В этом исследовании изучают, могут ли крошечные молекулы внутри удалённой опухоли, называемые микроРНК, помочь врачам лучше предсказывать, у кого наиболее вероятен рецидив после трансплантации, чтобы последующее наблюдение можно было точнее адаптировать к нуждам конкретного пациента.
Более подробный взгляд на рак печени после трансплантации
Гепатоцеллюлярная карцинома, самая распространённая форма первичного рака печени, часто развивается у людей с длительно существующим поражением печени по причинам, таким как злоупотребление алкоголем, вирусные гепатиты или жировая болезнь печени. При небольших опухолях, которые нельзя безопасно удалить резекцией, трансплантация печени даёт мощный двойной эффект: она замещает рубцовую печень и одновременно удаляет опухоль. Поскольку донорские органы ограничены, центры трансплантации руководствуются жёсткими правилами, основанными в основном на размере и числе опухолей — известными критериями Милана и UCSF — чтобы выбрать тех, кто, вероятно, получит наибольшую пользу. Тем не менее даже при соблюдении этих правил у 8–20% пациентов опухоль возвращается, что показывает: одни только размеры не отражают всю агрессивность конкретной опухоли.
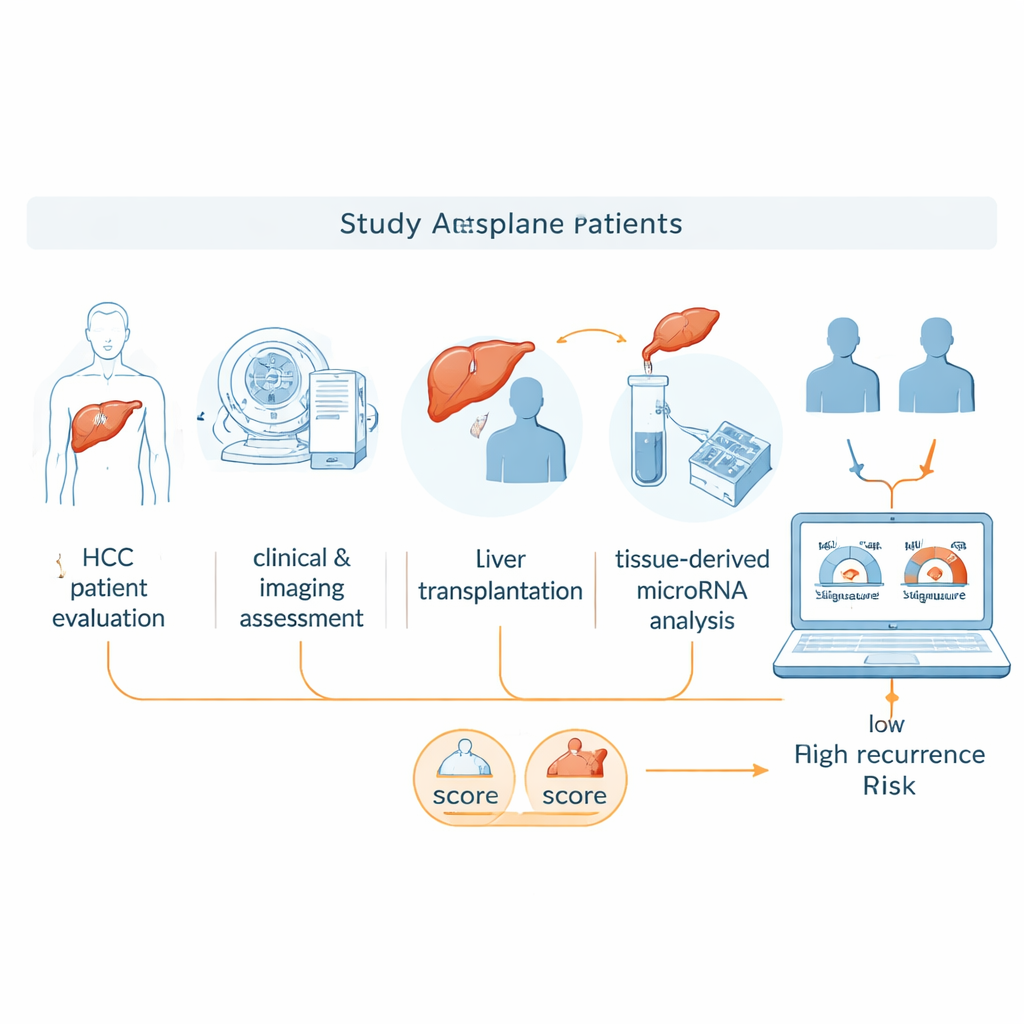
Крошечные РНК с большим потенциалом
МикроРНК — короткие фрагменты генетического материала, которые сами по себе не кодируют белки, но помогают регулировать включение и выключение других генов. Разные опухоли могут иметь собственные микроРНК‑«отпечатки», и эти закономерности могут показывать, насколько быстро растёт опухоль или какова её склонность к метастазированию. В этом пилотном исследовании учёные проверяли, можно ли взять микроРНК из ткани рака печени, удалённой во время трансплантации, и совместить их с существующими клиническими правилами, чтобы улучшить прогноз рецидива. Они сосредоточились на образцах ткани, консервированных в парафине — рутинном методе, применяемом в больницах, — чтобы оценить, насколько такое молекулярное тестирование практично в реальных условиях.
Как проводилось исследование
Команда проанализировала 20 пациентов, которым выполняли трансплантацию печени по поводу рака в период с 2007 по 2021 год. У половины из них после трансплантации произошёл рецидив, у другой половины рецидива не было в течение как минимум пяти лет. Всем пациентам перед операцией проводили стандартные клинические оценки и КТ‑исследования. Из удалённой опухоли у каждого пациента извлекали РНК и измеряли активность примерно 3 600 микроРНК с помощью микрочипа. Сначала искали микроРНК с выраженными различиями между группами с рецидивом и без него, затем сужали список по статистической значимости и по наличию предыдущих свидетельств связывания отдельных микроРНК с поведением рака печени.
ТрёхмикроРНК‑сигнал тревоги
В результате был выделен один сильно информативный микроРНК, называемый miR‑3692‑5p, уровень которого был заметно ниже у пациентов, у которых позднее произошёл рецидив. Ещё две микроРНК — miR‑424 и miR‑718 — были добавлены, поскольку предыдущие исследования связывали их с исходами при раке печени, и они демонстрировали похожее снижение в группе рецидива. Вместе это трио образовало «3‑miRNA-подпись», которая сама по себе уже довольно точно различала рецидив и отсутствие рецидива в этой небольшой выборке. Когда исследователи наложили эту микроРНК‑подпись поверх четырёх обычно используемых клинических моделей, включая критерии Милана и UCSF и показатель AFP по крови, комбинированные модели предсказывали рецидив намного лучше, чем одни лишь клинические правила.
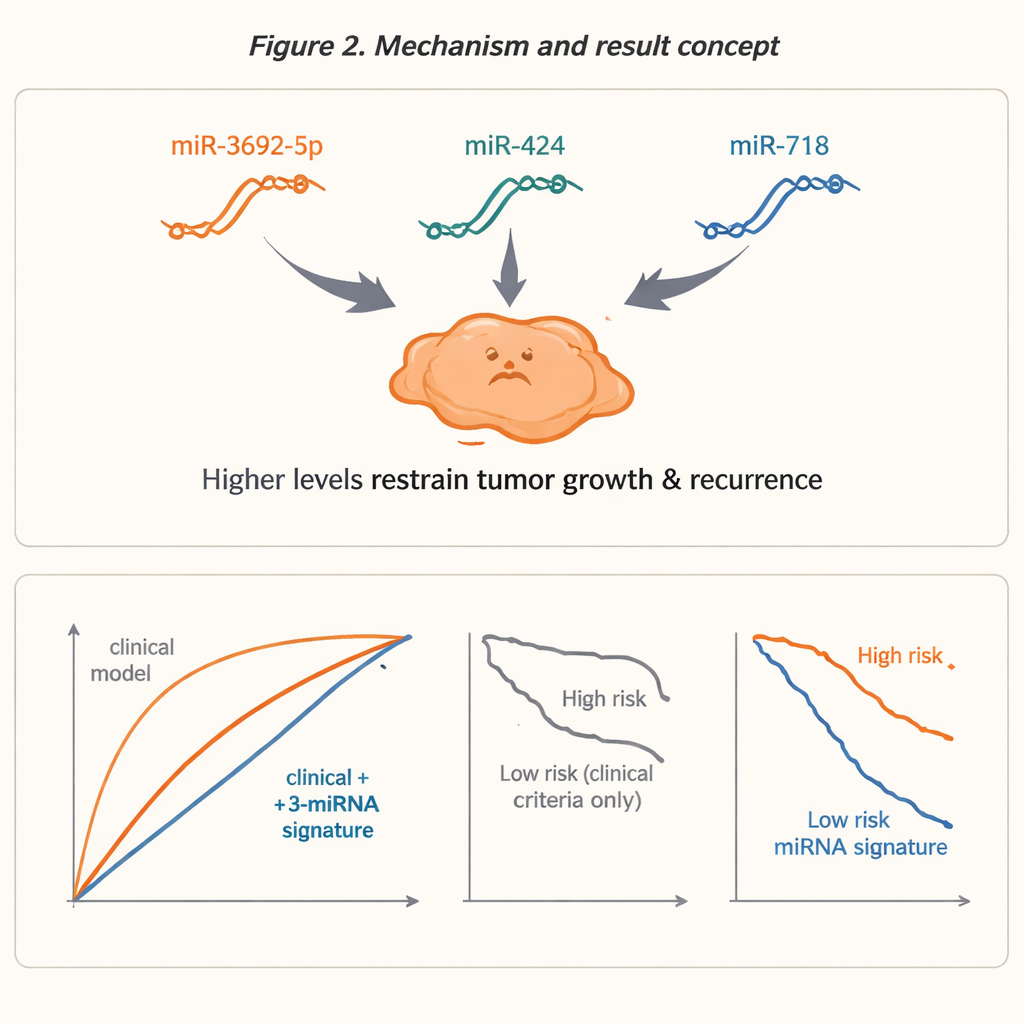
Как выглядит лучшее предсказание на практике
Для оценки эффективности команда использовала стандартные статистические инструменты, измеряющие, насколько хорошо тест разделяет пациентов на группы с высоким и низким риском. Клинические модели сами по себе лишь умеренно отличали эти группы. После добавления трёх микроРНК предсказательная способность заметно возросла, при этом показатели точности приближались к 0,94–0,96 на шкале, где 1,0 соответствует идеальному тесту. Улучшенные модели перевели примерно половину пациентов в другие категории риска, что указывает на то, что многих людей, сейчас помечаемых как «безопасные» или «высокого риска», можно неверно классифицировать, если опираться только на правила, основанные на размере. Важно, что пациенты, обозначенные как высокорисковые по комбинированным моделям, имели существенно более короткое время безрецидивной выживаемости — примерно 17 месяцев против 38,5 месяцев в одном из примеров — что показывает, что эти молекулярные сигналы действительно коррелировали с реальными исходами.
Что это значит для будущей помощи
Для неспециалистов основная мысль такова: изучение «сигналов управления» внутри опухоли, здесь представленных тремя конкретными микроРНК, может раскрыть её истинную природу лучше, чем одни только размер или количество очагов. Поскольку это было небольшое исследование предварительного характера, которое требует подтверждения в более крупных многоцентровых когортах и в образцах, доступных легче (например, в крови), оно демонстрирует техническую осуществимость тестирования на рутинных тканях, хранящихся в больницах. В случае валидации такой подход может помочь трансплантационным командам разумнее выбирать режимы наблюдения и терапевтические стратегии, концентрируя наиболее интенсивный контроль и профилактические меры на тех, чьи опухоли несут молекулярные признаки вероятного возвращения, и, в то же время, потенциально избавляя пациентов низкого риска от ненужных тестов.
Цитирование: Lederer, T., Lehr, K., Bobe, S. et al. Combining tissue-derived microRNAs with clinical risk models for prediction of HCC recurrence after liver transplantation: A proof-of-concept study. Sci Rep 16, 7742 (2026). https://doi.org/10.1038/s41598-026-41688-9
Ключевые слова: рак печени, трансплантация печени, биомаркеры микроРНК, риск рецидива рака, персонализированная онкология