Clear Sky Science · ru
Гибридная настроенная модель глубокого обучения для диагностики рака молочной железы на основе генетических данных
Почему это важно для пациентов и их семей
Рак молочной железы теперь является самым часто диагностируемым видом рака у женщин во всем мире, и раннее обнаружение часто решает вопрос жизни и смерти. Врачам все чаще доступна генетическая информация пациента, но превращение десятков тысяч измерений активности генов в понятные ответы чрезвычайно сложно. В этой работе описана новая компьютерная модель, которая считывает эти сложные генетические паттерны, чтобы обнаруживать рак молочной железы и прогнозировать исходы с впечатляющей точностью, потенциально предоставляя клиницистам мощного помощника для более ранних и надежных решений.
От генов к предупредительным признакам
Каждая опухоль молочной железы несет молекулярный отпечаток, закодированный в активности тысяч генов. Авторы поставили задачу создать систему, которая могла бы напрямую читать этот отпечаток, а не полагаться только на изображения или на небольшой набор известных генов, таких как BRCA1 и BRCA2. Они работали с двумя крупнейшими общедоступными ресурсами по геномике рака: когорте TCGA по раку молочной железы, где представлена активность 17 814 генов в 590 образцах, и исследованием METABRIC, содержащим геномные и клинические данные более чем для 1 400 пациентов. Их цель была амбициозна: разработать метод, способный обработать этот поток данных, найти наиболее информативные сигналы и при этом надежно работать на полностью независимых группах пациентов.
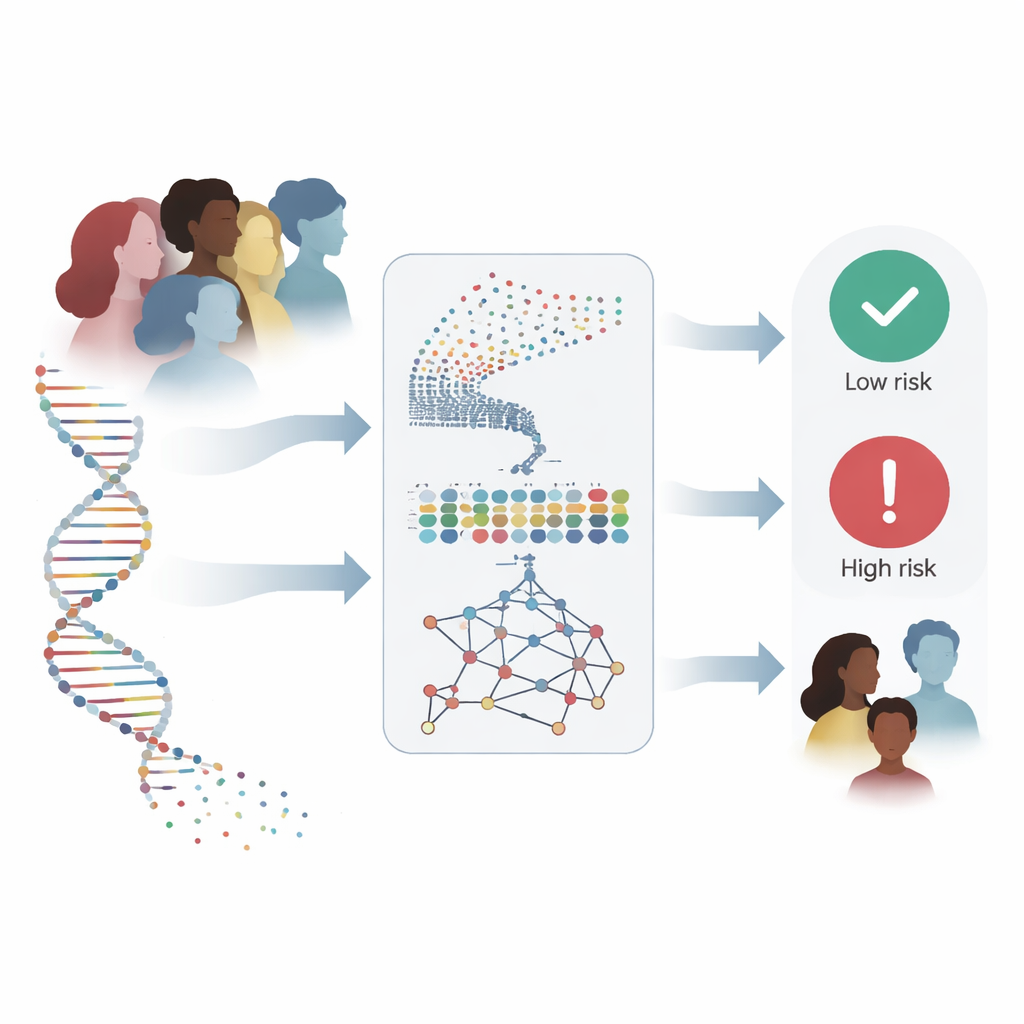
Сведение тысяч генов к полезному набору
Одновременный анализ почти восемнадцати тысяч генов подавляет даже продвинутые алгоритмы и повышает риск улавливания бессмысленного шума. Поэтому исследователи использовали двухступенчатое «сито», чтобы выделить меньший набор действительно информативных генов. Сначала они применили метод Random Forest, который с помощью множества деревьев решений определяет, какие гены важны для разделения раковых и здоровых образцов. Этот шаг сократил список до 436 перспективных генов. Затем они изучили совместное поведение этих генов с помощью поиска ассоциативных правил — метода, выявляющего группы генов, которые склонны проявляться одновременно в опухолях. Этот дополнительный слой анализа выявил пары и сети генов, связанные с ключевыми процессами рака, такими как быстрый дележ клеток, восстановление повреждений ДНК и изменения окружения ткани вокруг опухоли. После этой фильтрации осталось 332 гена — по-прежнему насыщенные биологическим смыслом, но гораздо более управляемые для углубленного анализа.
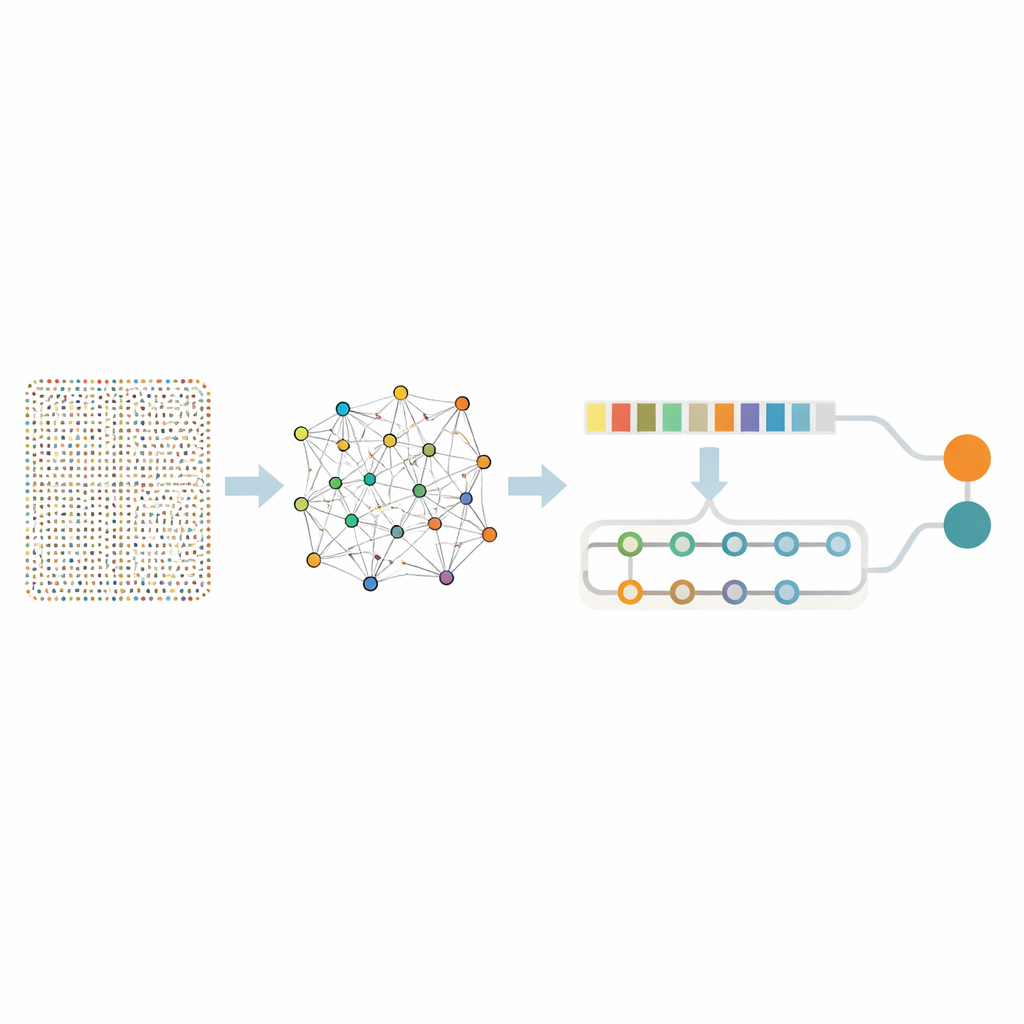
Двухчастная нейронная сеть, которая изучает паттерны и контекст
Имея этот сфокусированный набор генов, команда построила гибридную модель глубокого обучения, объединяющую два типа нейронных сетей. Одна часть, сверточная сеть, сканирует список генов, улавливая локальные паттерны — кластеры генов, которые склонны повышаться или понижаться одновременно. Вторая часть, двунаправленная сеть с памятью, рассматривает ту же информацию с учётом дальнодействующих взаимосвязей, фиксируя, как отдалённые гены влияют друг на друга по всему профилю. Перед обучением авторы уравновесили данные, чтобы образцы рака и не-рака были представлены справедливо, и добавили небольшое количество искусственного шума, обучая модель не поддаваться случайным флуктуациям.
Как система показала себя в реальных проверках
При обучении и тестировании на данных TCGA гибридная сеть с точностью примерно 97% корректно различала опухолевые и нормальные образцы и продемонстрировала почти идеальную способность разделять эти две группы. Важно, что она превосходила более простые настройки глубокого обучения и стандартные методы машинного обучения, такие как логистическая регрессия и машины опорных векторов, даже когда эти конкурирующие методы получали тот же тщательно отобранный набор генов. Самым строгим испытанием было проверить, выдержит ли модель полностью другую базу данных. При применении к METABRIC, собранной в других больницах и с использованием различных лабораторных методов, система сохранила высокую эффективность: в лучшем прогоне она достигла 99,3% точности и корректно идентифицировала каждого пациента, который позднее скончался от рака молочной железы — критическое свойство для инструмента, предназначенного для отметки групп высокого риска.
Что это может значить для будущего ухода
Для неспециалиста главный вывод таков: это исследование предлагает умный фильтр и интерпретатор генетических данных, который может надежно выявлять рак молочной железы и связанный с ним риск в больших группах пациентов. Сочетая продуманную стратегию выбора генов с двухветвевой нейронной сетью, авторы демонстрируют, что компьютеры способны извлекать клинически значимые сигналы из огромных генетических наборов данных не только в одном исследовании, но и в независимых когортах. Хотя требуется дополнительная работа для проверки метода в разнообразных популяциях и для подробного объяснения его решений, подход указывает на будущее, в котором простой образец крови или ткани может быть введён в такие модели и помочь врачам обнаруживать опухоли раньше и точнее подбирать лечение.
Цитирование: Hesham, F., Abbassy, M.M. & Abdalla, M. Hybrid tuned deep learning model for breast cancer diagnosis using genetic data. Sci Rep 16, 9664 (2026). https://doi.org/10.1038/s41598-026-41643-8
Ключевые слова: геномика рака молочной железы, диагностика с помощью глубокого обучения, биомаркеры экспрессии генов, раннее выявление рака, поддержка клинических решений