Clear Sky Science · ru
Оценка метагеномики длинных ридов для диагностики инфекций крови: пилотное исследование из тайской тertiарной больницы
Почему важны более быстрые тесты на инфекцию крови
Когда бактерии попадают в кровоток, каждое час имеет значение. Врачам нужно быстро выбрать правильный антибиотик, но современные лабораторные тесты могут занимать несколько дней, чтобы выявить возбудителя и определить, какие препараты, вероятно, окажутся неэффективными. Это исследование из крупной тайской больницы изучает новый способ ускорить процесс — чтение генетического материала всех микробов в образце крови одновременно с помощью портативного секвенсора ДНК. Цель — перейти от ожидания ответов в течение нескольких дней к получению детальной картины инфекции в пределах одной рабочей смены.
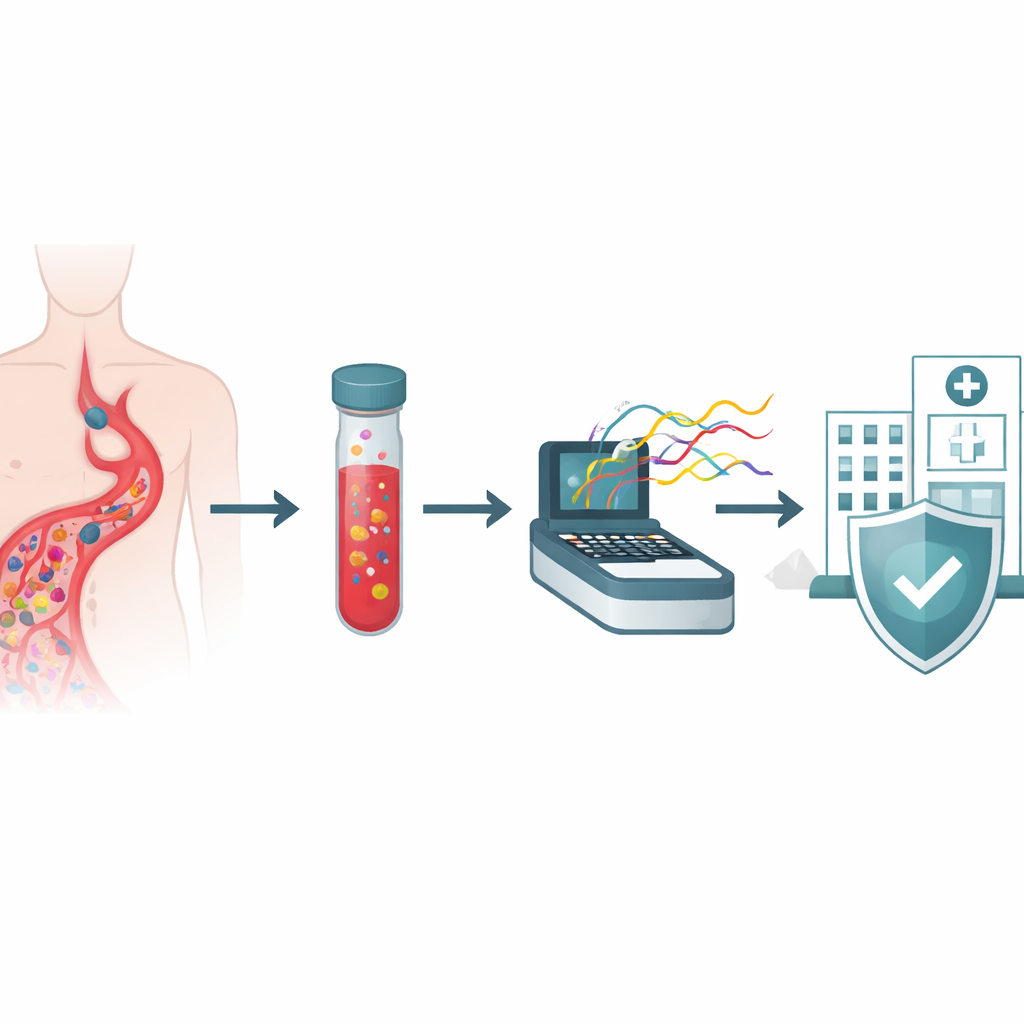
Новый способ «читать» микробы в крови
Исследователи сосредоточились на пациентах, у которых стандартные бутылочки для посева крови уже показали бактериальный рост — такие бутылочки рутинно используются в больницах по всему миру. Вместо того чтобы выращивать каждую бактерию на отдельных чашках и проводить серию химических тестов, они отобрали жидкость непосредственно из 40 положительных бутылочек и извлекли всю микробную ДНК. Эту ДНК затем пропустили через секвенсор Oxford Nanopore — устройство, которое протягивает длинные нити генетического материала через крошечные поры и считывает их последовательность в реальном времени. Поскольку метод не зависит от отдельного выращивания организмов, в принципе он может обнаруживать множество видов, их механизмы устойчивости к лекарствам и факторы вирулентности в одном упрощённом рабочем процессе.
Что обнаружили в инфекциях крови в Таиланде
Традиционные анализы тех же 40 образцов дали 45 бактериальных выделений, что отражает наличие у некоторых пациентов смешанных инфекций более чем одним видом. Обычная система VITEK показала, что два знакомых кишечных вида — Escherichia coli и Klebsiella pneumoniae — вызвали почти 40% этих инфекций, и что многие из штаммов были устойчивы к нескольким препаратам. Подход на основе нанопоров в целом подтвердил эту картину, идентифицировав 43 различных бактериальных генома и подтвердив доминирование представителей группы Enterobacterales. Он также обнаружил несколько редких или неправильно классифицированных видов, таких как экологическая бактерия Ralstonia mannitolilytica и желудочный возбудитель Campylobacter jejuni, которые рутинные методы пропустили или определили лишь в общих чертах. В некоторых смешанных инфекциях секвенирование, однако, испытывало трудности с полной дифференциацией близкородственных микробов, когда один вид присутствовал на значительно более низком уровне, чем другой.
Взгляд на устойчивость и скрытые тактики
Поскольку новый метод читает длинные участки ДНК, он может делать больше, чем просто называть бактерии: он может выявлять генетические механизмы, которые помогают им сопротивляться антибиотикам и вызывать болезнь. Команда просканировала геномы в поисках известных генов резистентности и «факторов вирулентности», которые помогают микроорганизмам прикрепляться к тканям, образовывать защитные биопленки, захватывать железо или производить токсины. У E. coli и K. pneumoniae обнаружилось много таких генов, включая те, которые нейтрализуют ключевые группы антибиотиков, такие как бета-лактамы и аминогликозиды. Секвенирование также выявило мощные наборы сопротивления у госпитально устойчивых видов, таких как Acinetobacter baumannii и Pseudomonas aeruginosa, чьи геномы были богаты системами выброса препаратов и другими защитными механизмами. В то же время у некоторых более редких бактерий кровотока арсеналы были относительно скромными, что указывает на меньшую, но всё же значимую угрозу. 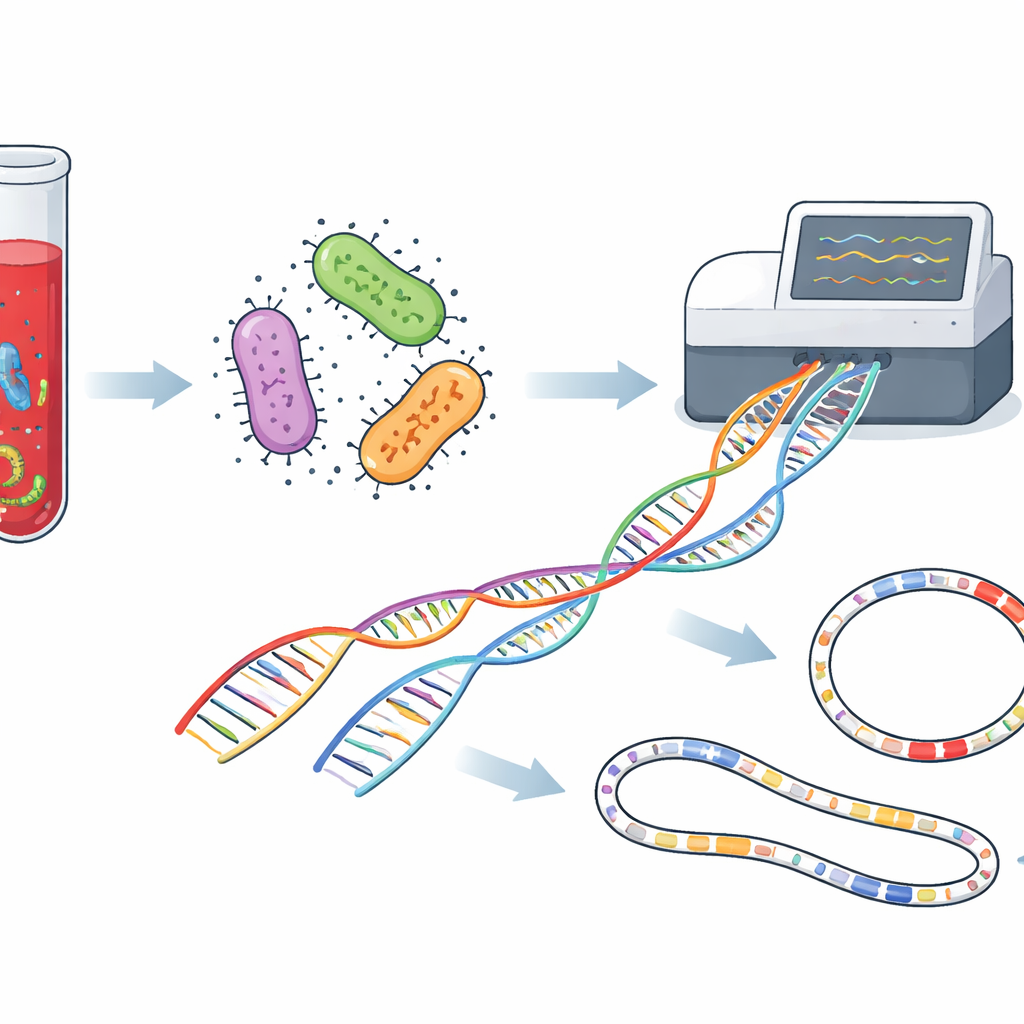
Отслеживание резистентности на мобильной ДНК
Ещё одно преимущество длинноридного секвенирования — способность собирать целые бактериальные хромосомы вместе с круглыми молекулами ДНК, называемыми плазмидами, которые могут перескакивать между бактериями и распространять гены резистентности. В исследовании учёные каталогизировали десятки типов плазмид. Некоторые были тесно связаны с конкретными видами, в то время как другие встречались у нескольких родов бактерий, что намекает на продолжающийся обмен генами в условиях больницы. Многие несли известные двигатели неэффективности лечения, такие как расширенные бета-лактамазы и карбапенемазы — ферменты, ослабляющие действие одних из важнейших антибиотиков. Картирование этих мобильных элементов помогает службам контроля инфекций понять, как опасные свойства распространяются по больнице с течением времени.
Ускорение ответов для врачей и больниц
По части времени новый подход демонстрирует самое очевидное преимущество. Стандартные рабочие схемы часто занимают от пяти до семи дней с момента положительного результата посева крови до получения полной идентификации и данных по чувствительности к антибиотикам. В отличие от этого, нанопоровая установка в этом пилотном исследовании предоставляла ранние идентификации видов в течение двух-четырёх часов после начала прогона и отмечала ключевые гены резистентности в пределах шести-восьми часов. Хотя более длительные прогоны секвенирования улучшали полноту геномов, они не меняли основных клинических выводов. Хотя это было небольшое исследование ранней стадии, которое ещё не связывало результаты с исходами пациентов и не оценивало затраты, оно указывает на то, что интеграция длинноридного метагеномного секвенирования в больничные лаборатории может предоставить более быструю и богатую информацией основу для выбора терапии, поддержки рационального применения антибиотиков и укрепления регионального мониторинга лекарственно-устойчивых инфекций.
Что это значит для ухода за пациентами
Для непрофессионала суть такова: врачи вскоре могут получить генетическую «мгновенную фотографию» инфекции крови в тот же день, когда посев становится положительным, вместо того чтобы ждать почти неделю. Эта «снимок» не только называет возбудителя, но и выделяет многие его уязвимые места и его потенциал передавать устойчивость другим. Хотя нужны дополнительные исследования с большими группами пациентов, более строгим контролем загрязнений и анализом затрат, это тайское пилотное исследование показывает, что карманные секвенсоры ДНК могут приблизить нас к быстрой, основанной на геномах помощи при жизнеугрожающих бактериальных инфекциях крови.
Цитирование: Yaikhan, T., Wongsurawat, T., Jenjaroenpan, P. et al. Evaluating long-read metagenomics for bloodstream infection diagnostics: a pilot study from a Thai Tertiary Hospital. Sci Rep 16, 9330 (2026). https://doi.org/10.1038/s41598-026-41247-2
Ключевые слова: инфекция крови, антимикробная резистентность, метагеномное секвенирование, нанопоровая технология, клиническая микробиология