Clear Sky Science · ru
Нормализация окрашивания в гистопатологии: бенчмаркинг методов на многoцентровом наборе данных
Более чёткие изображения тканей для врачей и компьютеров
Когда патологи рассматривают образцы тканей под микроскопом, они опираются на тонкие оттенки розового и фиолетового, чтобы определить, здоровы ли клетки или злокачественны. Сегодня эти цвета сильно различаются между лабораториями, что затрудняет человеческую диагностику и сбивает с толку инструменты искусственного интеллекта, обученные на подобных изображениях. В этом исследовании поставлена задача измерить масштаб цветовой проблемы и протестировать, какие компьютерные методы лучше всего делают изображения слайдов более однородными без потери важной информации.
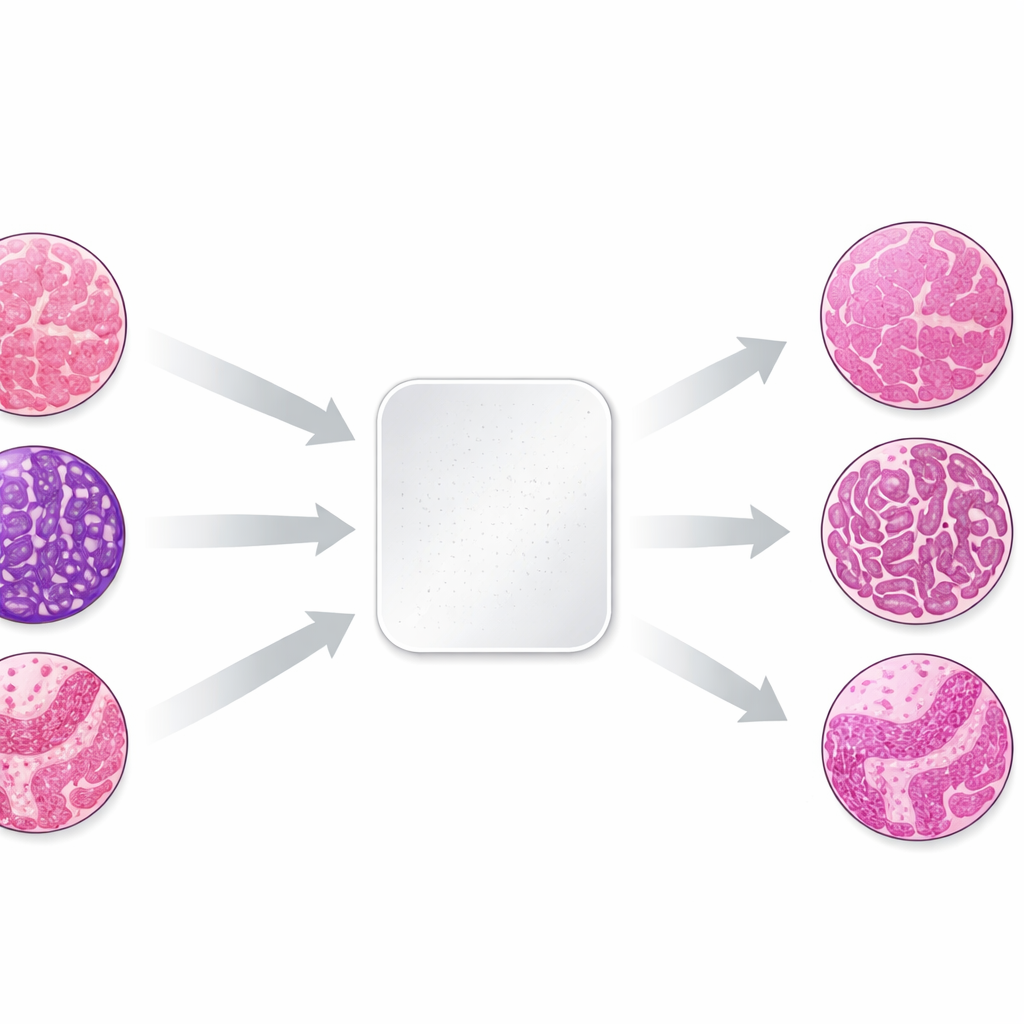
Почему цвет отличается от лаборатории к лаборатории
Работа сосредоточена на самой распространённой паре красителей в патологии — гематоксилине и эозине, где ядра клеток окрашиваются в синевато-фиолетовый, а окружающие ткани — в розовый. Небольшие различия в методах фиксации, обработке и окрашивания тканей, а также в способах сканирования изображений могут существенно смещать эти цвета. Чтобы изучить эффект в контролируемых условиях, авторы взяли три небольших образца ткани — кожа, почка и толстая кишка — из одних и тех же донорских блоков и отправили идентичные неокрашенные срезы в 66 лабораторий в 11 странах. Каждая лаборатория использовала свою рутинную процедуру окрашивания, а затем готовые слайды были оцифрованы. Поскольку биологический материал был почти одинаковым, любые различия во внешнем виде в основном отражали то, как каждая лаборатория окрашивала и изображала ткани.
Создание уникальной платформы для коррекции цвета
Полученная коллекция изображений продемонстрировала поразительную вариативность: слайды из одного и того же блокa могли варьироваться от бледных до почти чёрных или смещаться от холодных к очень тёплым тонам. Команда сначала количественно оценила эти различия, измерив средние уровни красного и синего в каждом слайде. Затем они выбрали по одному хорошо сбалансированному слайду для каждого типа ткани в качестве эталона и применили восемь различных методов нормализации окрашивания ко всем остальным. Четыре метода были традиционными математическими подходами, которые корректируют глобальную цветовую статистику или разделяют и перерасширяют компоненты окрашивания. Четыре других базировались на современных «генеративных» методах ИИ, которые учатся преобразовывать изображения из одного цветового стиля в другой с помощью нейронных сетей.
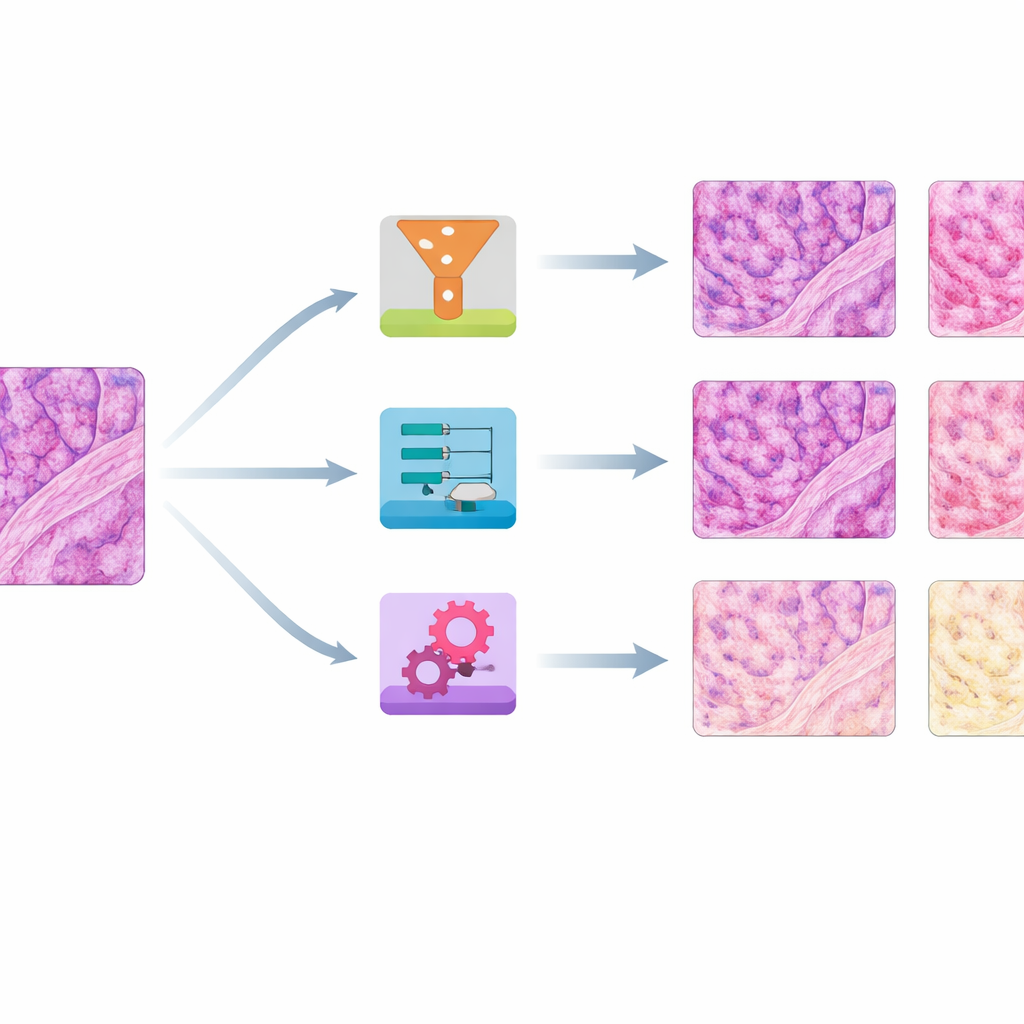
Какие методы лучше работали по цвету и по сохранению структуры
Для оценки эффективности авторы задали два основных вопроса: насколько исправленные изображения соответствуют цветам эталона и насколько хорошо они сохраняют мелкую структуру ткани? Они использовали несколько числовых метрик для сравнения распределений цветов, высокоуровневую меру сходства изображений из компьютерного зрения и структурный индекс, чувствительный к размытию или искажениям. По трем типам ткани — кожа, почка и кишка — простой метод, называемый согласованием гистограмм (histogram matching), то есть приведение распределения цветов каждого слайда к распределению эталона, стабильно давал наиболее близкое цветовое соответствие при сохранении структур в основном неповреждёнными. Другой традиционный подход, нормализация Райнхарда (Reinhard), часто работал почти так же хорошо. Третий метод, Vahadane, превосходил в сохранении структуры, но имел склонность сдвигать все изображения в розоватую тональность и ослаблять синий окрас ядер.
Как изображения выглядели для экспертов и инструментов ИИ
Опытные патологи просмотрели нормализованные слайды кишки, чтобы оценить, как методы влияют на интерпретируемость в реальной практике. Они проверяли, остались ли важные слои и типы клеток легко различимы, улучшились ли чрезмерно или недостаточно окрашенные образцы и появились ли какие-либо странные цифровые артефакты. Ни один метод не устранил все проблемы, но согласование гистограмм в целом давало ровные, похожие на эталон цвета без очевидных артефактов, особенно в сильно переокрашенных образцах. Некоторые методы на основе ИИ, в частности определённые версии CycleGAN и Pix2pix, создавали реалистично выглядящие результаты, но иногда вводили тонкие поддельные структуры или цветовые сбои в кровяных клетках и фоновых областях. Команда также показала, что нормализация изменила подсчёт ядер современным алгоритмом обнаружения клеток и то, как крупная «фондовая» модель представила слайды, подчёркивая, что коррекция цвета может существенно влиять на последующее поведение ИИ.
Что это значит для будущей цифровой диагностики
В целом исследование показывает, что цветовые различия между лабораториями достаточно велики, чтобы иметь значение как для человеческих экспертов, так и для автоматических систем, и что приведение изображений к единому виду — важный шаг на пути к надёжной и совместно используемой цифровой патологии. Удивительно, но в этом тщательно контролируемом наборе данных с очень похожим содержимым тканей простые глобальные методы, такие как согласование гистограмм, часто превосходили более сложные методы глубокого обучения, которым требуется гораздо больше тренировочных данных, чем по одному слайду на лабораторию. Авторы открыто публикуют свой 66-центровый набор данных, чтобы другие могли сравнивать новые методы и лучше проектировать тренировочные выборки, отражающие реальную вариативность. Для пациентов прогресс в этой области может означать создание ИИ-систем, которые «переносятся» из одной больницы в другую и обеспечивают более последовательные диагнозы независимо от того, где обработали биопсию.
Цитирование: Khan, U., Härkönen, J., Friman, M. et al. Staining normalization in histopathology: Method benchmarking using multicenter dataset. Sci Rep 16, 11097 (2026). https://doi.org/10.1038/s41598-026-40943-3
Ключевые слова: цифровая патология, нормализация окрашивания, гистологическая визуализация, медицинский ИИ, цветовые вариации