Clear Sky Science · ru
Пан-раковая классификация замороженных срезов с использованием визуального трансформера с мягкой смесью экспертов при слабом контроле
Почему это важно в операционной
Когда хирурги удаляют подозрительную опухоль, у них часто есть всего несколько минут, чтобы определить, удалён ли весь рак. Патологи спешат исследовать быстро замороженный срез ткани и дать ответ, пока пациент ещё на столе. Этот процесс при высоком давлении может осложняться размытыми препаратами, тонкими очагами опухоли и банальными временными ограничениями. Описанное здесь исследование изучает, как система искусственного интеллекта (ИИ) может помочь патологам быстро и надёжно отличать безвредную ткань от опасной в разных органах, используя оборудование, реалистичное для обычных больниц.
Быстрый тест со встроенными трудностями
Анализ замороженных срезов — стандарт современной хирургии: тонкий кусочек ткани замораживают, режут, окрашивают и рассматривают под микроскопом, чтобы установить, доброкачественный он или злокачественный и очищен ли операционный край. В отличие от постоянных лабораторных препаратов, замороженные срезы часто страдают от трещин, складок и неравномерного окрашивания. Разные патологи могут расходиться во мнениях по пограничным случаям, и время всегда поджимает. Эти проблемы особенно серьёзны в небольших или загруженных больницах, где несколько специалистов вынуждены охватывать многие виды рака. Авторы утверждают, что надёжный компьютерный помощник может сделать решения по замороженным срезам более последовательными, быстрыми и доступными.
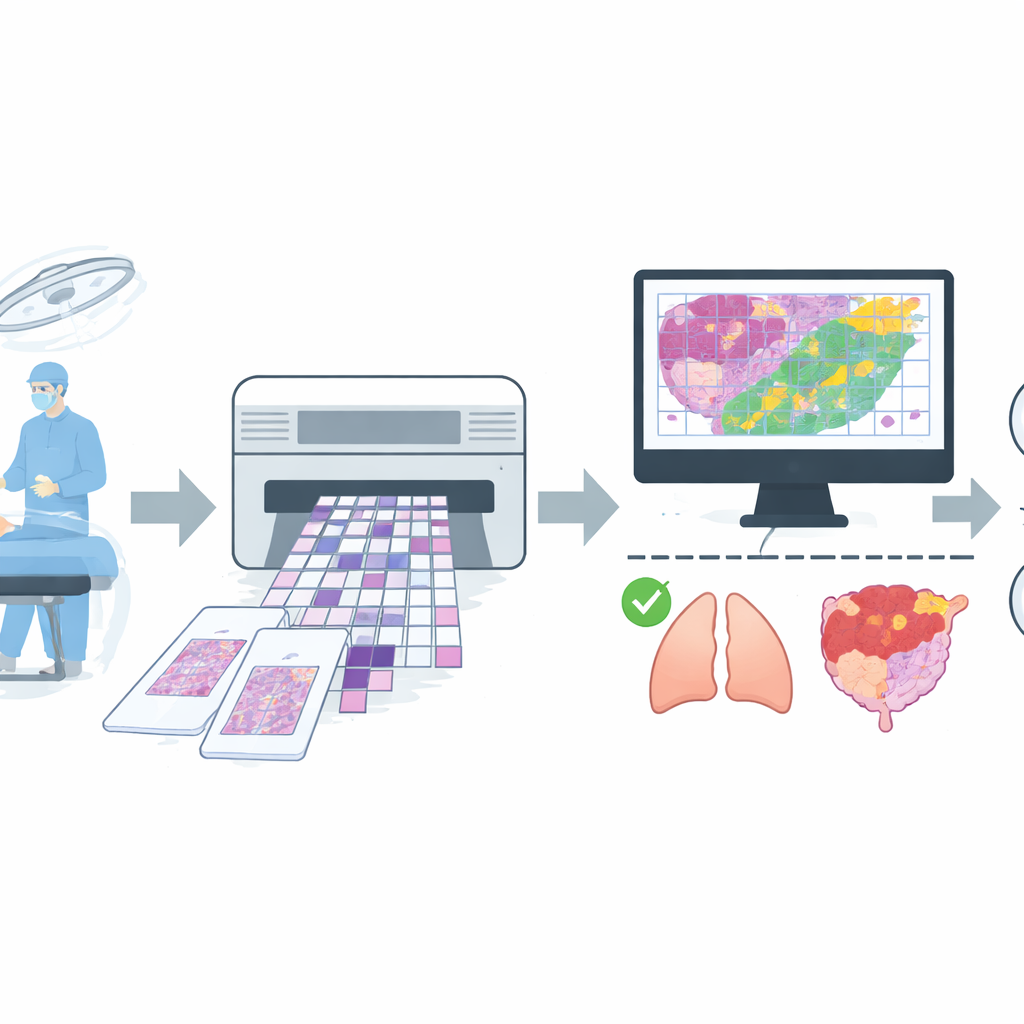
Создание широкого набора реальных изображений
Чтобы обучить такого помощника, команда собрала большую коллекцию цифровых изображений из рутинных операций в крупной больнице. Они накопили 4 754 целых слайда замороженной ткани более чем от 2 600 пациентов, затем применили строгие правила качества, чтобы удалить препараты с выраженными артефактами или неуверенными диагнозами. Итоговый набор содержал 4 667 слайдов, каждый из которых был помечен просто как доброкачественный или злокачественный на основе согласия между быстрым чтением замороженного среза и последующим, более тщательным отчётом по постоянному срезу. Слайды охватывали распространённые локализации, такие как лёгкие, молочная железа, щитовидная железа, лимфатические узлы и органы женской репродуктивной системы, а также смешанную группу менее частых мест, таких как желудок, печень и кожа. Данные были разделены на отдельные группы для обучения, тонкой настройки и финального тестирования с заботой о том, чтобы изображения одного и того же пациента не попадали в разные группы.
Как ИИ учится по слабым подсказкам
Исследователи построили свою модель на классе нейросетей, называемых Vision Transformer, которые превосходно находят закономерности в больших изображениях. Каждое большое изображение ткани автоматически разрезали на множество мелких тайлов и патчей, чтобы обработать их на стандартном графическом оборудовании. Ключевым нововведением стало замещение части сети «мягкой смесью экспертов» — набором многих небольших специализированных ветвей, каждая из которых фокусируется на разных визуальных паттернах. Вместо жёсткого переключения экспертов система плавно смешивает их вклады, что стабилизирует обучение и лучше использует ограниченные данные. Поскольку патологи не вычерчивали контуры опухолей, модель должна была учиться при слабой разметке: ей было известно только, является ли весь слайд доброкачественным или злокачественным. Стратегия множественного экземпляра (multiple-instance learning) выводила наиболее подозрительные патчи на злокачественном слайде как положительные примеры, что позволяло сети постепенно сосредоточиться на самых информативных областях.
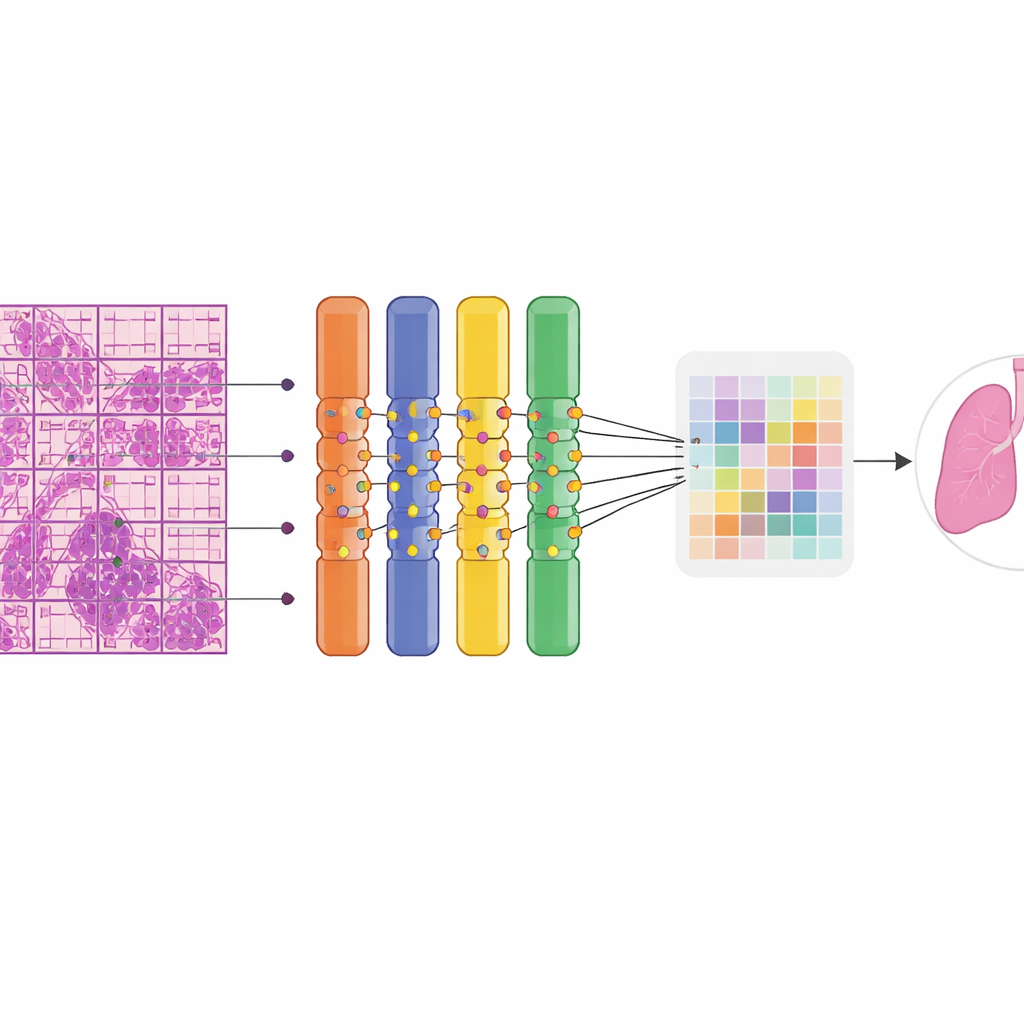
Как система работает на практике
При тестировании на 669 ранее невидимых слайдах ИИ с высокой точностью отделял доброкачественную ткань от злокачественной. В целом он правильно классифицировал около 90% случаев и показал отличную способность разделять две группы по порогам вероятности. Чувствительность, вероятность отмечать действительно злокачественный слайд, составляла примерно четыре из пяти, в то время как специфичность, вероятность правильно назвать доброкачественный слайд доброкачественным, была ещё выше. Что важно, качество работы оставалось высоким по разным органам: в тестовой выборке система идеально обнаружила все злокачественные случаи лёгких и молочной железы и хорошо показала себя на реже встречающихся группах, таких как опухоли придатков у женщин и смешанные «прочие» органы. Наложенные цветовые тепловые карты показали, что внимание модели концентрировалось на областях, которые эксперты-патологи признавали опухолью, включая метастатические очаги в лимфоузлах, в то время как нормальные структуры в основном игнорировались. Система работала эффективно, требуя менее 5 ГБ оперативной памяти, что делает её пригодной для использования на широко доступных графических картах, а не на дорогих кластерах.
Ограничения, ошибки и пути улучшения
Авторы также исследовали, где ИИ давал сбои. Ложные отрицательные результаты часто были связаны с крайне редкими раковыми клетками, размытыми участками сканирования или сильным воспалением, маскирующим злокачественные гнёзда. Ложные положительные срабатывания возникали при доброкачественных состояниях, имитирующих рак в микроскопе, таких как реактивная гиперплазия или искажённые замороженные ткани. Поскольку рутинные хирургические рабочие процессы не включают детальные контуры опухолевых областей, команда не могла количественно оценить, насколько тепловые карты соответствуют пометкам экспертов, полагаясь вместо этого на качественный обзор. Некоторые типы органов, например язык или определённые опухоли мягких тканей, оставались недостаточно представлены, что указывает на необходимость больших, многоцентровых коллекций для расширения возможностей системы.
Что это может значить для пациентов и больниц
В целом исследование демонстрирует, что тщательно спроектированная система ИИ может точно и интерпретируемо помогать в ключевой задаче хирургической патологии: принимать в реальном времени решение о том, доброкачественная ли ткань или злокачественная в разных типах органов. Работая только с пометками на уровне слайда, исполняясь на широко доступном оборудовании и выделяя подозрительные области для проверки человеком, модель предлагает практический путь к более последовательным решениям по замороженным срезам. Для пациентов это может означать лучше информированные операции в рамках одной процедуры; для больниц, особенно с ограниченным числом специалистов, — перспективу, где современные цифровые инструменты помогают обеспечивать высококачественную онкологическую помощь более равномерно.
Цитирование: Wu, J., Yang, M., Li, J. et al. Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision. Sci Rep 16, 10297 (2026). https://doi.org/10.1038/s41598-026-40924-6
Ключевые слова: замороженный срез, цифровая патология, диагностика рака, визуальный трансформер, обучение со слабой разметкой