Clear Sky Science · ru
Эффективное разделение в вихрях Дина при сниженных расходах для сортировки редких клеток
Почему важно сортировать редкие клетки
Клетки рака, попадающие в кровоток или другие биологические жидкости, действуют как сигналы раннего предупреждения о болезни. Они, однако, сильно уступают по численности обычным клеткам крови, поэтому их чрезвычайно трудно обнаружить и изучить. В этой работе описано новое микромасштабное устройство, которое использует бережные закрученные потоки внутри крошечного спирального канала, чтобы отводить более крупные, похожие на опухолевые, клетки от меньших лейкоцитов при намного более низкой скорости потока, чем обычно. Этот низконапрягающий, легко интегрируемый подход может помочь лабораториям обогащать редкие клетки для диагностики и мониторинга лечения без их повреждения.
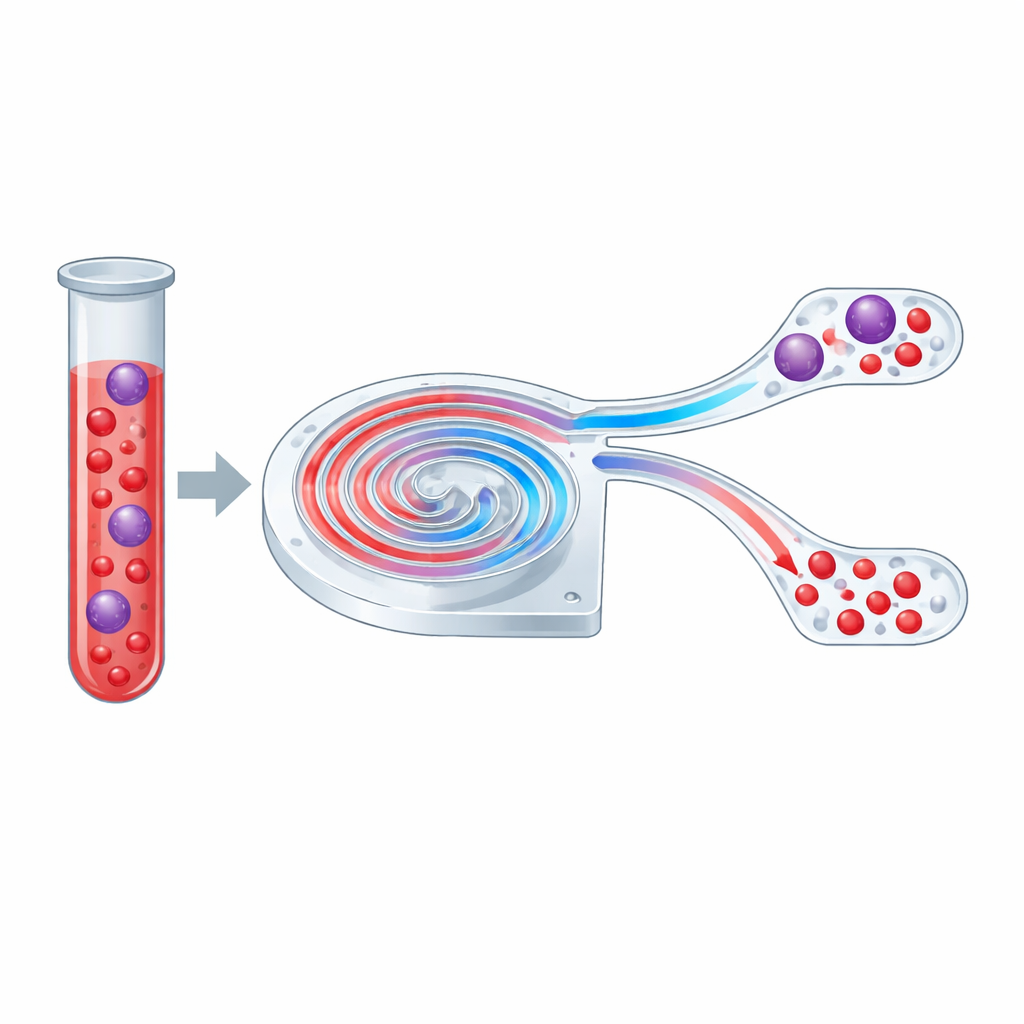
Крошечная спиральная дорога для клеток
В основе исследования — прозрачный микрочип с каналом в форме спирали, тоньше человеческого волоса. В прямом канале клетки в основном испытывают толчок вдоль направления потока и небольшое боковое смещение, зависящее от их размера. На изогнутом, спиральном пути появляется второй эффект: жидкость закручивается в парные водовороты поперек сечения канала, известные как вихри Дина. Эти водовороты уносят более мелкие объекты поперек струи, тогда как более крупные удерживаются ближе к одной стороне. Путем точной настройки этого баланса авторы спроектировали спираль, которая может разделять смесь частиц или клеток на два потока преимущественно по размеру.
Как заставить спирали работать на бережных скоростях
Большинство существующих спиральных устройств эффективно сортируют лишь при интенсивной подаче, на расходах в сотни или тысячи миллилитров в час. Такие условия сокращают время обработки, но увеличивают сдвиговое напряжение на клетки и затрудняют сопряжение спирали с другими микрофлюидными этапами, которые предпочитают более медленные, контролируемые потоки. Команда поставила иную цель: сохранить сильную сортировку по размеру при примерно 50 миллилитрах в час, то есть на порядок мягче. Для этого они систематически варьировали геометрию девяти спиральных конструкций — изменяя ширину и высоту канала, а также уклон внешней стенки — и сочетали эксперименты со численным моделированием циркулирующего потока.
Проследить частицы через водовороты
Чтобы сначала понять физику, исследователи прогоняли через каждую спираль флуоресцентные пластиковые шарики двух размеров — 10 и 15 микрометров. При низких скоростях оба типа шариков собирались у внутренней стенки. По мере увеличения потока фокусированный поток мигрировал поперек канала к внешней стенке, но при разных пороговых скоростях для каждого размера. Для одного характерного дизайна мелкие шарики смещались наружу примерно при 30 миллилитрах в час, тогда как большие — около 60 миллилитров в час. Это создавало промежуточный диапазон, в котором крупные и мелкие шарики выходили по разным сторонам. Моделирование движения жидкости показало, что при более высоких скоростях шарики стабилизируются очень близко к центрам вихрей Дина, что подтверждает давно выдвинутое, но ранее непроверенное представление о работе таких устройств.
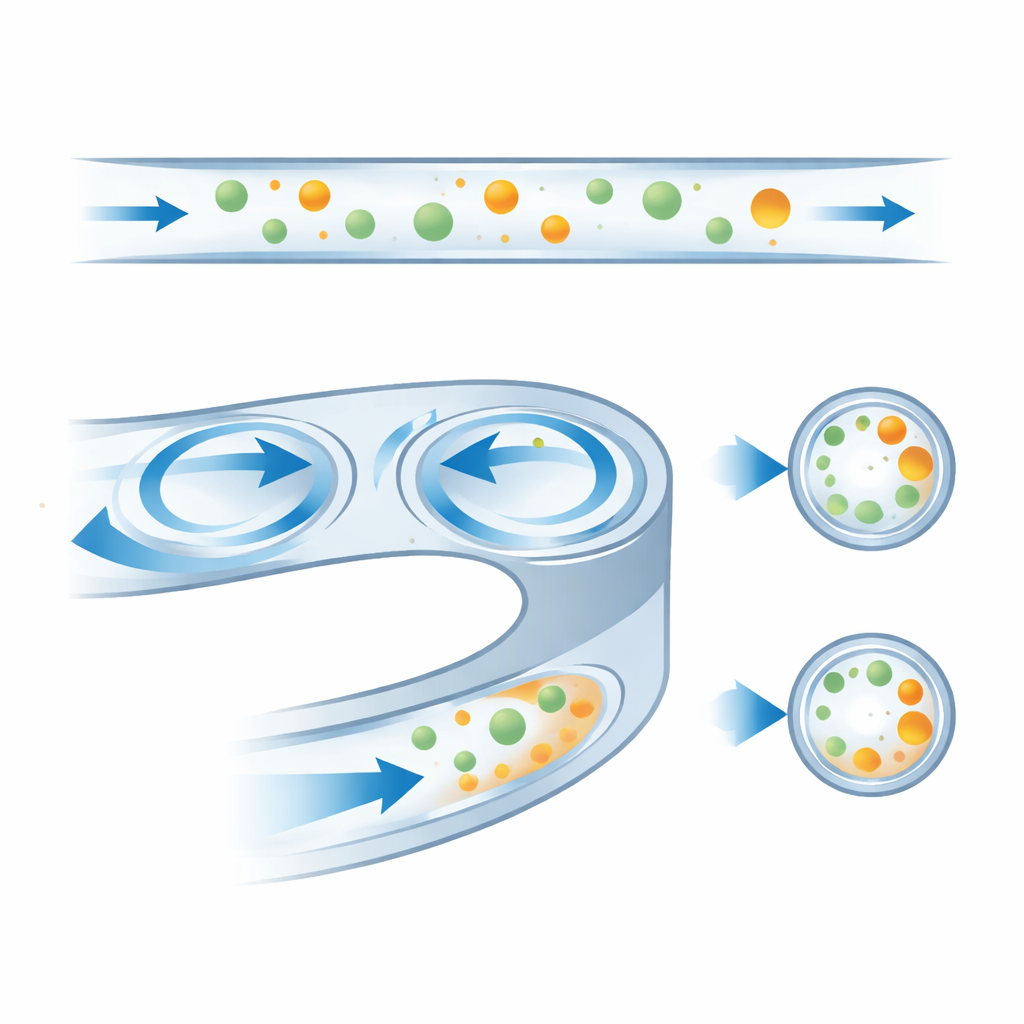
Форма канала для лучшего разделения
Сравнив множество вариантов, авторы выяснили, как простые геометрические решения управляют эффективностью. Более крутой уклон внешней стенки отодвигает внутренние водовороты дальше наружу, смещая устойчивые положения шариков и меняя расход, при котором они меняют стороны. Узкие каналы подводят вихри слишком близко к внутренней стенке, из‑за чего частицы втягиваются в них слишком рано, тогда как очень плоские каналы требуют больших скоростей, прежде чем произойдет сдвиг. Лучший компромисс — канал шириной 250 микрометров с умеренным уклоном стенки и соотношением сторон, который обеспечивал четкую разницу между двумя размерами шариков при 40–60 миллилитрах в час и оставался устойчивым к небольшим колебаниям расхода.
От пластиковых шариков к живым раковым клеткам
С оптимизированной спиралью в руках команда перешла к биологическим образцам. Они протестировали несколько клеточных линий рака, имитирующих циркулирующие опухолевые клетки, и сравнили их поведение с лейкоцитами из подготовленной крови. Несмотря на то, что клетки более мягкие и более вариабельные по размеру, чем шарики, все типы фокусировались в узкие потоки и сдвигались с внутренней на внешнюю сторону по мере увеличения потока в выраженно зависимой от размера манере. При работе на 50 миллилитрах в час устройство направляло около 89% лейкоцитов в «отходный» поток, одновременно удерживая 75–86% более крупных клеток, похожих на опухолевые, в «обогащенном» потоке. Что важно, выживаемость клеток оставалась около 98% даже после прохождения через спираль при разных расходах.
Что это значит для будущих онкотестов
Проще говоря, авторы создали и расшифровали крошечный спиральный фильтр, который может деликатно снимать большую часть фона из клеток крови, одновременно удерживая более редкие, крупные клетки, похожие на опухолевые, и всё это при относительно медленных, благоприятных для клеток расходах. Прояснив, как формируются внутренний и внешний потоки и как форма канала их контролирует, работа превращает технологию, во многом основанную на методе проб и ошибок, в более предсказуемый инструмент. Сама по себе эта камера не захватит каждую отдельную опухолевую клетку, но она предоставляет мощный шаг предварительного обогащения, который можно напрямую связать с более селективными биологическими методами. Такое сочетание в конечном итоге может упростить обнаружение, анализ и мониторинг рака с использованием небольших образцов жидкости от пациентов.
Цитирование: Dupont, E., Artinyan, L., Brunin, C. et al. Effective dean vortex separation at reduced flow rates towards rare cell sorting. Sci Rep 16, 10422 (2026). https://doi.org/10.1038/s41598-026-40845-4
Ключевые слова: микрофлюидная сортировка клеток, спиральный микроканал, циркулирующие опухолевые клетки, вихри Дина, жидкостная биопсия