Clear Sky Science · ru
МикроРНК, образующаяся из сплайсинга экзона 4 амелогенина, регулирует формирование эмали через контроль сплайсинга экзона 4 и экспрессии амелогенина
Почему небольшая РНК важна для прочных зубов
Зубная эмаль — самая твердая субстанция в человеческом организме, но при нарушении процесса её формирования она может оказаться относительно хрупкой. В этом исследовании показано, как очень маленький фрагмент генетического материала, микроРНК под названием miR‑exon4, помогает клеткам, формирующим зубы, строить правильно минерализованную эмаль. Показав, что эта микроРНК тонко регулирует как главный белок эмали, так и сроки отложения минерала, работа связывает точечную обработку РНК внутри клеток с видимыми дефектами эмали, похожими на те, что наблюдаются при наследственном заболевании amelogenesis imperfecta.
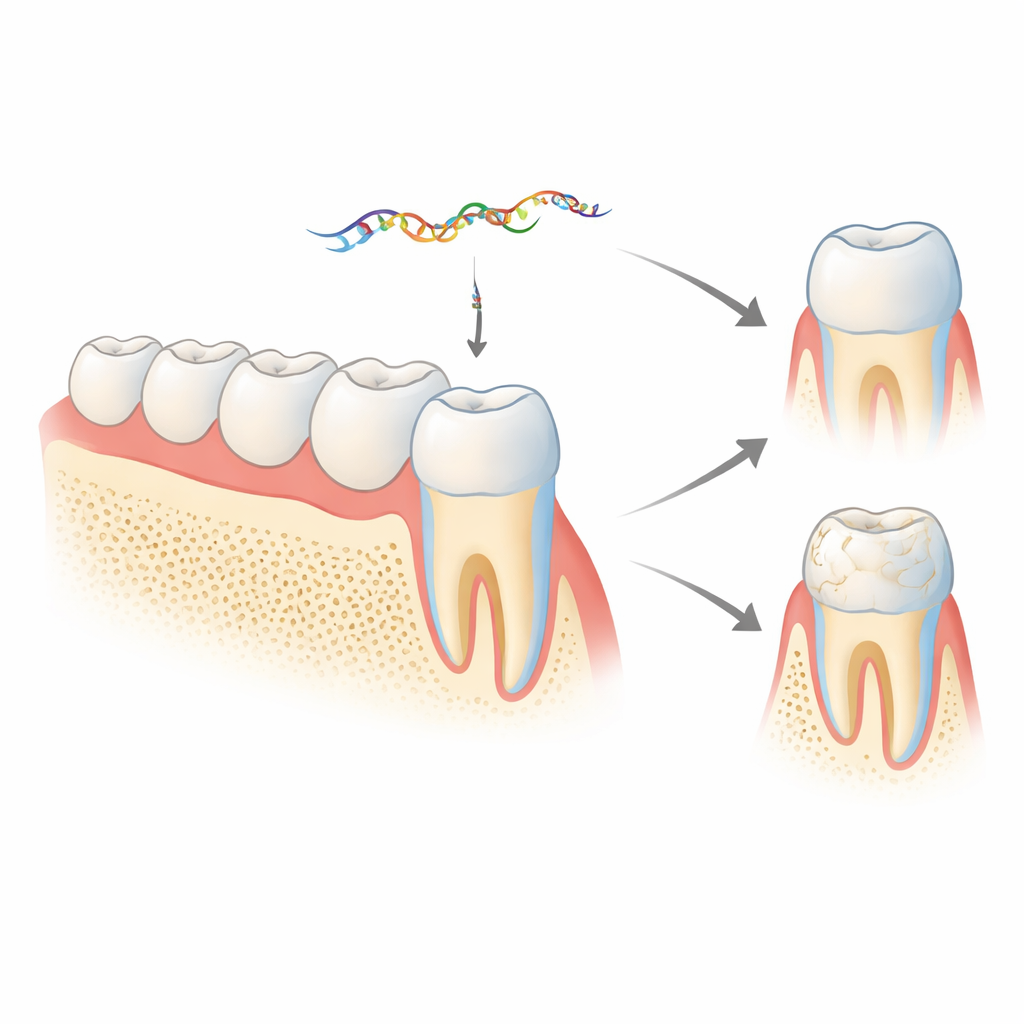
Скрытое послание внутри гена эмали
Эмаль в основном формируется из белка амелогенина, который продуцируют клетки, называемые амелобластами. Ген амелогенина (Amelx у мышей) может подвергаться альтернативному сплайсингу, образуя несколько версий белка, необходимых на разных этапах развития зуба. Один короткий участок, называемый экзоном 4, обычно удаляется из окончательной кодирующей РНК. Ранее эта группа показала, что отбрасываемый экзон 4 — не мусор: он обрабатывается в микроРНК miR‑exon4, которая может регулировать другие гены, важные для костей и эмали. Новое исследование задаётся вопросом, что происходит в живых организмах, когда эта микроРНК уменьшена или блокирована, и возвращается ли она к контролю за тем, как сам амелогенин собирается.
Регуляторная цепочка внутри формирующих зуб клеток
Исследователи сначала подтвердили на зубах мышей, что miR‑exon4 участвует в регуляторной цепочке, которую они ранее картировали в культуре клеток. В нормальных эмалевых органах miR‑exon4 сдерживает активность двух вышестоящих генов, Nfia и Prkch. Когда их уровни низки, возрастает концентрация ключевого транскрипционного фактора RUNX2. На мышах, у которых либо отсутствовал ген амелогенина, либо вводили дополнительную miR‑exon4, либо применяли блокатор miR‑exon4, команда показала: снижение miR‑exon4 повышает Nfia и Prkch и снижает RUNX2, а добавление miR‑exon4 даёт обратный эффект. Это подтвердило, что путь miR‑exon4–Nfia/Prkch–RUNX2 действует in vivo в развивающихся зубах.
От нарушенных сигналов к ослабленной эмали
Чтобы выяснить, как эти молекулярные сдвиги влияют на саму эмаль, учёные ингибировали miR‑exon4 у новорождённых мышат в течение недели в период активного формирования зубов. Трёхмерная рентгенография показала явное уменьшение сильно минерализованной эмали у обработанных животных как в резцах, так и в молярах. Тепловые карты и окрашенные срезы продемонстрировали, что начало накопления минерала вдоль слоя эмали задерживалось, а ранняя фаза минерализации укорачивалась, что приводило к более грубой поверхности и нечетким границам между эмалью и подлежащими тканями. Одновременно уровни белка RUNX2 в амелобластах снижались, тогда как белок амелогенина — включая варианты, содержащие экзон 4 — увеличивался. Эта картина схожа с предыдущими моделями, в которых чрезмерное образование длинной формы амелогенина с экзоном 4 приводит к дефектам эмали, что наводит на мысль, что избыточность этого изоформа, вызванная потерей miR‑exon4, может напрямую нарушать нормальную минерализацию.
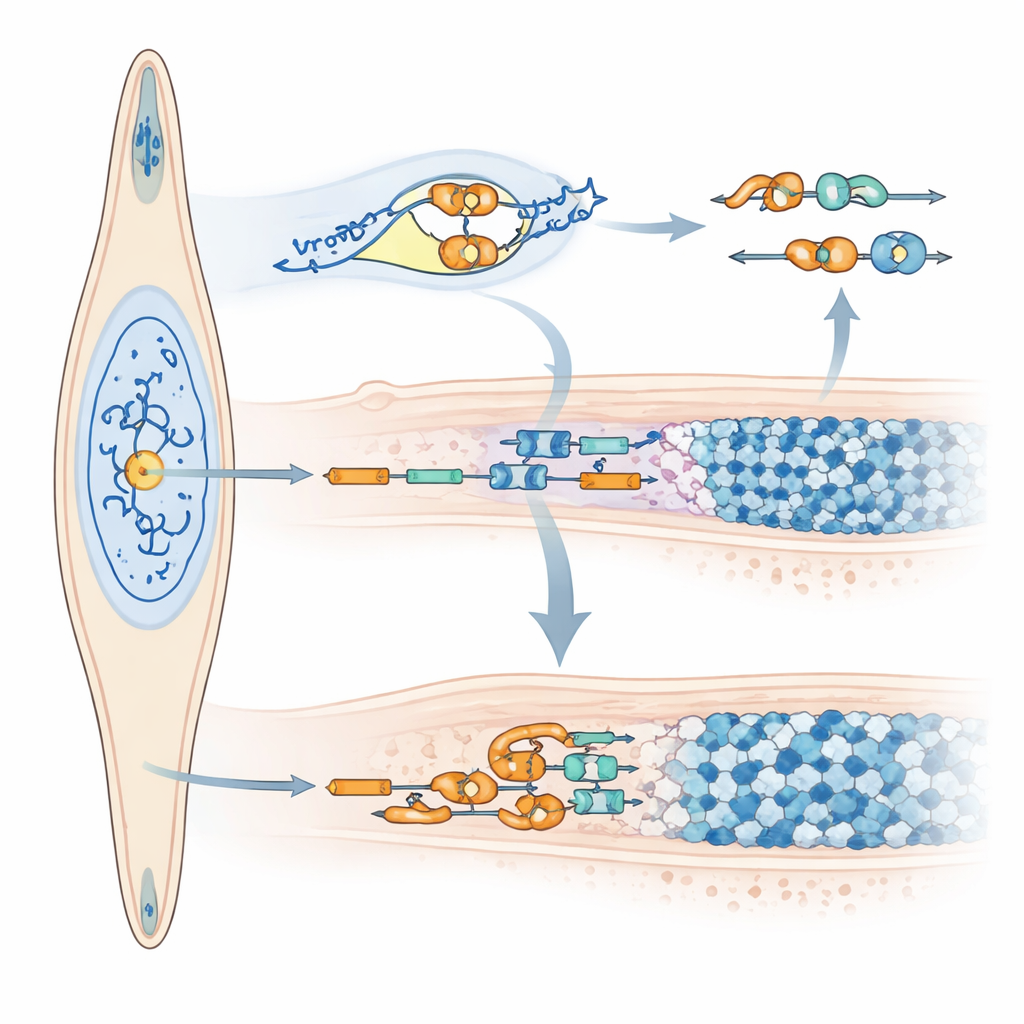
Как микроРНК меняет «послание» амелогенина
Помимо изменения количества синтезируемого амелогенина, miR‑exon4 также влияет на то, как РНК амелогенина рассекается и сплайсируется. Кратковременная блокировка miR‑exon4 снизила долю РНК-молекул, всё ещё содержащих экзон 4, без изменения общего уровня амелогенина, что указывает на более частое исключение экзона 4. Команда связала этот сдвиг с изменениями ряда генов‑регуляторов сплайсинга (SRSF), некоторые из которых увеличивались, а другие уменьшались при снижении miR‑exon4. В клеточных моделях с специально модифицированным вариантом гена амелогенина, который производит меньше miR‑exon4, пропускание экзона 4 также происходило чаще. Важный момент: сама микроРНК была обнаружена в ядре клетки, где происходит сплайсинг, и биохимические тесты показали, что она ассоциируетcя с прекурсорной РНК амелогенина в конкретной контрольной точке соседнего интрона. Эти данные поддерживают двоякую роль miR‑exon4: косвенно формировать выбор экзонов через регулирование факторов сплайсинга и непосредственно связываться рядом с экзоном 4, влияя на то, будет ли он сохранён или удалён.
Что это значит для здоровья эмали
В совокупности исследование показывает miR‑exon4 как небольшого, но центрального координатора формирования эмали. Когда она присутствует в нужном количестве, она поддерживает адекватную активность RUNX2, удерживает производство амелогенина в равновесии и помогает обеспечивать включение или исключение экзона 4 на соответствующих стадиях. При отсутствии или снижении miR‑exon4 этот баланс нарушается: сигнальные пути сбиваются, экзон 4 обрабатывается неправильно, состав изоформ амелогенина смещается, и ранняя минерализация эмали ослабляется. Эти данные помогают объяснить, как некоторые мутации в гене амелогенина могут вызывать наследственные расстройства эмали, и подчёркивают важную роль ядерных микроРНК в формировании самой твердой ткани организма.
Цитирование: Shemirani, R., Duong, T., Kim, R. et al. A splicing-derived microRNA from amelogenin exon4 regulates enamel formation via control of exon4 splicing and amelogenin expression. Sci Rep 16, 11044 (2026). https://doi.org/10.1038/s41598-026-40706-0
Ключевые слова: зубная эмаль, амелогенин, микроРНК, сплайсинг РНК, врожденная гипоплазия эмали (amelogenesis imperfecta)