Clear Sky Science · ru
ABE9, соединённый с SpRY Cas9 никказойзой, позволяет точно создавать мышиные модели без побочных изменений
Более точные инструменты для создания лучших моделей болезней
Многие тяжёлые заболевания вызваны «опечатками» в нашей ДНК — одиночными заменами букв. Чтобы понять эти состояния и в перспективе лечить их, учёные нередко создают мышей с теми же мутациями, что и у пациентов. Но переписывать ДНК настолько точно сложнее, чем кажется: старые методы могут оставлять шрамы в геноме, вносить дополнительные изменения и искажать результаты экспериментов. В этом исследовании описан усовершенствованный инструмент редактирования генов, названный ABE9-SpRY, предназначенный для замены одной конкретной буквы ДНК при минимальном воздействии на соседние нуклеотиды и остальной геном.
От грубых разрезов к аккуратным корректировкам ДНК
Традиционный CRISPR-Cas9 действует как молекулярные ножницы, разрезая обе цепи ДНК. Клетки восстанавливают эти разрывы несовершенно, часто оставляя небольшие вставки или делеции, которые непредсказуемо нарушают гены. Это годится для выключения генов, но не для точного воспроизведения отдельной вызывающей болезнь мутации. Базовые редакторы, напротив, не разрезают ДНК: они химически переводят одну букву в другую — здесь A в G — сохраняя при этом структуру двойной спирали. Такой подход заметно сокращает крупные делеции и перестройки, но ранние адениновые редакторы всё ещё страдали от трёх ключевых проблем: они иногда редактировали соседние «наблюдательные» нуклеотиды, могли работать только рядом со строгими короткими метками-последовательностями и иногда вносили изменения в нежелательных местах генома.
Проектирование более избирательного молекулярного карандаша
Исследователи поставили цель одновременно устранить все три ограничения. Они начали с ABE9 — новой версии базового редактора, которая фокусирует активность на очень узком участке ДНК, сужая «окно редактирования», так что гораздо меньше соседних букв меняются случайно. Затем они слили ABE9 с инженерной никказойзой Cas9, называемой SpRY. В отличие от стандартного Cas9, требующего строгой метки «NGG» рядом с целью, SpRY распознаёт гораздо более широкий набор последовательностей ДНК. Это делает доступными для редактирования участки, ранее недостижимые. Полученный фермент ABE9-SpRY призван быть одновременно высокоточен и значительно более гибок в выборе целей.
Испытание нового редактора в клетках и эмбрионах
Чтобы проверить, оправдывает ли ABE9-SpRY ожидания, команда сравнила его с широко используемым, более агрессивным редактором ABE8e-SpRY. Они нацелились на четыре клинически значимые позиции в генах ионных каналов (TPC1, TPC2 и TRPM4), которые играют важную роль в работе сердца и печени. В культивируемых мышиных нейронах ABE8e-SpRY эффективнее менял целевую букву, но также изменял и многие соседние основания. ABE9-SpRY, наоборот, давал меньше общих правок, но гораздо большую долю «чистых» результатов — прочтений, в которых изменена только намеренная буква без дополнительных мутаций в локальной области. Та же картина наблюдалась и в мышиных эмбрионах. При инъекции компонентов редактирования в оплодотворённые яйца ABE8e-SpRY часто конвертировал почти все копии целевого гена, но с множеством побочных изменений. ABE9-SpRY редактировал меньше копий в целом, однако там, где он вмешивался, последовательность ДНК, как правило, исправлялась точно по плану.
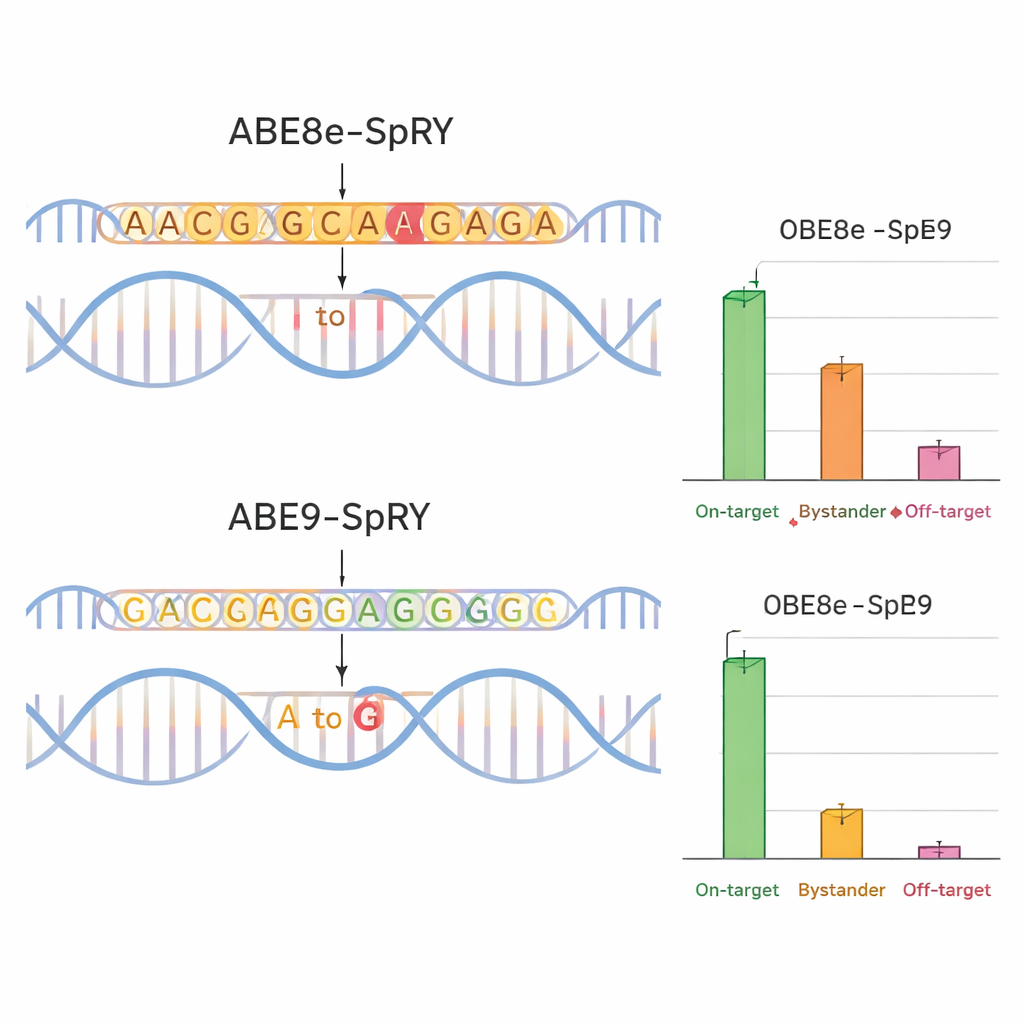
Чище правки, меньше побочных эффектов
Точность — это не только локальное окружение ДНК. Команда также проверяла, изменял ли редактор удалённые участки генома. С помощью вычислительных прогнозов и целевого секвенирования они измеряли внецелевые изменения в местах с похожими последовательностями в мышиных эмбрионах. ABE8e-SpRY часто вносил непреднамеренные замены A→G в этих локусах, иногда на удивительно высоком уровне. ABE9-SpRY показал значительно меньше таких событий, с редкими внецелевыми правками и отсутствием обнаруживаемой активности в специализированном тесте на Cas9-независимое повреждение ДНК. Важно, что при использовании ABE9-SpRY в одиночку — не в смешанных тестах — для внесения двух конкретных мутаций у мышей было получено много основателей, в которых желаемая правка присутствовала в высоком титре и надёжно передавалась потомству, опять же с минимальными побочными изменениями или небольшими вставками и делециями.
Распространение точного редактирования на человеческие стволовые клетки
Поскольку стволовые клетки, полученные от пациентов, всё шире используются для изучения болезней и тестирования лекарств, исследователи также пробовали ABE9-SpRY в человеческих индуцированных плюрипотентных стволовых клетках. Они нацелились на человеческую версию гена TPC1 в положении, эквивалентном одному из мышиных сайтов. С помощью флуоресцентного репортера для обогащения отредактированных клеток они обнаружили, что ABE8e-SpRY даёт более высокий «сырые» уровень редактирования, но снова модифицирует несколько соседних оснований. ABE9-SpRY правил меньше аллелей в целом, но доля идеально отредактированных последовательностей — одна намеренная замена и ничего лишнего — была заметно выше, с меньшим количеством разрушающих вставок или делеций. В работе со стволовыми клетками, где отдельные клоны расширяют для детальных исследований, такого рода «чистая» правка обычно ценится больше, чем грубая эффективность.
Почему это важно для будущих исследований заболеваний
Для учёных, пытающихся понять, как одна замена буквы ДНК приводит к болезни, дополнительные непредвиденные мутации могут существенно запутать результаты. Это исследование показывает, что ABE9-SpRY, хотя и уступает по скорости «сырых» правок, способен вносить одиночные замены в геномы мышей и человеческих стволовых клеток с впечатляющей точностью и широкой гибкостью в выборе целей. Это делает его многообещающим инструментом для создания достоверных животных и клеточных моделей генетических заболеваний человека, особенно в ситуациях, где даже одна случайная мутация может исказить биологию или сорвать потенциальную терапию.
Цитирование: Ong, J.K., Bhunia, S., Hilbert, B. et al. ABE9 fused to SpRY Cas9 nickase enables precise generation of bystander free mouse models. Sci Rep 16, 7463 (2026). https://doi.org/10.1038/s41598-026-40642-z
Ключевые слова: адениновая базовая редактура, модели заболеваний CRISPR, генетика мышей, внецелевые эффекты, редактирование генов hiPSC