Clear Sky Science · ru
Низкоаффинное связывание антитела против B7-H3 клона MJ18 с мышиным B7-H3 не вызывает регрессии опухоли
Почему это важно для исследований рака
Иммунотерапия рака во многом опирается на антитела — лабораторно созданные белки, которые связываются с опухолевыми клетками и помогают иммунной системе их уничтожать. Одной из перспективных мишеней является молекула B7-H3, часто обильно экспрессируемая в различных человеческих опухолях и редкая в здоровых тканях. В этой работе тщательно проверили широко используемое исследовательское антитело MJ18, которое предполагалось блокировать B7-H3 в мышиных моделях. Авторы обнаружили, что MJ18 слабо связывается со своей предполагаемой мишенью и не замедляет рост опухоли, что ставит под сомнение интерпретацию прежних доклинических экспериментов с использованием этого инструмента.
Перспектива «флага» опухоли
B7-H3 привлекает повышенное внимание, потому что действует как молекулярный щит: опухоли с высокой экспрессией этого белка обычно содержат меньше агрессивных иммунных клеток и связаны с худшими прогнозами пациентов. В нескольких мышиных моделях удаление гена B7-H3 в опухолевых клетках усиливало иммунную реакцию и могло приводить к уменьшению или исчезновению опухолей. Эти наблюдения стимулировали разработку препаратов, инженерных иммунных клеток и антитело‑лекарственных конъюгатов, нацеленных на B7-H3 в человеческих опухолях. Тем не менее точный механизм, с помощью которого B7-H3 подавляет иммунитет — и даже его рецептор на иммунных клетках — остаётся неясным, особенно учитывая структурные различия между мышиным и человеческим B7-H3.
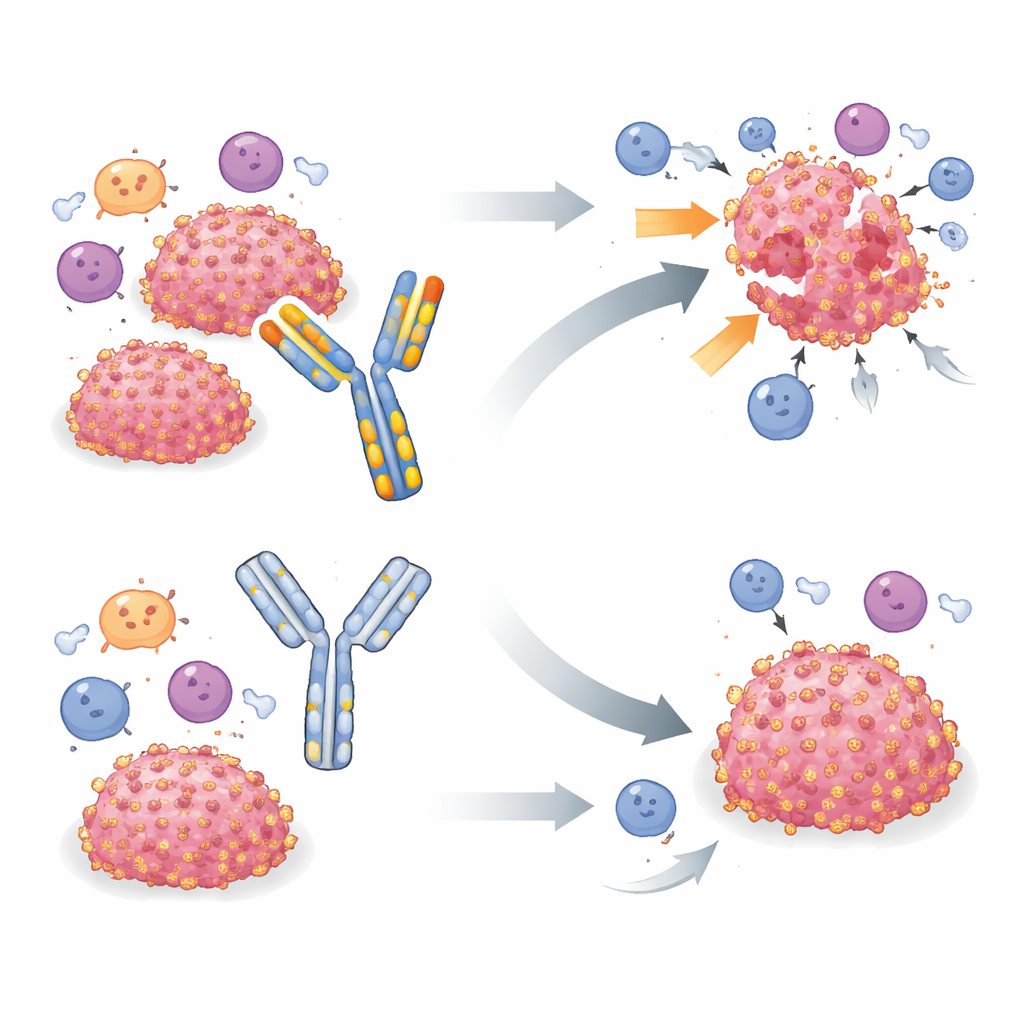
Внимание к распространённому инструменту
Для изучения B7-H3 in vivo многие группы опирались на одно родственное крысе антитело MJ18, которое, как сообщалось, распознаёт мышиный B7-H3 и блокирует его иммуносупрессивную активность. Предыдущие исследования с MJ18 в разных моделях заболеваний, включая рак, часто описывали замедление роста опухолей и улучшение выживаемости. Текущая команда сначала протестировала MJ18 в мышиной модели рабдомиосаркомы — детской опухоли мягких тканей, где B7-H3 уже был отмечен как важный механизм уклонения. Когда MJ18 не улучшило контроль над опухолью, исследователи расширили тесты на две другие B7-H3‑положительные опухоли — поджелудочную и молочную железу — которые явно чувствительны к удалению гена B7-H3. Во всех трёх моделях нокаут B7-H3 в опухолевых клетках надёжно задерживал или устранял опухоли, тогда как лечение мышей MJ18 в дозах и режимах, похожих на описанные в литературе, не оказало заметного влияния на рост опухоли или выживаемость.
Проверка: действительно ли MJ18 поражает цель
Авторы затем поставили базовый вопрос, который удивительно редко был строго проверен: действительно ли MJ18 связывается с мышиным B7-H3 и с какой силой? С помощью проточной цитометрии они сравнили MJ18 с другим антителом, EPNCIR122, известным распознавать B7-H3. На нескольких линиях мышиных опухолевых клеток EPNCIR122 давало чёткий сигнал, который исчезал при нокауте гена B7-H3, подтверждая его специфичность. MJ18, напротив, не показало убедительного связывания даже при высоких концентрациях. При исследовании иммунных клеток селезёнки MJ18 связывалось, но рисунок связывания не совпадал с экспрессией B7-H3, а EPNCIR122 совершенно не обнаруживало B7-H3 на этих клетках, что указывало на то, что MJ18 цепляется за что‑то иное.
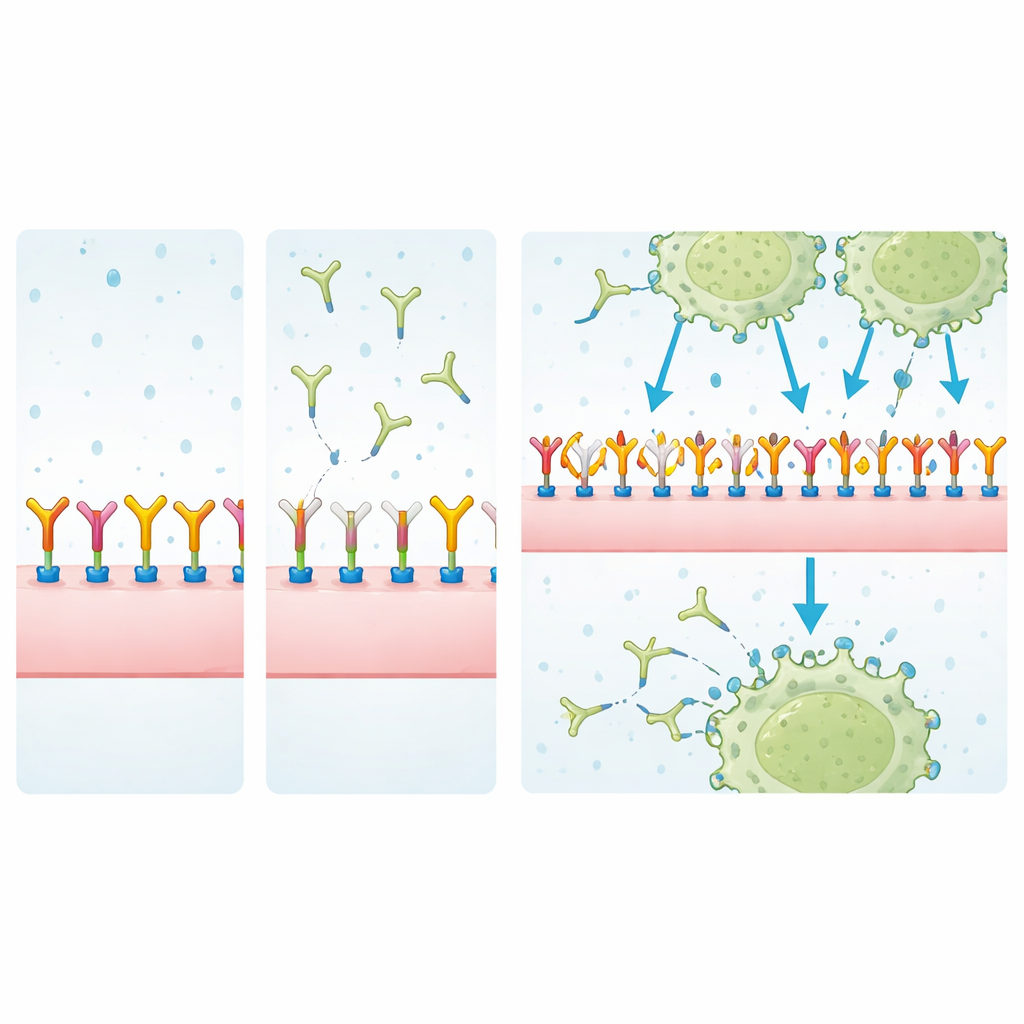
Поиски партнёров по связыванию
Чтобы выяснить, что же на самом деле распознаёт MJ18, исследователи выделяли поверхностные белки клеток с помощью MJ18 или EPNCIR122 и анализировали их методом масс‑спектрометрии, отфильтровывая распространённые фоновые контаминанты. В опухолевых клетках EPNCIR122 сильно обогащало B7-H3 по сравнению с другими белками, подтверждая, что это высокоспецифичный реагент. MJ18, однако, вытягивало смесь белков, в которой B7-H3 присутствовал только слабо и на уровне, сопоставимом с неспецифическими связывателями. Измерения поверхностного плазмонного резонанса, чувствительной техники для количественной оценки молекулярных взаимодействий, подтвердили вывод: аффинность MJ18 к мышиному B7-H3 была примерно в 7 000 раз слабее, чем у EPNCIR122 — значительно ниже типичных значений для терапевтических антител.
Когда антитела «цепляют» неправильные клетки
История не ограничилась слабым связыванием. В клетках селезёнки дополнительные тесты показали, что MJ18 и похожие крысиные антитела распознаются мышиными Fc‑рецепторами — молекулами на иммунных клетках, которые естественно связывают хвостовую часть антител. Блокирование этих рецепторов резко снижало сигнал MJ18, что подразумевает: большая часть видимого связывания происходила из‑за того, что иммунные клетки захватывали само антитело, а не из‑за ориентира MJ18 на конкретный поверхностный белок. Попытки идентифицировать уникального белкового партнёра MJ18 на иммунных клетках выявили только кандидатов на уровне, неотличимом от фонового шума. В совокупности данные указывают, что MJ18 действует в основном как низкоаффинное, неспецифическое антитело, взаимодействие которого определяется захватом через Fc‑рецепторы, а не точным распознаванием B7-H3.
Что это значит для будущих исследований
Для неспециалистов вывод прост: B7-H3 остаётся привлекательной мишенью во многих опухолях, но антитело MJ18 не является надёжным инструментом. Оно слабо связывает B7-H3 у мышей и не воспроизводит сильный контроль над опухолью, наблюдавшийся при удалении гена B7-H3. Ранние мышиные исследования, сообщавшие о драматических преимуществах при использовании MJ18, возможно, отражали другие эффекты — например, взаимодействие хвоста антитела с рецепторами иммунных клеток — а не истинную блокаду B7-H3. Авторы настаивают, что полю необходимо срочно получить хорошо валидированные, высокоаффинные антитела к мышиному B7-H3, и что исследователи должны рутинно подтверждать специфичность и силу таких инструментов. Только при наличии надежных реагентов можно доверять выводам из животных моделей при разработке следующего поколения терапий, нацеленных на B7-H3 для пациентов.
Цитирование: Gulyás, D., Nammor, T., Frizzell, J. et al. Low-affinity binding of anti-B7-H3 clone MJ18 to murine B7-H3 fails to induce tumor regression. Sci Rep 16, 9519 (2026). https://doi.org/10.1038/s41598-026-40628-x
Ключевые слова: B7-H3, иммунотерапия рака, валидация антител, иммунные контрольные точки, модель опухоли