Clear Sky Science · ru
Определение пола и генотипа в яйце с помощью ПЦР: вклад в принципы 3R при разведении кур
Почему важно то, что происходит внутри яйца
Ежегодно миллионы петушков погибают вскоре после вылупления, потому что они бесполезны для яйценоскости. Одновременно лаборатории по всему миру выводят больше животных, чем нужно, просто потому что не могут заранее определить пол или генетический состав эмбриона. В этом исследовании демонстрируется практический способ «прочитать» пол и генотип цыплёнка, пока он ещё развивается в яйце, с помощью стандартных ДНК‑тестов. Выполняя это рано и аккуратно, метод направлен на предотвращение вылупления лишних животных и снижение страданий без необходимости дорогого промышленного оборудования.
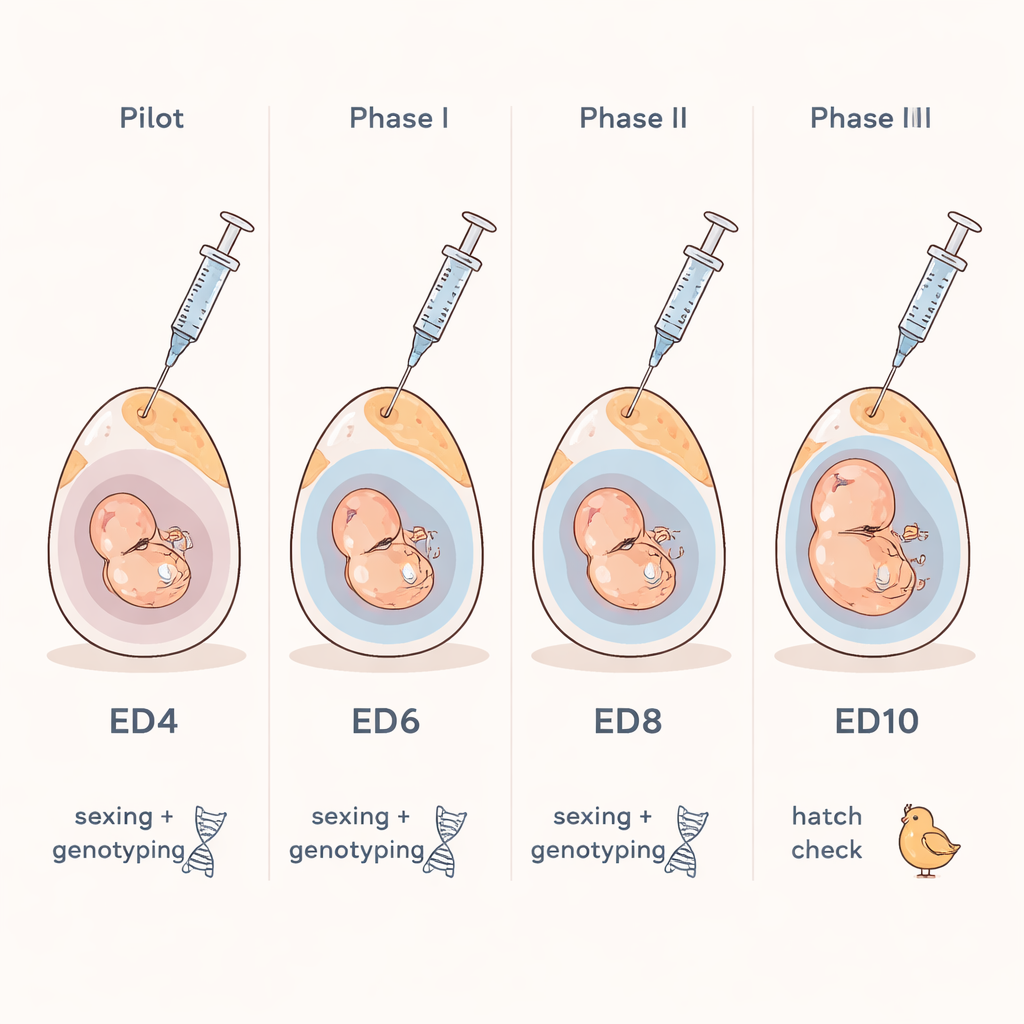
Заглянуть внутрь яйца, не раскрывая его
Учёные сосредоточились на простом вопросе: можно ли безопасно взять крошечную пробу жидкости из оплодотворённого куриного яйца и использовать её для определения пола эмбриона и ключевых генетических признаков? Они опирались на концепцию, знакомую из медицины человека, где врачи исследуют околоплодные воды для поиска генетических состояний. У кур образуется тонкий мешок, заполненный жидкостью — аллантоис — вокруг эмбриона по мере его роста. К седьмому дню инкубации в этом мешке скапливается достаточно жидкости, чтобы тонкая игла могла добраться до неё, не касаясь самого эмбриона. Команда использовала яркий свет, чтобы найти воздушную камеру у тупого конца яйца, проделала отверстие размером с булавочную головку в скорлупе и отсосала всего несколько капель жидкости маленьким шприцем.
От нескольких капель к генетическому отпечатку
Жидкость, взятая из яиц на ранних стадиях развития, содержит лишь крошечные количества ДНК. Чтобы обойти это ограничение, учёные сначала амплифицировали весь генетический материал из каждой пробы, создавая множество копий без изменения содержания. Затем они применили два рутинных лабораторных теста: стандартную полимеразную цепную реакцию (ПЦР) и вариант, называемый Kompetitive Allele Specific PCR (KASP). Обе методики различают половые хромосомы самцов и самок и способны выявлять специфические генетические маркеры, например мутацию, вызывающую голубую окраску скорлупы, или наличие лабораторно внесённого гена в специализированных исследовательских линиях. На более чем 800 яйцах разных пород — включая коммерческих несушек, пёстрые помеси Арауканы и генетически модифицированную исследовательскую линию — эти методы дали корректные результаты примерно в 92–100% случаев.
Поиск наименее опасного момента для взятия пробы
Слишком ранняя проба рискует повредить хрупкие структуры, жизненно важные для эмбриона, тогда как слишком поздняя оставляет мало времени на применение результатов. Чтобы определить оптимальное окно, команда сначала выращивала эмбрионы в бесскорлупной культуре, наблюдая за тем, как со временем расширяются оболочки и жидкостные полости. Затем они провели серию поэтапных проб в интактных яйцах. Жидкость можно было собирать с четвёртого дня, но в эти ранние дни успешность ДНК‑тестов была ниже, а процедура технически сложнее. Сравнивая показатели вылупляемости в проколотых и нетронутых контрольных яйцах, исследователи обнаружили, что седьмой день представляет наилучший компромисс: в этот момент в аллантоисе достаточно прозрачной жидкости, ДНК‑тесты работали надёжно, и большинство эмбрионов выживали до вылупления. На этом этапе оставалось ещё несколько дней до предполагаемого начала восприятия боли у эмбриона, что даёт этический запас для принятия решений.
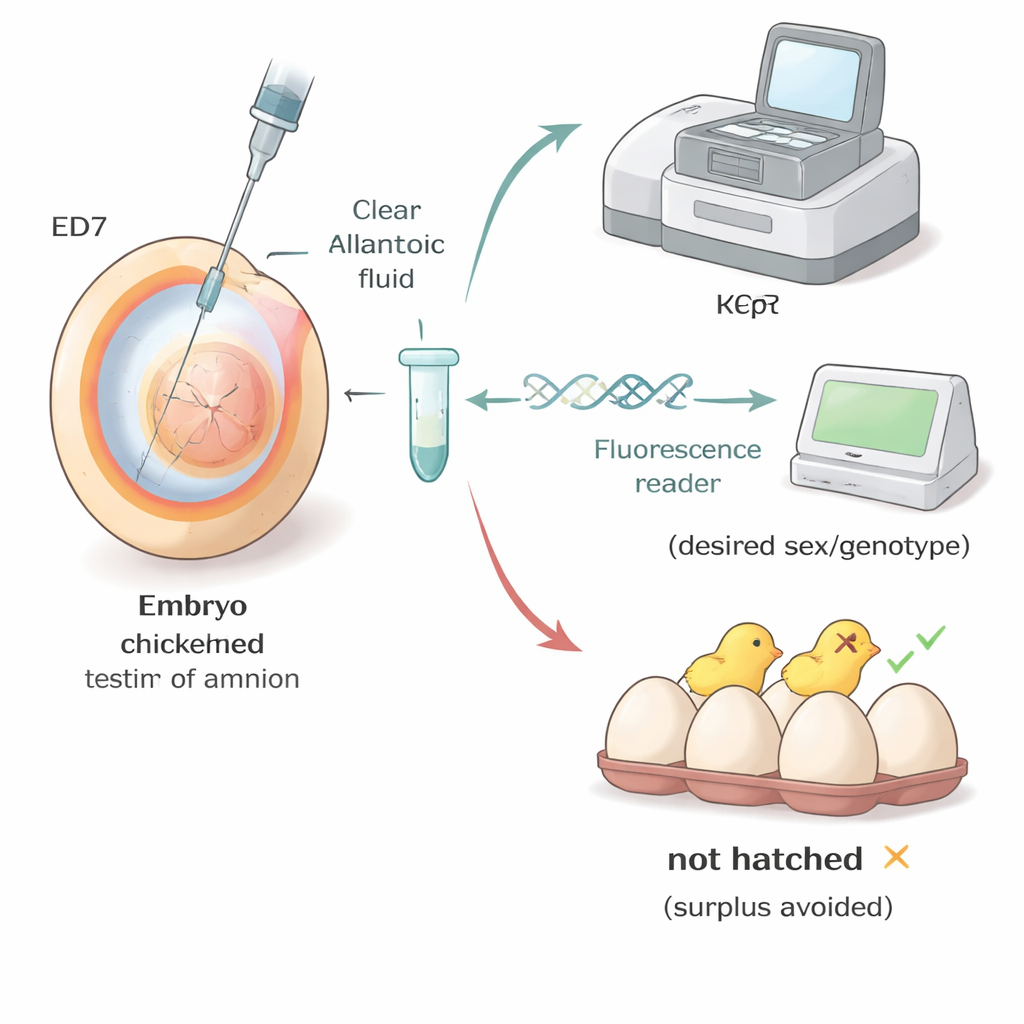
Применение метода в реальных стадах
Исследователи испытали свою методику в условиях, близких к используемым на племенных фермах и в университетских лабораториях. В коммерческих линиях коричневых и белых несушек яйца, взятые на пробу между четвёртым и седьмым днями, показали, что вылупляемость в целом улучшалась при более позднем заборе, а лучшие результаты вновь наблюдались на седьмой день. В специализированной «реципиентной» линии, используемой для продвинутой работы с генетикой, команда пошла дальше: они определяли пол и генотип эмбрионов на седьмой день, а затем оставляли для дальнейшего вылупления только тех, кто соответствовал желаемой комбинации пола и генов. Почти все отобранные эмбрионы вылупились в здоровых птенцов, которые выросли ожидаемо, что демонстрирует: ранний отбор может резко сократить число нежелательных животных без ущерба для качества цыплят.
Что это означает для благополучия животных и науки
Для неспециалиста основной вывод прост: с помощью укола булавочной иглы и рутинных лабораторных средств теперь можно узнать, пока цыплёнок ещё находится внутри яйца, является ли он самцом или самкой и несёт ли он конкретные генетические признаки. Исследование показывает, что проведение этой процедуры около седьмого дня инкубации технически надёжно и достаточно деликатно, чтобы большинство эмбрионов выживало. Позволяя удалять нежелательных эмбрионов до того, как они, вероятно, способны ощущать боль, подход поддерживает широко признанные принципы 3R: замену, сокращение и уточнение использования животных в науке. Для инкубаторов и научных лабораторий эта методика предлагает реалистичный путь к уменьшению числа лишних животных, более рациональному использованию ресурсов и повышению стандартов благополучия — без необходимости сложных промышленных машин.
Цитирование: Dierks, C., Förster, A., Meunier, D. et al. In ovo sexing and genotyping using PCR techniques: a contribution to the 3R principles in chicken breeding. Sci Rep 16, 7464 (2026). https://doi.org/10.1038/s41598-026-40562-y
Ключевые слова: эмбрион курицы, определение пола in ovo, ПЦР‑генотипирование, благополучие животных, принципы 3R