Clear Sky Science · ru
Открытие гидрокситриазола как потенциального ингибитора глиоксилазы‑I с использованием методов компьютерного дизайна лекарств
Почему остановка маленькой «пылесосной» системы клетки может бороться с раком
Раковые клетки часто растут так быстро, что тонут в собственных отходах. Одна из их уловок выживания — встроенная «бригада уборки», которая детоксифицирует вредные побочные продукты расщепления сахара. В этом исследовании изучают, как выключить одного ключевого участника этой бригады — фермент глиоксилазу‑I — с помощью компьютеров, перебирающих десятки тысяч молекул, и экспериментов для проверки лучших кандидатов. Цель — найти новые стартовые точки для лекарств, которые однажды могли бы позволить врачам избирательно отравлять раковые клетки изнутри.
Скрытая система утилизации внутри наших клеток
Каждая клетка постоянно расщепляет сахар для получения энергии, и этот процесс порождает реактивный побочный продукт — метилглиоксаль. В нормальных количествах наш организм превращает метилглиоксаль в безвредную молочную кислоту с помощью системы глиоксаля — двухступенчатого пути, в котором важную роль играет вспомогательная молекула глутатион. Глиоксилаза‑I осуществляет первый и самый критический шаг в этой цепочке. Раковые клетки, которые сжигают сахар с бешеной скоростью, сильно зависят от глиоксилазы‑I, чтобы не допустить накопления метилглиоксаля до токсичных уровней. Если этот фермент блокировать, метилглиоксаль накапливается и может подтолкнуть повреждённые клетки к программируемой гибели. Это делает глиоксилазу‑I привлекательной мишенью для противораковых препаратов, бьющих по фундаментальной слабости опухолевого метаболизма.
Поиск в химическом пространстве с помощью кремния и статистики
Вместо того чтобы испытывать случайные вещества в лаборатории, исследователи использовали компьютерный дизайн лекарств для поиска в большой коммерческой коллекции более 50 000 малых молекул. Специализированное программное обеспечение сначала очищало и стандартизировало каждую молекулу, затем прогнозировало её трёхмерную форму и поведение при физиологическом pH. Быстрый этап виртуального скрининга оценивал, насколько хорошо каждый кандидат может поместиться в активном центре глиоксилазы‑I. Команда затем применила простые правила относительно размера, растворимости и других свойств, пригодных для лекарств, чтобы отсеять молекулы, маловероятно работающие в организме. Более детальная программа докинга проанализировала, как наиболее перспективные молекулы могут ориентироваться внутри фермента, особенно как они могут добираться до атома цинка и захватывать его — того самого металла, который лежит в основе химии глиоксилазы‑I.
Новый способ захвата металлического ядра фермента
Ранние попытки блокировать глиоксилазу‑I фокусировались на известных химических группах, таких как карбоксильные и гидроксамовые кислоты, которые хорошо связывают металлы, но часто страдают низкой стабильностью или нежелательными побочными эффектами. В этом исследовании выявили другой тип «металло‑захватывающей» единицы — кольцо гидрокситриазола. Среди шестнадцати молекул с наивысшими рейтингами, выбранных для покупки и лабораторного тестирования, одна с этим кольцом — под кодом SPB07393SC — оказалась выдающейся. В виртуальном докинге её гидрокситриазоловая группа тянулась к атому цинка, а два ароматических кольца упрятывались в близлежащие гидрофобные карманы фермента. Компьютерное моделирование комплекса в течение десятков наносекунд показало, что молекула оставалась плотно связанной: расстояния были стабильными, конформация белка компактной, а сеть водородных связей сохранялась.
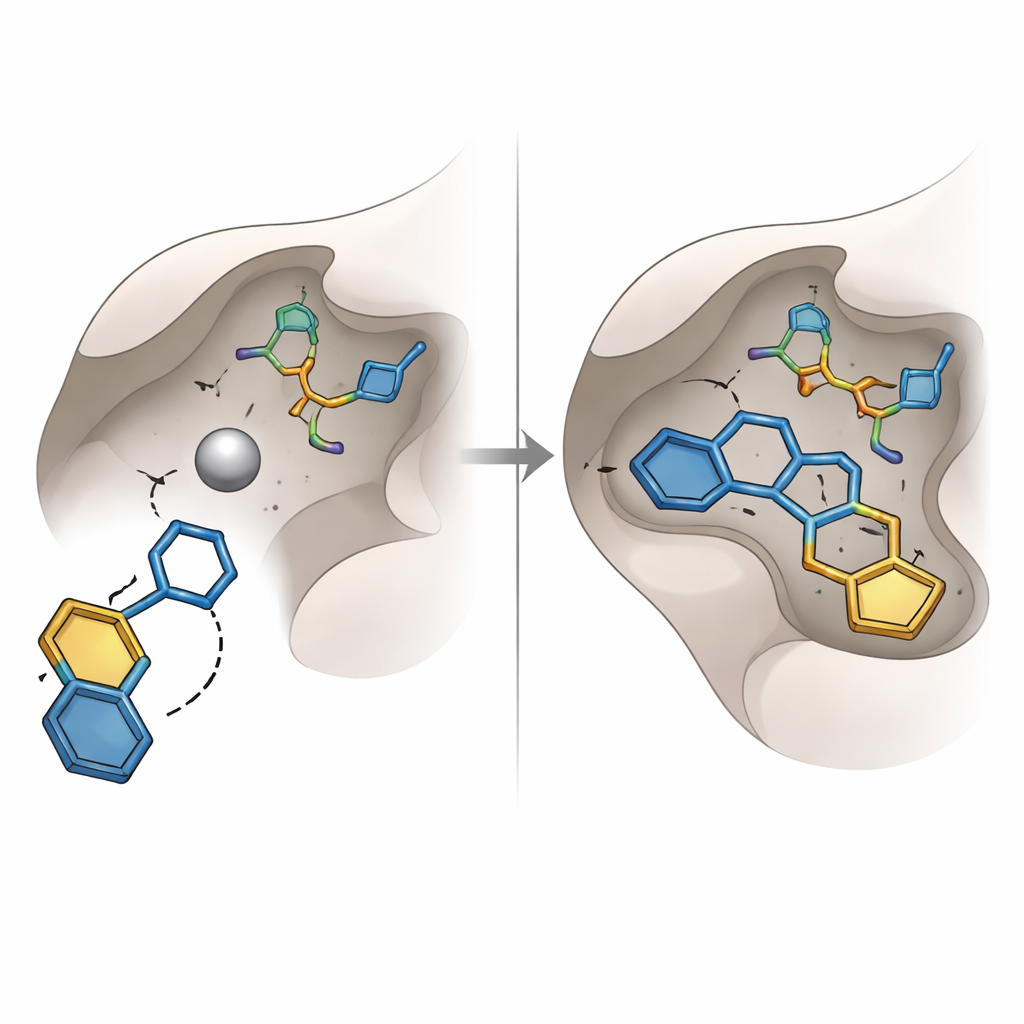
Проверка предсказаний на практике
Чтобы выяснить, переносились ли компьютерные модели в реальный мир, команда измерила, насколько эффективно отобранные молекулы замедляют активность очищенной человеческой глиоксилазы‑I в планшетном (микропланшетном) анализе. Пятнадцать из шестнадцати кандидатов показали лишь слабую или незначительную ингибицию в протестированных условиях, что подчёркивает подводные камни полагания только на статические оценки докинга. В отличие от них, SPB07393SC сильно ингибировал фермент, с промежуточной микромолярной активностью, что делает его прочным ранним «хитом», но не готовым лекарством. Дополнительные программные средства предсказали, что эта молекула должна обладать приемлемой растворимостью, хорошей абсорбцией, способностью при необходимости проникать в мозг и низкой вероятностью вызывать определённые генетические или печёночные токсичности, хотя эти предсказания безопасности требуют экспериментальной верификации.
Что это значит для будущих противораковых препаратов
Работа представляет гидрокситриазол как новый способ анкеровки кандидатов в лекарства к атому цинка в ядре глиоксилазы‑I, расширяя набор химических приёмов, доступных разработчикам препаратов. Хотя SPB07393SC сам по себе — лишь отправная точка, его сочетание блокирующей активности, предсказанных лекарственных свойств и стабильного связывания в динамических симуляциях делает его многообещающим каркасом для дальнейшей оптимизации. Более широко, исследование демонстрирует и сильные стороны, и ограничения компьютерно‑направленного скрининга: он может быстро сузить огромные химические библиотеки до нескольких реальных претендентов, но тщательные лабораторные эксперименты по‑прежнему необходимы, чтобы выяснить, какие молекулы действительно выключают фермент, на который полагаются раковые клетки для управления своими токсичными отходами.
Цитирование: Al-Qazzan, M., Al-Balas, Q., Alnajjar, B. et al. Discovery of hydroxytriazole as a potential glyoxalase-I inhibitor utilizing computer-aided drug design techniques. Sci Rep 16, 9945 (2026). https://doi.org/10.1038/s41598-026-40497-4
Ключевые слова: глиоксилаза I, метаболизм рака, компьютерный дизайн лекарств, ингибиторы, связывающие цинк, молекулярный докинг