Clear Sky Science · ru
Реактивные на стимулы хитозановые покрытия на ферритовых нанонесителях для направленной доставки капсаицина и зависимости биоактивности, избирательной к клеткам HepG2, от сердцевины
Пряность с скрытой силой
Чили придают еде не только остроту: жжение вызывается капсаицином — природным соединением, которое также способно убивать раковые клетки. Однако применение капсаицина в медицине усложнено: он плохо растворим в воде, быстро выводится из организма и при высоких дозах раздражает здоровые ткани. В этом исследовании рассматривают способ приручить эту «жгучую» молекулу, поместив её внутрь крошечных умных частиц, которые могут безопасно переносить капсаицин по кровотоку и высвобождать его преимущественно внутри опухолей печени.
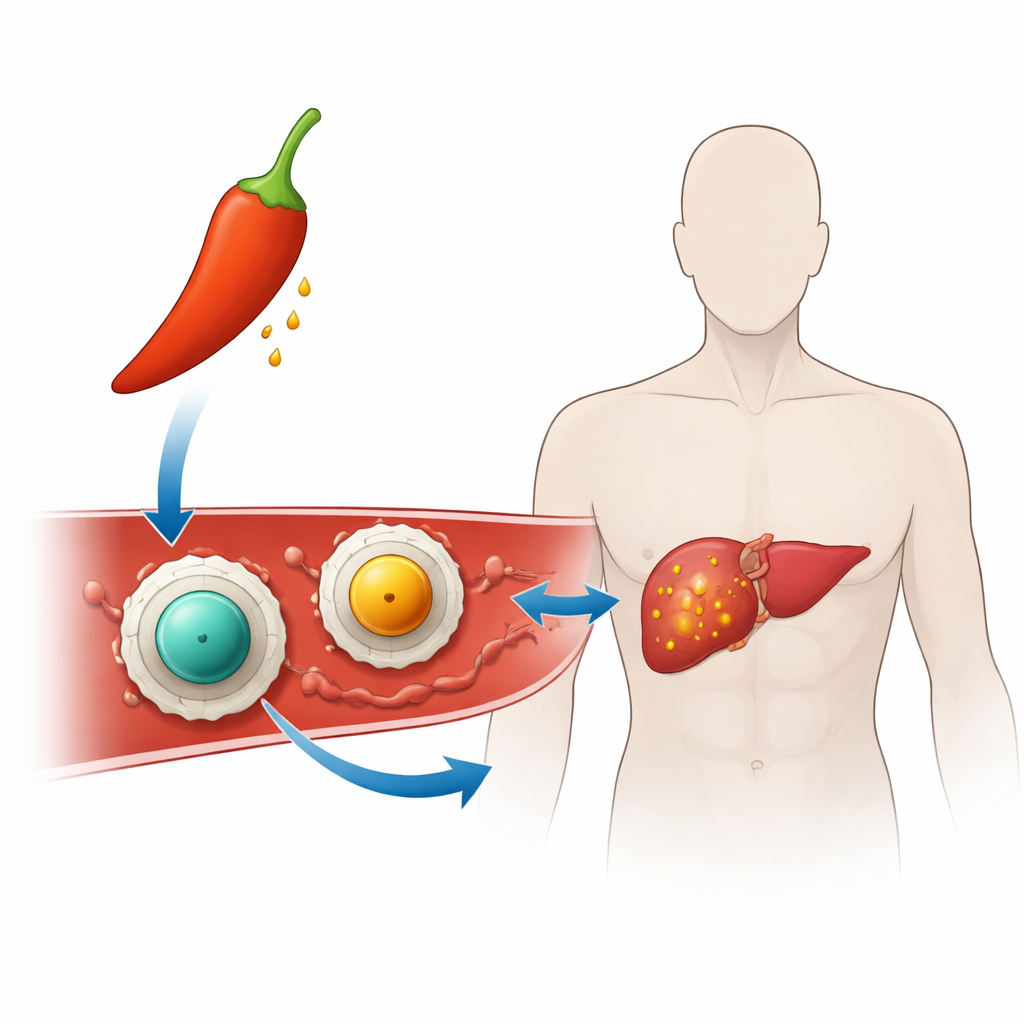
Преобразование острого перца в направленную терапию
Исследователи создали «нанонесители» — частицы в тысячи раз меньшие, чем зерно песка — чтобы транспортировать капсаицин к раковым клеткам. Каждый нанонеситель имеет твёрдое ядро из магнитного минерала феррита (либо цинкового феррита, либо марганцевого феррита), покрытое тонкой оболочкой из хитозана — углеводоподобного вещества, получаемого из панцирей ракообразных и уже применяемого в медицине и пищевой промышленности. Это покрытие улучшает суспендируемость частиц в воде и помогает им прилипать к поверхности клеток и к ДНК, что важно для противоракового действия. Загружая капсаицин в хитозановую оболочку, команда рассчитывала сохранить лекарство стабильным и скрытым до тех пор, пока оно не достигнет агрессивной среды внутри опухоли.
Умное высвобождение в опухолевых условиях
Ключевая особенность опухолей — их склонность к большей кислотности и повышенному содержанию некоторых антиоксидантов, таких как глутатион, по сравнению со здоровыми тканями. Команда сконструировала нанонесители так, чтобы те чувствовали эти условия. В лабораторных тестах при нормальном pH крови менее 10 процентов загруженного капсаицина вышло из частиц за двое суток, что указывает на то, что частицы смогут безопасно нести груз во время циркуляции. В условиях, имитирующих опухоль — при более высокой кислотности и избытке глутатиона — частицы выпустили около трети капсаицина. Такое «вкл/выкл» поведение означает, что лекарство с большей вероятностью будет освобождено внутри раковых клеток, а не по пути, что потенциально повышает пользу и снижает побочные эффекты.
Как состав частиц формирует безопасность и эффективность
Хотя два типа нанонесителей выглядели схожими внешне, их внутренние ядра сыграли существенную роль. Частицы на базе цинка tended быть меньшими и сильнее удерживали капсаицин, тогда как на базе марганца были более пористыми и легче отдавали препарат. Оба типа имели выраженный положительный поверхностный заряд, что помогает им взаимодействовать с отрицательно заряженными поверхностями клеток и ДНК. Тесты на образцах человеческой крови показали очень низкое повреждение эритроцитов, а пустые частицы оказались щадящими для нормальных клеток легкого, подтверждая их базовую безопасность. После загрузки капсаицином обе системы стали более активными против клеток рака печени, но марганцевая версия достигла наилучшего баланса: она сильнее повреждала раковые клетки, оставаясь относительно безопасной для нормальных клеток.
Не только против рака: дополнительные защитные эффекты
Нанонесители выполняли не только роль доставки капсаицина. В некоторых испытаниях они замедляли рост ряда патогенных бактерий так же эффективно, как стандартный антибиотик, и помогали нейтрализовать вредные свободные радикалы, связанные с воспалением и повреждением тканей. Точные оптические измерения показали, что после упаковки в феррит–хитозановые частицы капсаицин сильнее и стабильнее связывается с ДНК. Быстрые кинетические эксперименты выявили двухступенчатый процесс: сначала ДНК прочно притягивается к положительно заряженной поверхности частицы, затем комплекс реорганизуется в более плотное и долговременное соединение. Эти усиленные взаимодействия вероятно объясняют, почему загруженные частицы демонстрируют более выраженные противораковые, антимикробные и антиоксидантные эффекты, чем капсаицин или ферритовые частицы по отдельности.
Что это может означать для пациентов
Пока что эти результаты получены в лабораторных условиях, а не у пациентов. Тем не менее они указывают на то, что тщательно спроектированные нанонесители могут превратить пряный пищевой ингредиент в более точное противораковое средство. Выбор правильного материала сердцевины и оболочки позволил создать крошечные «посылки», которые сохраняют капсаицин стабильным, безопасно переносят его в крови и предпочтительно разгружают в опухолевых условиях, особенно в клетках рака печени. Среди протестированных вариантов частицы на основе марганца показали наиболее перспективное сочетание направленного повреждения рака, низкого вреда для нормальных клеток и дополнительных антимикробных и антиоксидантных преимуществ. При дальнейшем исследовании на животных и проверках безопасности такие «умные» частицы, вдохновлённые перцем, однажды могут способствовать более щадящим и целенаправленным терапиям рака печени и, возможно, других заболеваний.
Цитирование: Bakr, E., Elshami, F.I., Okba, E.A. et al. Stimuli-responsive chitosan-coated ferrite nanocarriers for targeted capsaicin delivery and core-dependent HepG2-selective bioactivity. Sci Rep 16, 8957 (2026). https://doi.org/10.1038/s41598-026-40433-6
Ключевые слова: капсаицин, рак печени, наночастицы, направленная доставка лекарств, носители, реагирующие на стимулы