Clear Sky Science · ru
Альтернативный сплайсинг и дифференциальная экспрессия генов при изменениях восприимчивости эндометрия у пациенток с рецидивирующей неудачей имплантации
Почему некоторые эмбрионы не имплантируются
Многие пары, проходящие через экстракорпоральное оплодотворение, сталкиваются с досадной загадкой: даже при переносе эмбрионов высокого качества беременность может не наступить. В этом исследовании внимательно изучается слизистая оболочка матки — эндометрий — чтобы понять, почему у некоторых женщин систематически не происходит имплантация. Анализируя, какие гены включаются и выключаются, как их сообщения разрезаются и перестраиваются, а также как ведут себя иммунные клетки в короткое окно, когда матка готова принять эмбрион, исследование выявляет новые молекулярные подсказки, которые в будущем могут помочь создать более точные тесты и методы лечения.
Краткое «приёмное» окно матки
Имплантация возможна только в течение короткого промежутка в каждом цикле, когда слизистая становится «восприимчивой». Исследователи сравнили образцы ткани от 90 фертильных женщин и 73 женщин с рецидивирующей неудачей имплантации, все взятые в три ключевых момента: непосредственно перед тем, как слизистая становится восприимчивой, в период восприимчивого окна и вскоре после его закрытия. С помощью высокопроизводительного секвенирования РНК они измеряли, какие гены активны и как обрабатываются их РНК‑сообщения. Такой дизайн позволил проследить, как здоровая слизистая готовится к эмбриону и как эта подготовка нарушается у женщин, которые многократно не могут добиться имплантации, несмотря на качественные эмбрионы. 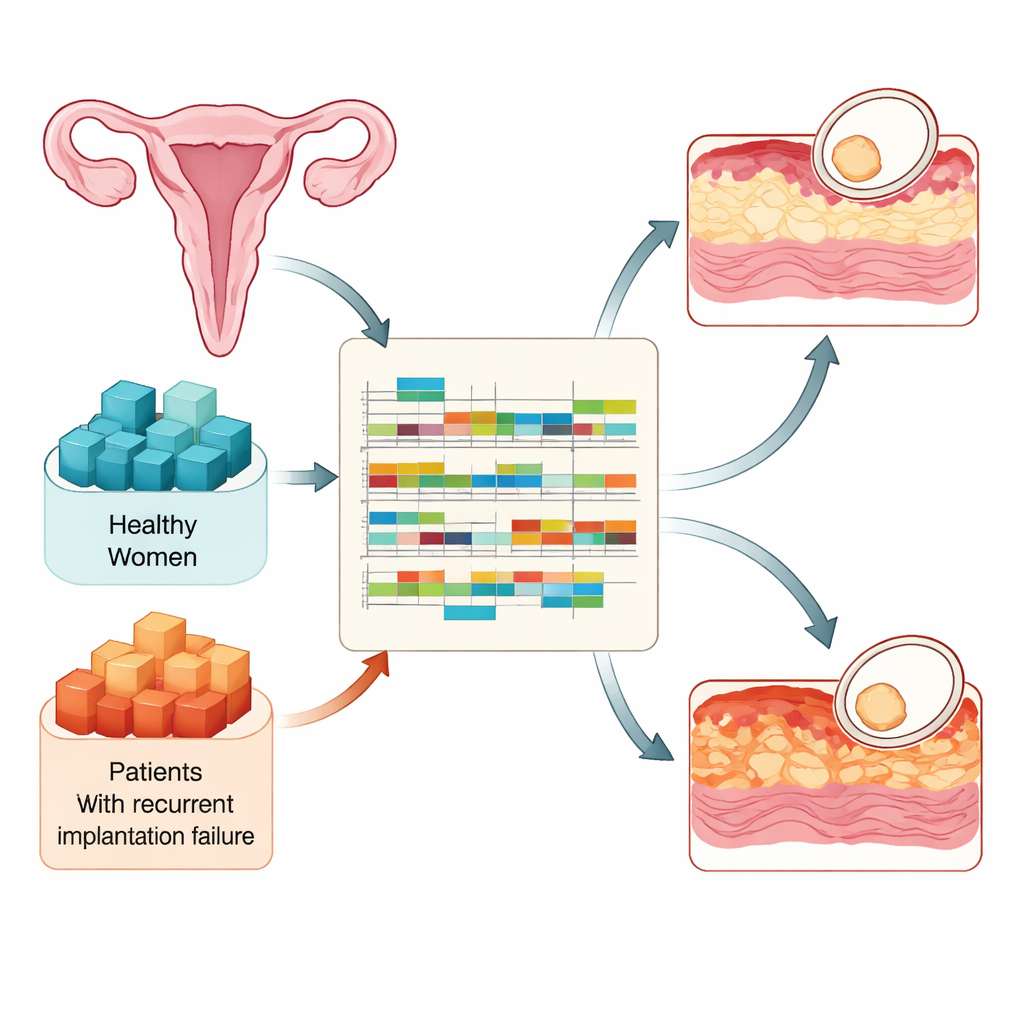
Сообщения генов: разрезы и перестановки
Помимо учета уровней активности генов, команда сосредоточилась на альтернативном сплайсинге — процессе, благодаря которому один ген может быть разрезан на разные варианты сообщений, дающие разные формы белков. Они обнаружили более миллиона событий сплайсинга в сравнениях, при этом особенно распространены были два типа — пропуск целых участков и выбор между взаимоисключающими участками. При рассмотрении только частых и статистически надежных изменений выявилось от сотен до тысяч сдвигов в сплайсинге при переходе слизистой из невосприимчивого в восприимчивое состояние, особенно при переходе от ранней (предвосприимчивой) стадии к окну имплантации. Многие из этих изменений происходили даже при неизменном общем уровне гена, то есть форма белка менялась без изменения общей активности гена.
Клетки прилипают, перестраиваются и «разговаривают» с иммунной системой
Гены, затронутые измененным сплайсингом и изменениями активности, были тесно связаны с тем, как клетки сцепляются друг с другом, как перестраивается их цитоскелет и как они посылают и принимают иммунные сигналы. Эти функции жизненно важны, когда эндометрий превращается из простой барьерной поверхности в среду, способную принять и закрепить эмбрион при одновременном ремоделировании сосудов. У фертильных женщин и у женщин с неудачами имплантации в восприимчивую фазу наблюдались сильные перестройки в этих путях, но у пациенток с рецидивами сплайсинговые изменения были более частыми или имели иной рисунок. Некоторые вовлеченные гены уже предлагались в качестве маркеров оптимального окна имплантации, что подтверждает идею о том, что важна не только активность генов, но и точная форма их продуктов для определения истинной готовности слизистой.
Иммунные клетки и ключевой регулятор сплайсинга
Команда также оценивала типы иммунных клеток в ткани на основе тех же данных РНК. У женщин с неудачей имплантации в восприимчивой фазе отмечалось меньше цитотоксических Т‑клеток и покоящихся натуральных киллеров, но больше моноцитов и некоторых макрофагов по сравнению с ранними фазами. Позже, после закрытия окна, соотношения снова менялись, включая изменения в активированных натуральных киллерах и подтипах макрофагов. Некоторые из этих сдвигов в иммунных клетках тесно коррелировали с конкретными событиями сплайсинга, что наводит на мысль о связи между переработкой генетических сообщений и иммунным балансом. Среди белков, контролирующих сплайсинг, выделялся один — KHDRBS3 — как центральный узел, связанный со многими измененными событиями и систематически снижавший уровень при наступлении восприимчивой фазы как у фертильных, так и у затронутых женщин. Это говорит о том, что он может способствовать переключению паттернов сплайсинга, сопровождающему открытие окна имплантации. 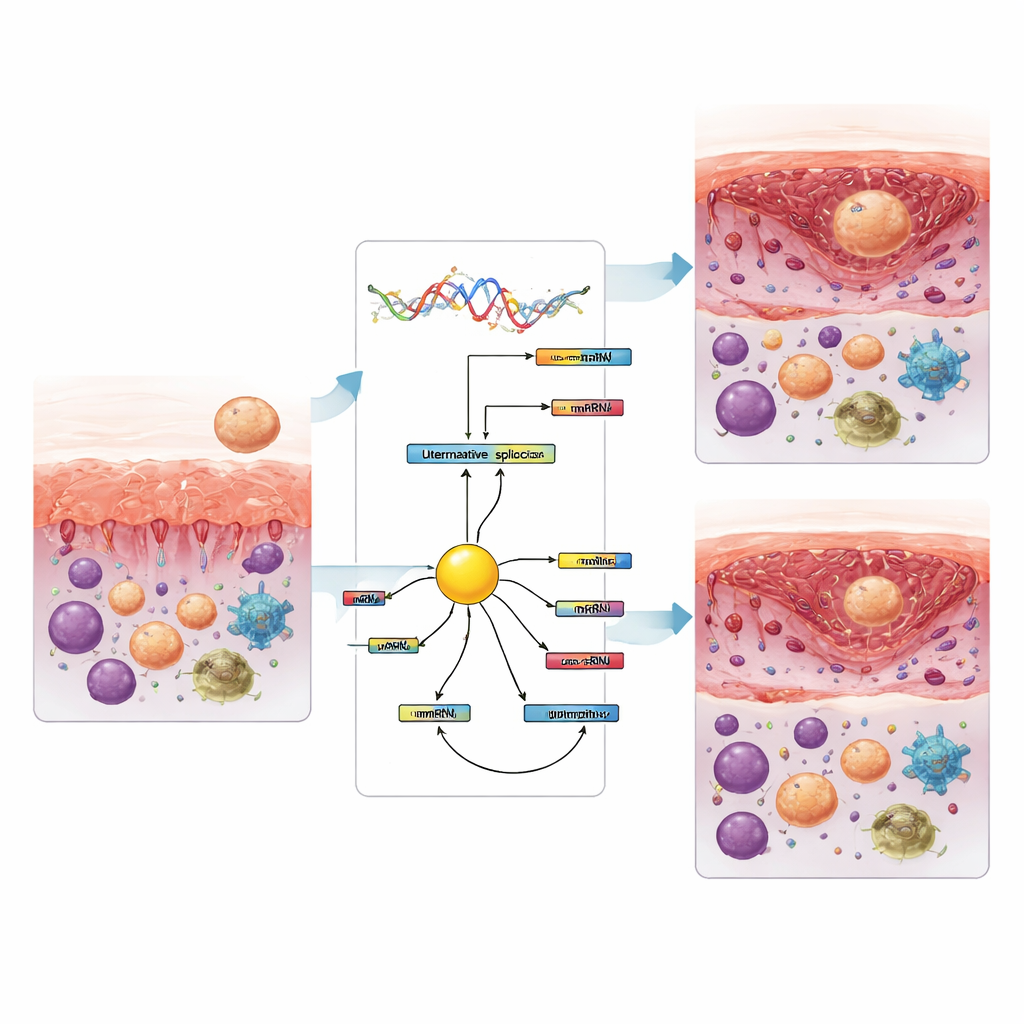
Указания на будущие тесты и терапии
Чтобы превратить эти молекулярные закономерности в возможные терапевтические подходы, исследователи проверили, могут ли существующие малые молекулы противодействовать выявленным аномальным подписям сплайсинга. Сопоставив списки генов с крупными базами данных реакции на препараты, они выделили несколько одобренных или экспериментальных соединений, нацеленных на гены, связанные с имплантацией, включая вещества, влияющие на иммунные ответы или гормонально связанные пути. Хотя эти препараты далеки от клинического применения в данном контексте, они дают отправную карту для лабораторного тестирования.
Что это значит для пациенток
В целом исследование показывает, что неудача имплантации — это не просто «неправильные» гены, а то, как эти гены редактируются в разные сообщения и как со временем настраивается иммунная среда матки. Работа выделяет KHDRBS3 и родственные факторы как перспективные регуляторы этого процесса и обнаруживает координированные сдвиги в иммунных клетках, которые могут либо поддерживать, либо препятствовать попытке эмбриона закрепиться. В долгосрочной перспективе такие данные могут привести к более тонким тестам для определения истинного времени и качества восприимчивого окна женщины, а также к целенаправленным вмешательствам, мягко корректирующим генетическое «сообщение» или иммунный баланс, чтобы дать эмбрионам больше шансов на имплантацию.
Цитирование: Wang, Ml., Lu, Bj., Lu, X. et al. Alternative splicing and differential gene expression during changes in endometrial receptivity in patients with recurrent implantation failure. Sci Rep 16, 9754 (2026). https://doi.org/10.1038/s41598-026-40386-w
Ключевые слова: восприимчивость эндометрия, рецидивирующая неудача имплантации, альтернативный сплайсинг, маточные иммунные клетки, вспомогательные репродуктивные технологии