Clear Sky Science · ru
Адаптивный отбор примеров для прототипно-объяснимого обнаружения митозов в цифровой патологии
Почему это важно для ухода за пациентами с раком
Когда патологи рассматривают образцы опухолей под микроскопом, подсчёт числа активно делящихся клеток помогает судить об агрессивности опухоли и выбирать лечение. Искусственный интеллект теперь может быстро находить такие делящиеся клетки на цифровых слайдах, но его решения часто остаются загадкой даже для экспертов. В этой статье предложен метод под названием Adaptive Example Selection (AES), который позволяет системе ИИ «показать свои доводы», указывая на реальные прошлые случаи, подтверждающие или опровергающие каждое решение, делая автоматическое обнаружение митозов более прозрачным и клинически надёжным.
Задача: обнаружить делящиеся клетки
Делящиеся клетки опухоли, или митотические фигуры, малы, редки и визуально разнообразны. При обычном розово-фиолетовом окрашивании они могут сильно напоминать безвредные структуры, например умирающие клетки или некоторые клетки иммунной системы. Экспертам приходится просматривать гигантские цифровые слайды в поисках таких клеток — это медленный, утомительный процесс, подверженный расхождениям во мнениях. Современные глубокие сети могут сопоставимо или лучше справляться с этой задачей, но ведут себя как «чёрные ящики»: они выдают оценку для каждой подозрительной клетки, не объясняя, почему. В медицине, где на решения о лечении часто зависят судьбы пациентов, такая неясность серьёзно препятствует внедрению ИИ в повседневную практику.
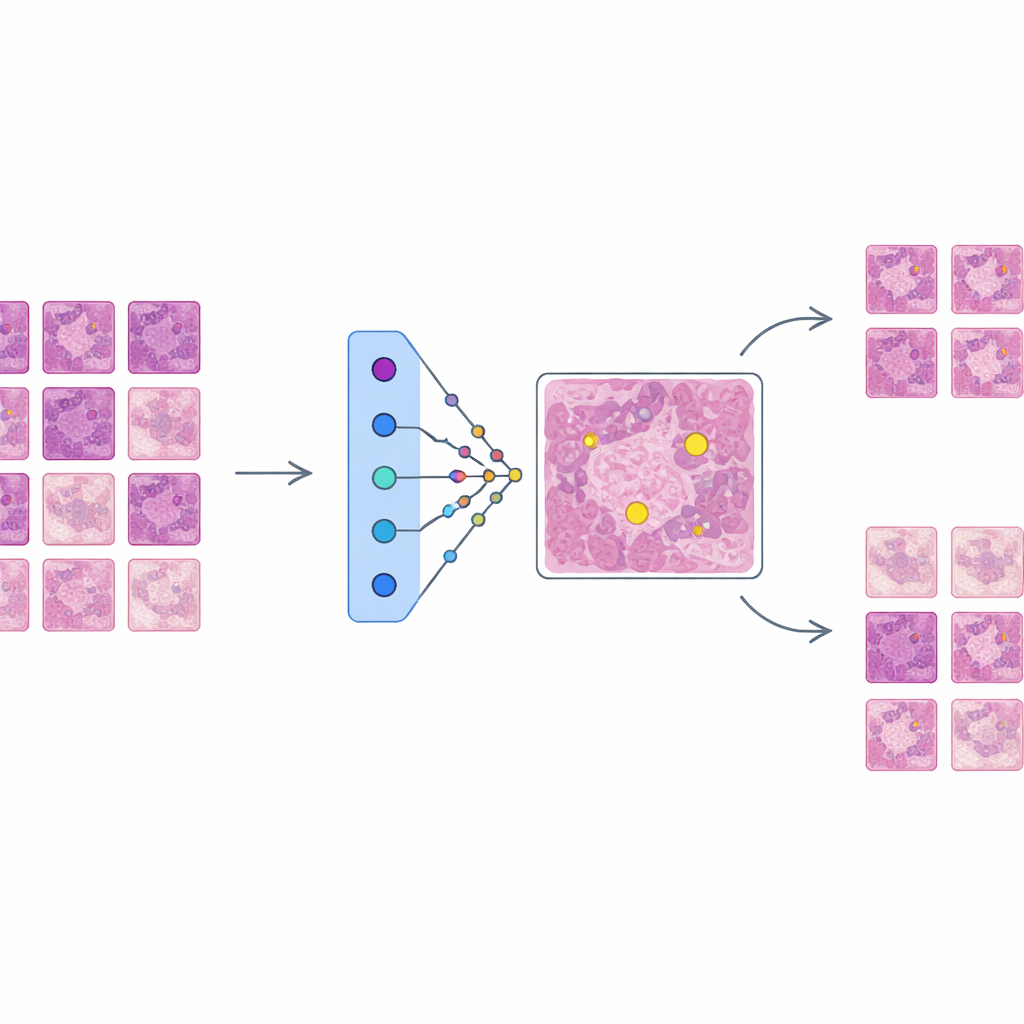
Создание сильного, но непрозрачного детектора
Авторы сначала обучают современную сеть для обнаружения объектов на базе архитектуры Faster R-CNN находить митотические фигуры в большой и разнообразной базе данных MIDOG++. Эти изображения получены как из человеческих, так и из собачьих опухолей различных типов и лабораторий и содержат более одиннадцати тысяч тщательно размеченных делящихся клеток. Чтобы сохранить тонкие детали, слайды разрезают на небольшие патчи и интенсивно аугментируют, имитируя реальные вариации окраски и съёмки. Получившийся детектор показывает устойчивую производительность по разным типам опухолей с F1-оценками до 0,84, подтверждая, что он точен, но сложен — именно такой системе требуется улучшенная объяснимость, чтобы клиницисты могли ей доверять.
Обучение ИИ объяснять свои решения с помощью примеров
AES располагается поверх обученного детектора в виде слоя интерпретируемости, не изменяя сам механизм детектора. Для каждого кандидата, отмеченного детектором как возможный митоз, AES обращается к библиотеке реальных тканевых патчей из обучающего набора. Из этой библиотеки он выбирает небольшой набор «поддерживающих» примеров, похожих на истинные митозы, и набор «противоречащих» примеров, которые больше напоминают немитотические клетки. Внутри системы AES рассматривает доверительные оценки детектора как гладкий ландшафт и использует математический инструмент — радиальные базисные функции — чтобы аппроксимировать, как меняется эта уверенность в окрестности каждого случая. Сохраняются только те прототипы, которые существенно влияют на локальную уверенность, поэтому объяснение для одного решения обычно включает около десяти тщательно отобранных примеров, а не сотни слабо релевантных.
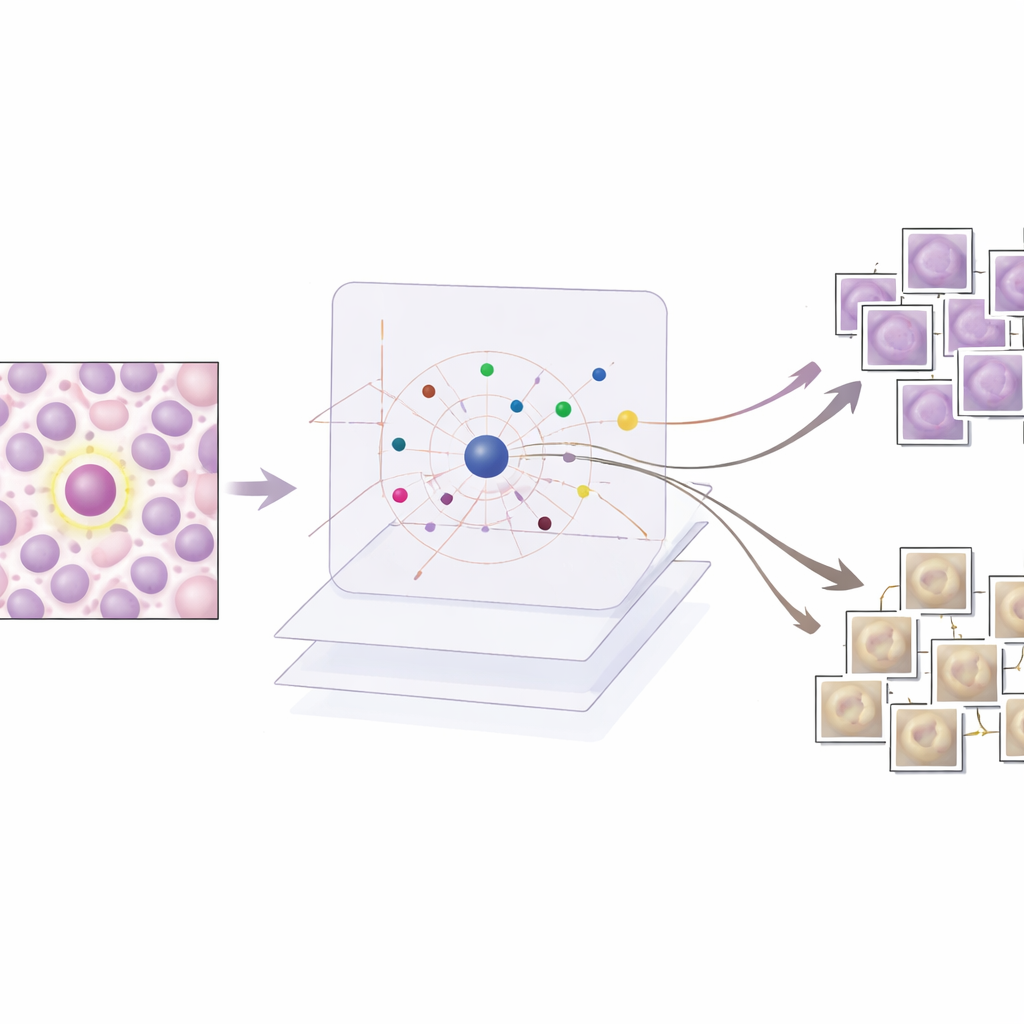
Что показывают примеры о решениях ИИ
Исследователи оценивают AES как количественно, так и качественно. В числовом выражении они демонстрируют, что компактный словарь из примерно 190 прототипных изображений может с очень высокой точностью воспроизводить доверительные оценки детектора, при этом число примеров, показываемых на случай, остаётся достаточно небольшим для обзора человеком. Качественно они рассматривают три типичных сценария. Когда детектор явно прав, AES возвращает только митотические прототипы, которые сильно поддерживают решение, что успокаивает клиницистов. Для ложных срабатываний метод показывает похожие митотические примеры, объясняющие, почему детектора ввело в заблуждение сходство текстуры или паттернов хроматина, часто вместе со слабее выраженными немитотическими прототипами, указывающими на неопределённость. В случае пропущенных митозов AES, как правило, возвращает в основном немитотические или неоднозначные примеры, указывая на «слепые зоны» в обучающих данных и подсвечивая, где нужны новые или лучше размеченные примеры.
От чёрного ящика к инструменту для совместной работы
Опираясь на каждое предсказание на горстке реальных размеченных тканевых патчей, AES заставляет сложный детектор ИИ вести себя скорее как коллега-человек, который обосновывает решения, вспоминая прошлые случаи. Система не только сообщает, вероятно ли деление клетки, но и показывает почему и с какой степенью уверенности, через сочетание и влияние поддерживающих и противоречащих прототипов. Такая конструкция позволяет патологам быстро подтверждать уверенные предсказания, фокусироваться на пограничных или запутанных зонах и выявлять систематические ошибки, которые могут направить дальнейшее обучение. Хотя метод разработан для обнаружения митозов, тот же подход можно распространить на другие задачи цифровой патологии, помогая превратить ИИ из непрозрачной автоматизации в интерпретируемого, основанного на прецедентах ассистента, которого клиницисты могут ставить под вопрос, которому могут доверять и которого могут дорабатывать.
Цитирование: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
Ключевые слова: объяснимый ИИ, цифровая патология, обнаружение митозов, модели на основе прототипов, диагностика рака