Clear Sky Science · ru
Избирательное выведение моноклональных антител через маннозный рецептор зависит от парности гликанов
Почему рисунок сахаров в лекарствах имеет значение
Многие современные блокбастеры среди лекарств — это моноклональные антитела: конструированные белки, которые могут оставаться в кровотоке неделями и высокоточно нацеливаться на заболевания, такие как рак и аутоиммунные расстройства. Но не все антитела ведут себя одинаково после введения. В этом исследовании поставлен на вид простейший на первый взгляд вопрос с большими последствиями: как тонкий «узор сахаров», присоединённых к антителу, определяет скорость его выведения организмом и может ли это также влиять на побочные эффекты, например иммунные реакции?
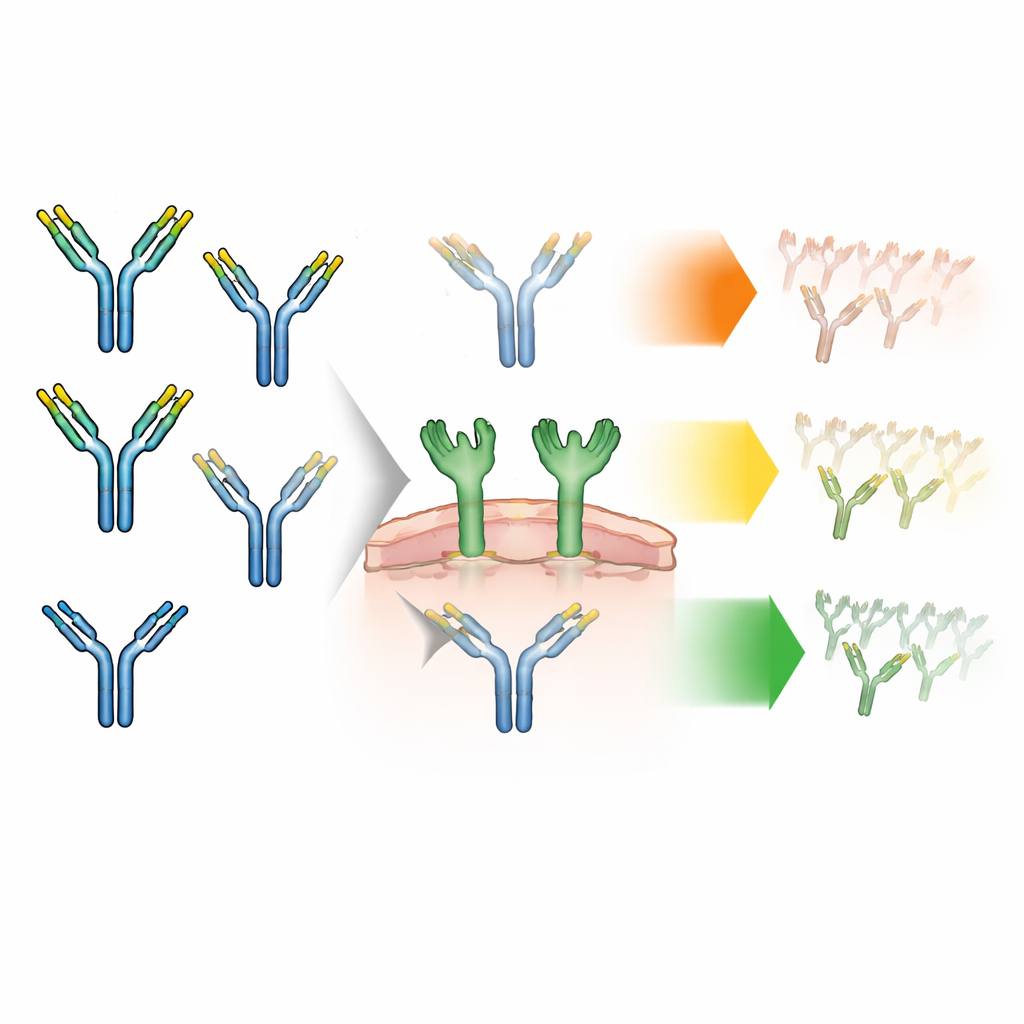
Мелкие сахара как сигналы движения
Антитела естественным образом несут короткие цепочки сахаров — гликаны — на своей белковой матрице. Эти гликаны бывают разных «вкусов». Большинство имеют «сложную» структуру, но меньшинство — «высокоманнозные», более простого типа, который в прошлых работах связывали с ускоренным удалением из крови. Каждое антитело имеет два сайта для сахаров, которые действуют как пара, и они могут совпадать (симметричные пары) или различаться (асимметричные пары). До сих пор производители препаратов в основном считали, сколько каждого типа сахара присутствует в целом, не разбираясь, как именно паруются два сахара на одном антителе. Авторы предположили, что эта схема парования может менять силу взаимодействия антител с особым белком-датчиком сахаров на иммунных клетках — маннозным рецептором — а следовательно, и скорость выведения препарата.
Сортировка антител по их сахарным парам
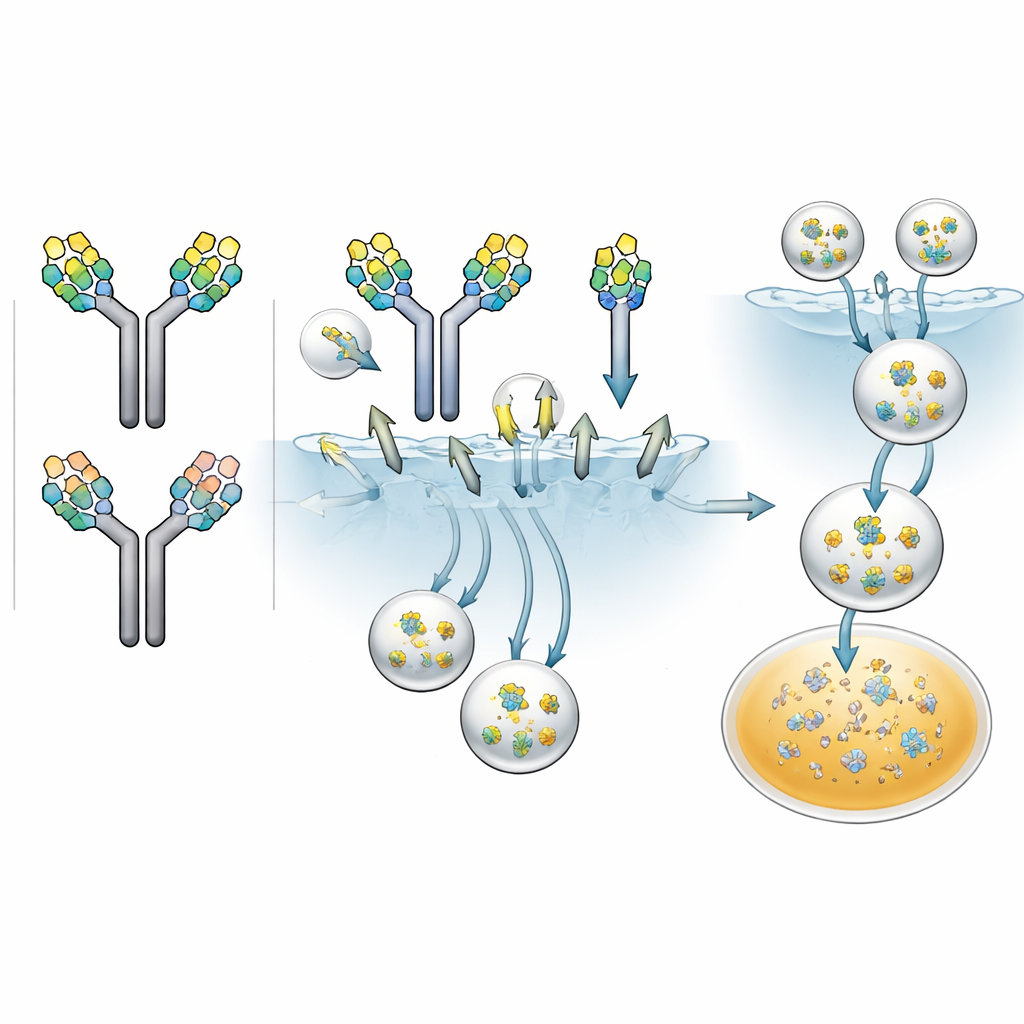
Чтобы это выяснить, команда инженерно обогатила антитела высокоманнозными гликанами и затем физически разделила их на три основные группы: антитела с двумя сложными гликанами, с одним сложным и одним высокоманнозным (асимметричные) и с двумя высокоманнозными гликанами (симметричные). Они тщательно проверили, что эти группы почти не различаются по всем остальным характеристикам: по размеру, форме, заряду и стабильности, а также по сродству к рецептору рекультивации, который обычно защищает антитела от разрушения. Это означало, что любые последующие различия, обнаруженные в клеточных экспериментах или на животных, можно было отнести именно к парности гликанов, а не к скрытым повреждениям или примесям.
Наблюдая, как клетки поглощают антитела
Далее исследователи оценили, с какой скоростью каждый сахарный рисунок позволяет антителам захватываться клетками, несущими маннозный рецептор. Они пометили разные фракции антител флуоресцентной меткой и инкубировали их с человеческими клетками, генетически модифицированными для экспрессии этого рецептора. В течение почти трёх дней они отслеживали свечение внутри клеток как меру поглощения. Все антитела в той или иной степени захватывались, но скорости различались: антитела с двумя высокоманнозными гликанами интернализовались быстрее всего, с одним — промежуточно, а с только сложными гликанами — медленнее всего. Когда команда добавляла маннан — природный сахар, конкурирующий за маннозный рецептор — поглощение высокоманнозных антител резко снижалось, что подтвердило, что именно этот рецептор ответственен за большую часть быстрого захвата.
Слежение за «сахарными» антителами в живых животных
Ключевой проверкой было то, перейдут ли эти клеточные различия в реальное поведение препарата. Учёные сформулировали продукт, богатый как симметричными, так и асимметричными высокоманнозными парами, а также парами только со сложными гликанами, и ввели его крысам. С помощью чувствительных методов масс-спектрометрии они могли отслеживать не только общий уровень антител в течение двух недель, но и то, как каждая пара гликанов снижалась со временем. Картина оказалась впечатляющей: антитела с двумя высокоманнозными гликанами исчезали быстрее всего — с периодом полувыведения примерно 2,4 дня; антитела с одним высокоманнозным гликаном жили дольше — около 7,2 дня; а антитела только со сложными гликанами сохранялись примерно 17,4 дня. Площадь под кривой концентрации со временем упала до 38% для двойной высокоманнозной пары и до 73% для смешанной пары по сравнению с парой только со сложными гликанами. По сути, каждая дополнительная высокоманнозная цепочка действовала как ещё один флаг «убери меня» для маннозного рецептора.
Что это значит для более безопасных и долговечных лекарств
Для пациентов эти результаты проясняют, почему два препарата-антитела, которые на бумаге выглядят похожими, могут вести себя по-разному в организме. Исследование показывает, что важна не только наличие, но и парность высокоманнозных гликанов: она сильно определяет скорость выведения антител, вероятно через захват маннозным рецептором и последующий распад в иммунных клетках. Поскольку тот же путь может также доставлять антигены в цепочку событий, запускающую иммунный ответ, эти сахарные узоры могут влиять на риск формирования антител против лекарства и аллергических реакций. Авторы утверждают, что производителям следует контролировать и управлять парностью гликанов — а не только общей сахарной композицией — при разработке и тестировании антительных терапий. Это может помочь обеспечить более предсказуемые режимы дозирования, более длительный эффект и меньшую вероятность нежелательных иммунных реакций.
Цитирование: Baumeister, J., Meudt, M., Wei, W. et al. Selective clearance of monoclonal antibodies via the mannose receptor is dependent on glycan pairing. Sci Rep 16, 8489 (2026). https://doi.org/10.1038/s41598-026-40268-1
Ключевые слова: моноклональные антитела, гликозилирование, маннозный рецептор, фармакокинетика, иммуногенность