Clear Sky Science · ru
Молекулярная эволюция и разнообразие РНК-зависимой РНК-полимеразы норовируса
Почему кишечные инфекции постоянно нас удивляют
Норовирус — печально известный «желудочный грипп», который способен за считанные дни парализовать круизные лайнеры, школы и больницы. Он легко распространяется, ежегодно заражает сотни миллионов людей и постоянно порождает новые варианты. В этом исследовании авторы заглядывают под капот этой эволюции, сосредоточив внимание на одном ферменте вируса — внутренней «копировальной машине», называемой РНК-полимеразой, чтобы понять, как она меняется со временем и насколько стабильна на самом деле. Понимание этого скрытого двигателя изменений может помочь объяснить, почему некоторые штаммы норовируса доминируют в мире, и направить разработку будущих противовирусных препаратов.
Внутренняя копировальная машина вируса
Норовирус хранит свой генетический материал в виде РНК и полагается на фермент РНК-зависимую РНК-полимеразу для копирования этой РНК внутри инфицированных клеток. Этот фермент длиной примерно 510 аминокислот напоминает свернутую руку с «пальцами», «ладонью» и «большим пальцем», образующими канал, через который проходят матрица РНК и новые мономеры. В этой структуре расположены семь небольших «горячих точек», почти идентичных у разных штаммов; эти участки выполняют основную химию копирования генома. Поскольку полимераза необходима для размножения вируса, даже небольшие нарушения в этих горячих точках могут быть катастрофическими для вируса, поэтому эволюция очень строго их сохраняет.
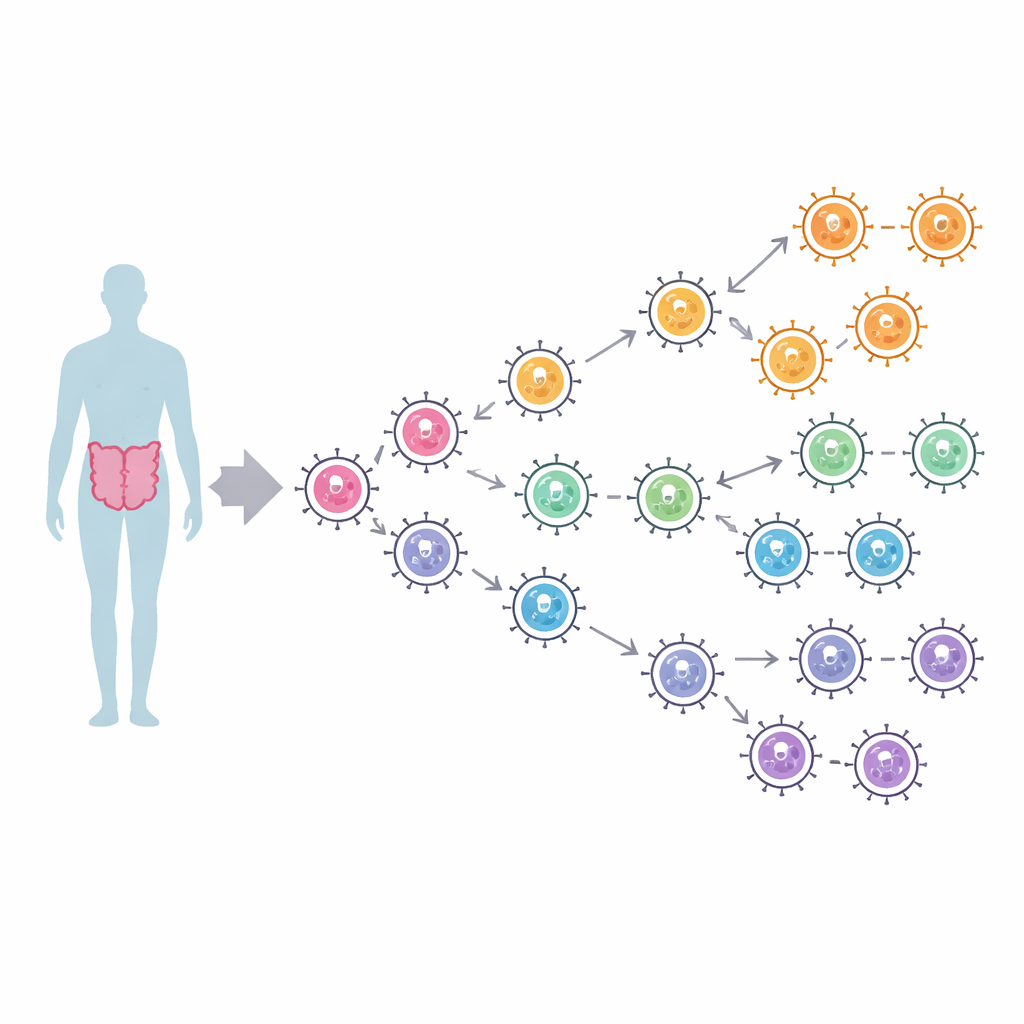
Сотни штаммов, несколько ключевых семей
Исследователи собрали 1 094 полных последовательности полимеразы из двух основных групп человеческого норовируса, обозначаемых GI и GII, собранных по всему миру в период с 1972 по 2024 год. Используя вычислительные филогенетические деревья, учитывающие даты и места отбора, они проследили, как эти ферменты разветвлялись на протяжении почти четырёх столетий. Полимеразы GI образовали три основные линии, чьё расхождение, вероятно, началось примерно в XVII веке, тогда как полимеразы GII сформировали четыре линии, включая отдельную ветвь для типа, известного как P16. Современные инфекции доминируют двумя типами полимераз GII — P16 и P31, которые исторически связаны с пандемическим капсидным генотипом GII.4. Несмотря на глобальное распространение, деревья показали слабую географическую кластеризацию — штаммы с разных континентов смешивались, что указывает на то, что норовирус быстро перемещается по миру и не ограничивается отдельными регионами.
Медленные, ровные изменения с тщательно охраняемым ядром
Сопоставляя аминокислоты в каждой позиции полимеразы, команда зафиксировала тысячи изменений между типами. Изменений в GI оказалось существенно меньше, чем в GII, частично из‑за меньшего числа доступных последовательностей, но выявился ясный шаблон: семь консервативных «горячих точек» и соседняя область связывания РНК оставались практически нетронутыми. Когда в этих участках происходили замены, это обычно были мягкие перестановки между химически схожими аминокислотами, что указывает на то, что фермент допускает лишь очень бережные модификации в этих критических зонах. Большинство частых изменений сосредоточивалось в «пальцах» и других внешних областях фермента, вдали от центральной каталитической функции. Некоторые позиции демонстрировали обратимые колебания между вариантами в разных типах полимераз — признак конвергентной эволюции, когда несвязанные штаммы приходят к похожим решениям.
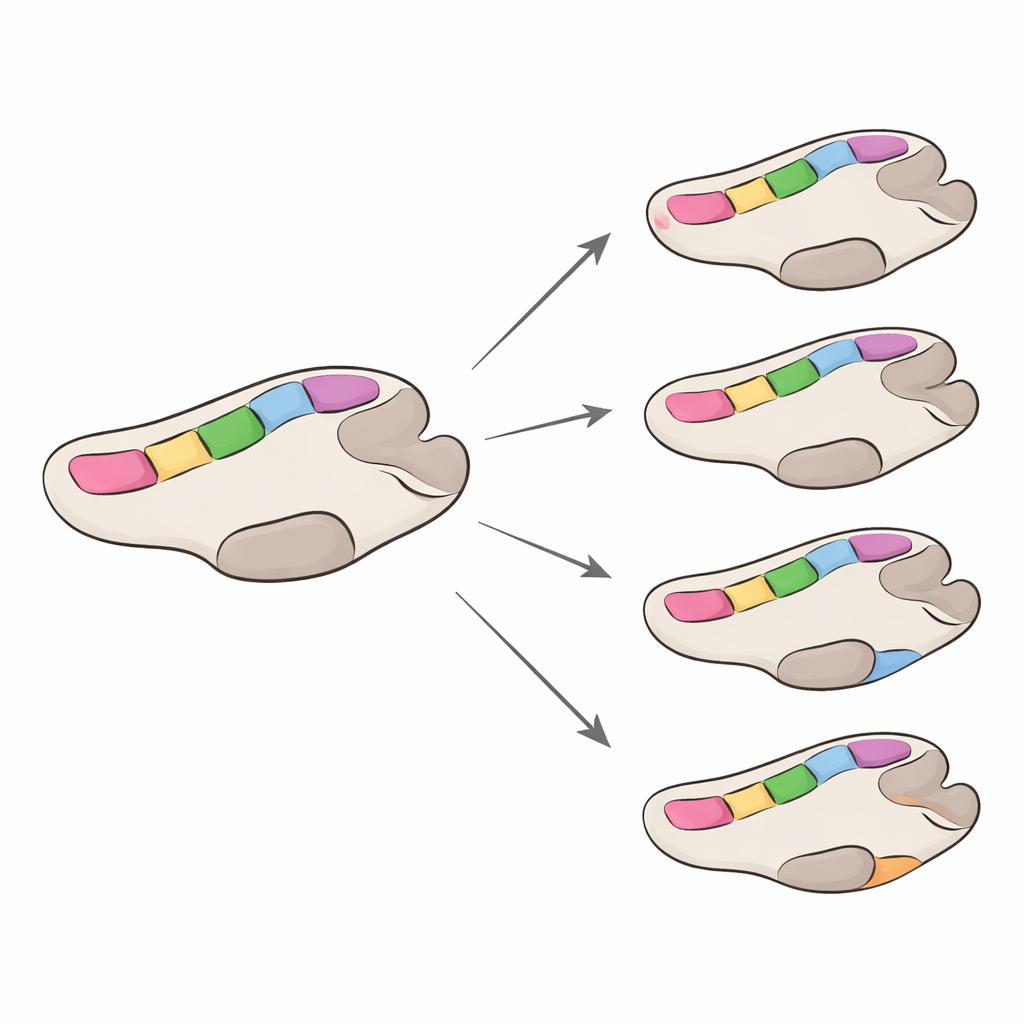
Разные скорости для разных семейств вируса
Далее команда оценивала скорость эволюции полимеразы, сосредоточившись на изменениях, приводящих к замене аминокислот, которые более вероятно влияют на функцию. В целом полимеразы GII изменялись примерно в четыре раза быстрее, чем GI, хотя обе группы эволюционировали медленнее, чем наружный белок оболочки норовируса, известный быстрыми изменениями в ходе ухода от иммунного ответа. Внутри каждой группы некоторые типы полимераз эволюционировали немного быстрее других, но различия были умеренными. Важно, что большая часть позиций в ферменте находилась под сильным «очищающим» отбором — вредные для функции мутации отсеивались, — тогда как лишь несколько сайтов демонстрировали признаки позитивного отбора. При нанесении этих сайтов на трёхмерные модели фермента они почти всегда располагались вне наиболее консервативных горячих точек, хотя некоторые находились достаточно близко, чтобы потенциально тонко регулировать связывание РНК или движения полимеразы во время копирования.
Что это означает для будущих вспышек и лечения
Вместе эти результаты описывают полимеразу норовируса как удивительно стабильное ядро, окружённое более гибкими регионами, позволяющими постепенную адаптацию. Полимеразы GII, особенно связанные с исторически пандемическими штаммами, эволюционируют несколько быстрее, что может помогать этим вирусам поспевать за изменениями хозяев и конкурирующими вариантами. Тем не менее глубокая консервация ключевых функциональных участков на протяжении столетий указывает на то, что этот фермент представляет собой перспективную стабильную мишень для противовирусных препаратов: нарушив основную машину копирования, вирус вряд ли сможет уйти от воздействия, не лишив себя жизнеспособности. Для неспециалистов основной вывод таков: внешние поверхности норовируса могут продолжать меняться, делая новые вспышки неизбежными, но внутренняя «машина», приводящая эти изменения в движение, строго ограничена и научно доступна — она предлагает стабильную прицельную точку для будущих терапий.
Цитирование: Flint, A., Jawad, M. & Nasheri, N. Molecular evolution and diversity of the norovirus RNA-dependent RNA polymerase. Sci Rep 16, 9042 (2026). https://doi.org/10.1038/s41598-026-40248-5
Ключевые слова: норовирус, вирусная эволюция, РНК-полимераза, противовирусные мишени, молекулярная эпидемиология