Clear Sky Science · ru
Мультимодальная характеристика инициирования и роста тромба, вызванного потоком, в оксигенаторах вне тела (ECMO)
Почему тромбы в аппаратах жизнеобеспечения имеют значение
Экстракорпоральная мембранная оксигенация, или ECMO, — это форма обхода сердца и лёгких, которая может поддерживать жизнь критически больных пациентов, пока их органы восстанавливаются. Но прогон крови через насосы и пластиковые трубки подвергает её суровым механическим нагрузкам, с которыми организм не рассчитан справляться. Эти силы могут запустить образование опасных тромбов внутри контура, что повышает риск инсульта, повреждения органов или отказа аппарата. В этом исследовании ставилась задача выяснить, как именно поток крови через насос ECMO формирует возникновение и рост таких тромбов, с долгосрочной целью сделать ECMO более безопасным и эффективным.
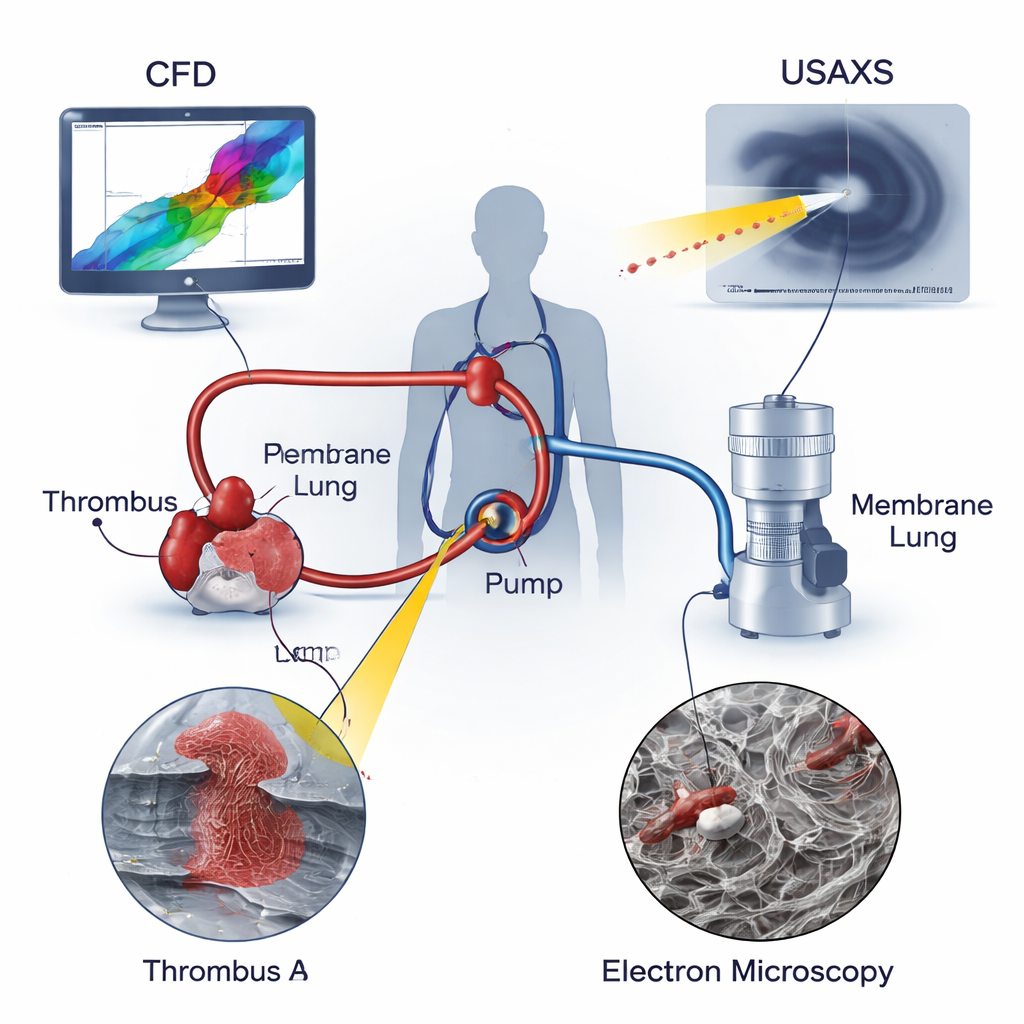
Как ECMO поддерживает пациентов
При ECMO кровь забирают из большой вены или артерии, продвигают центробежным насосом через «мембранное лёгкое», которое насыщает её кислородом и удаляет углекислый газ, а затем возвращают пациенту. В отличие от плавного потока по естественным сосудам, в контуре ECMO возникают экстремальные условия: очень быстрые струи, резкие изменения направления и почти застойные зоны, где кровь задерживается. Известно, что такие среды повреждают клетки крови и стимулируют тромбообразование. Классические медицинские модели сосредоточены на медленном или застойном кровотоке в сосудах, но они не полностью учитывают интенсивное сдвиговое и растягивающее воздействие, которое испытывает кровь внутри вращающегося насоса. Авторы утверждают, что для полноценного понимания риска тромбообразования в ECMO нужно изучать и механические силы в устройстве, и микроскопическую структуру образующихся тромбов.
Изучение тромбов с трёх сторон
Исследователи объединили три мощных метода для анализа двух реальных тромбов, извлечённых из контуров ECMO, применённых у детей: один тромб у входа в насос (Тромб A) и другой в трубке сразу за насосом (Тромб B). Численное моделирование гидродинамики (CFD) имитировало движение крови через насос, выявляя области рециркуляции и завихрения потока и указывая, где достигаются пиковые значения сдвиговых и растягивающих сил. Ультра-малоугловое рентгеновское рассеяние (USAXS) проникало глубоко в каждый тромб, измеряя степень уплотнения и направленной упорядоченности фибриновой «опоры» — белковой сети, держащей тромб вместе — по всему образцу. Сканирующая электронная микроскопия (SEM) давала сильно увеличенные изображения поверхности тромба, показывая формы эритроцитов, лейкоцитов, тромбоцитов и окружающих фибриновых волокон. Наложив эти три вида данных, команда смогла соотнести локальные условия потока с внутренней архитектурой каждого тромба.
Зона рециркуляции формирует жёсткий, выровненный тромб
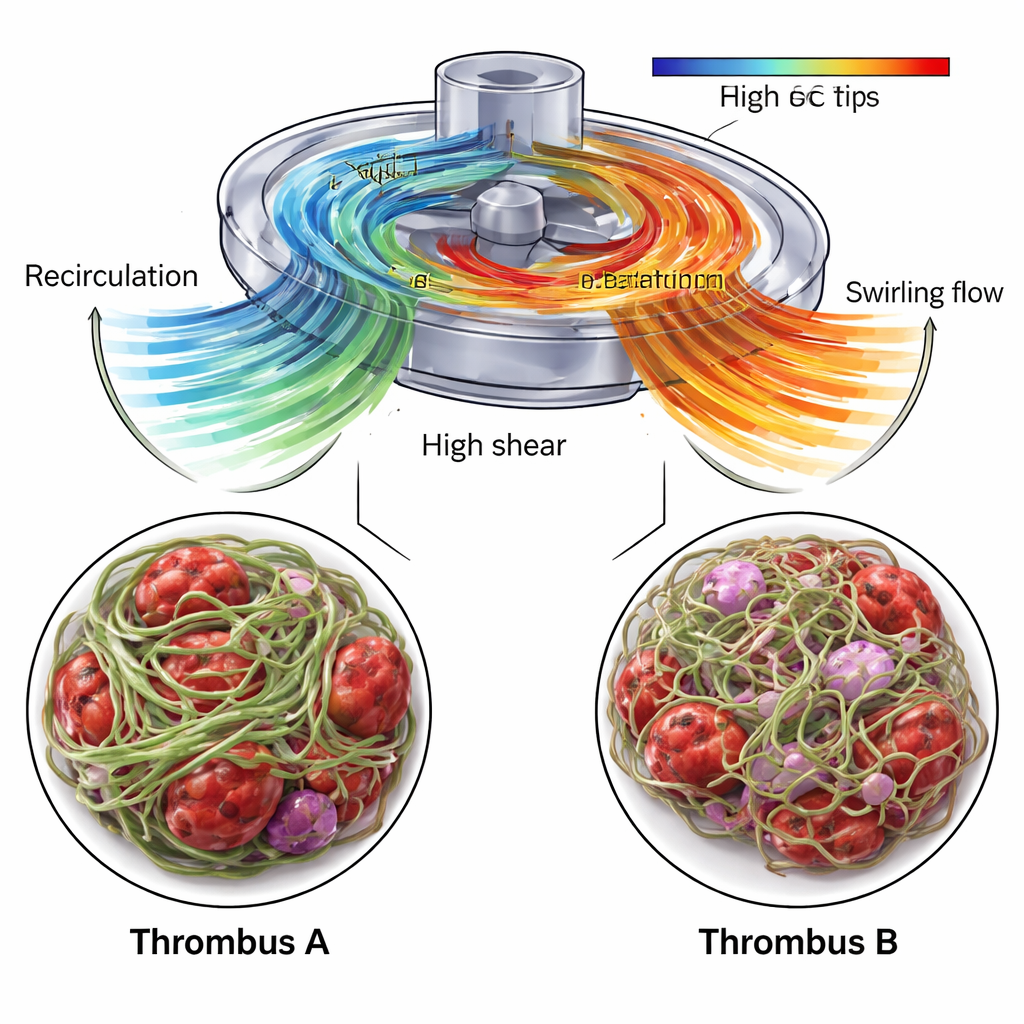
CFD показало, что участок у входа в насос, где образовался Тромб A, содержал зону рециркуляции: кровь отталкивалась назад и вверх вдоль корпуса перед тем, как вновь попасть в основной поток. Эта область позволяла компонентам крови задерживаться, одновременно испытывая резкие различия скоростей на границе между рециркулирующим и входящим потоком. Внутри Тромба A USAXS указало на высокий вклад фибрина — по крайней мере 70 процентов — и сильную общую выровненность волокон в предпочтительном направлении, что свидетельствует о плотной, жёсткой каркасе. SEM-изображения подтвердили плотно сплетённую сеть фибрина, перемежающуюся аномально деформированными эритроцитами и фрагментами тромбоцитов. Авторы предполагают, что сочетание длительного времени пребывания и сильного локального сдвига способствовало росту компактного, высокоорганизованного тромба, способного выдерживать механические нагрузки насоса.
Завихренный отток формирует более рыхлый, скрученный тромб
Напротив, Тромб B, взятый из трубки после насоса, развивался в области, где доминировал завихренный отток. CFD выявило вращающиеся, спиралевидные структуры потока, выходящие из сопла насоса, а данные USAXS показали, что фибриновая сеть по-прежнему доминирует, но менее плотная и в целом менее сильно выровнена. Основное направление ориентации фибрина постепенно смещалось по всему тромбу, от одного угла наклона к другому, отражая скручивающий паттерн потока. SEM-изображения продемонстрировали нити фибрина различной толщины и многочисленные захваченные клетки крови и иммунные клетки, включая признаки повреждения и воспаления. Важно, что моделирование также выявило небольшие, но значимые участки объёма насоса, где растягивающие силы были достаточны для разворачивания фактора фон Виллебранда — ключевого плазменного белка, который становится «липким» под нагрузкой и может быстро привлекать тромбоциты. Эти зоны концентрировались вблизи лопастей рабочего колеса и выхода, что делает их вероятными местами начальной активации, приведшей к образованию Тромба B.
К более безопасным аппаратам жизнеобеспечения
Объединив детальные симуляции кровотока с рентгеновскими и электронно-микроскопическими измерениями реальных тромбов из ECMO, это исследование показывает, что внутренняя «структура» и плотность тромба отражают механическую среду, в которой он формировался. Рециркулирующий поток у входа в насос связывали с плотным, сильно выровненным фибриновым каркасом, тогда как завихренный отток ассоциировался с более скрученным, открытым сетчатым образованием, которое всё ещё захватывало множество клеток крови и иммунных клеток. Эти выводы указывают на конкретные участки в насосах и трубках ECMO, где изменение конструкции или целенаправленная корректировка антикоагуляции могли бы наиболее эффективно снизить риск тромбообразования. В долгосрочной перспективе такая многомасштабная карта — от геометрии насоса и паттернов потока до расположения белков — может направлять разработку более безопасных устройств и помогать клиницистам лучше балансировать двойную угрозу кровотечения и тромбоза во время спасительной поддержки ECMO.
Цитирование: Nilsson, F., Sochor, B., Henriksson, S. et al. Multimodal characterization of flow-induced thrombus initiation and growth in extracorporeal membrane oxygenation. Sci Rep 16, 7166 (2026). https://doi.org/10.1038/s41598-026-40177-3
Ключевые слова: ECMO, свертывание крови, касательные напряжения, центробежный насос для крови, структура фибрина