Clear Sky Science · ru
Интеграция транскриптомных данных с помощью машинного обучения выявляет GFM1 как кандидатный биомаркер, связанный с лактиляцией, при расслаивающей аневризме аорты
Почему эта скрытая угроза в аорте имеет значение
Расслаивающая аневризма аорты — это неотложное состояние, при котором разрыв во внутренней оболочке главной артерии может привести к угрожающему жизни внутреннему кровотечению в течение нескольких часов. Врачи часто спасают пациентов с помощью экстренной операции, но до сих пор отсутствуют надёжные анализы крови, которые бы предупреждали о риске на ранней стадии, и лекарства, замедляющие само заболевание. В этом исследовании изучают, могут ли тонкие изменения в том, как клеткам сосудов удаётся управлять энергией и химическими сигналами, дать новые ранние признаки опасности, сосредоточив внимание на малоизвестном гене GFM1, который может связывать клеточный метаболизм с ослаблением стенки аорты.
Расшифровывая механизм опасного разрыва
При расслаивающей аневризме кровь проникает в стенку аорты, расслаивая её слои. Почему у некоторых людей аорта разрушается таким образом, пока полностью не выяснено. Авторы проанализировали образцы с активностью генов у пациентов с расслаиванием аорты и у лиц с нормальной аортой. Особое внимание они уделили генам, связанным с «лактилированием» — недавно открытым механизмом, при котором клетки используют лактат (вещество, накапливающееся в мышцах при интенсивной нагрузке) для тонкой настройки белков и регуляции генов. Поскольку лактилирование связано с воспалением и ремоделированием тканей, исследователи предположили, что гены, связанные с лактатом, также могут участвовать в повреждении стенки аорты.
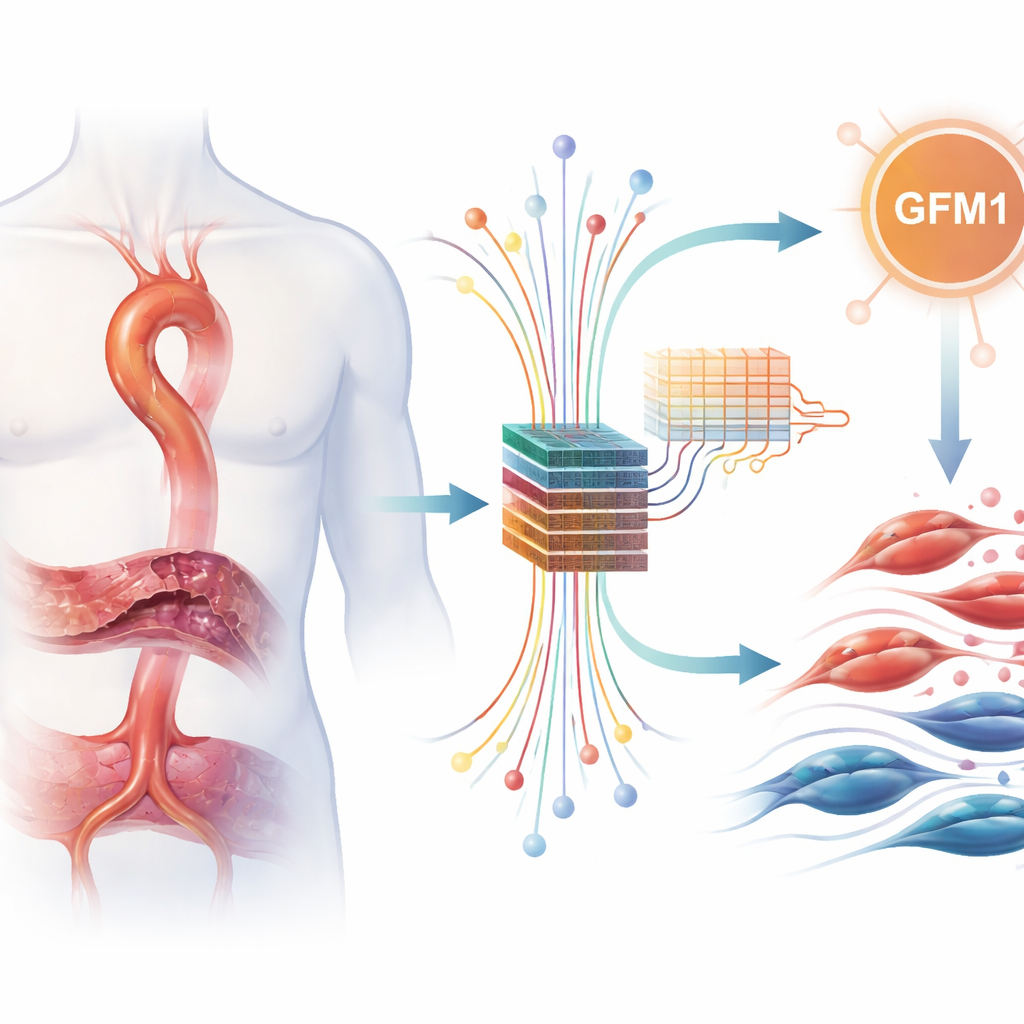
Добыча больших данных с помощью умных алгоритмов
Чтобы проверить эту гипотезу, исследователи объединили несколько общедоступных наборов данных, отражающих, какие гены включены или выключены в аортной ткани. Они тщательно скорректировали технические различия между исследованиями и затем искали гены, чья активность последовательно отличалась между больными и здоровыми образцами. Из тысяч генов они выделили 217 с явными изменениями, многие из которых указывали на иммунные реакции и ремоделирование внеклеточного каркаса, поддерживающего аорту. Дальше они сосредоточились на курируемом списке генов, связанных с обращением лактата и лактилированием, и выявили 11 генов, одновременно изменённых при расслаивании аорты и входящих в эти лактат-связанные программы.
Пусть машины проголосуют за ключевого подозреваемого
11 интересных генов всё ещё слишком много для глубокого лабораторного изучения, поэтому команда использовала методы машинного обучения как объективную «систему голосования». Они подали данные по этим генам в три модели — LASSO, Random Forest и XGBoost — которые широко применяются для выделения паттернов, лучше всего разделяющих пациентов и контрольные образцы. Каждая методика выделила свои фавориты, но только один ген, GFM1, был сильно и последовательно выбран всеми тремя моделями. Такой перекрёстный контроль вывел GFM1 как особенно надёжного кандидата, хотя модели использовались для ранжирования, а не для создания готового диагностического теста.
Прицел на мышечные клетки артерии
GFM1 участвует в контроле того, как митохондрии — энергетические «фабрики» клетки — синтезируют свои собственные белки. Поскольку энергетический баланс критичен для поведения клеток стенки артерии, авторы изучили GFM1 подробнее. Они подтвердили, что уровни GFM1 выше в тканях пациентов с расслаиванием аорты, чем в ненарушенной аорте. Затем они перешли к контролируемым культурам клеток, используя гладкомышечные клетки сосудов мыши — клетки, придающие аорте прочность. При стимуляции этих клеток ангиотензином II, гормоном, связанным с повышенным давлением и стрессом сосудов, клетки стали более склонны к пролиферации и миграции, имитируя вредные изменения, наблюдаемые в болезненных артериях. Когда исследователи подавляли GFM1 с помощью малых интерферирующих РНК, рост и миграция, вызванные ангиотензином, заметно снижались, что указывает на то, что GFM1 способствует этим рискованным поведением клеток.
Что это означает и чего это ещё не доказывает
В сумме результаты указывают на то, что GFM1 может выступать мостом между изменённым клеточным метаболизмом и агрессивным поведением клеток стенки аорты при расслаивающей аневризме. Проще говоря, повышенная активность GFM1 коррелирует с более нестабильной, склонной к повреждениям аортой, а снижение его уровня в культурах делает клетки менее склонными к чрезмерному росту и миграции. Однако авторы осторожно подчеркивают, что это исследование находится на ранней, генерирующей гипотезы стадии. Они не измеряли непосредственно лактилирование в тканях и не доказали, что сам GFM1 подвергается такой химической модификации, а прогностические способности моделей не проверялись на независимых когортах пациентов. Будущие исследования должны подтвердить результаты в больших группах и выяснить, как именно GFM1 и связанные с ним метаболические изменения ослабляют стенку аорты. Если эти усилия увенчаются успехом, GFM1 или связанные с ним пути могут в перспективе стать мишенью для новых анализов крови или терапий, направленных на предотвращение данного часто смертельного разрыва до его наступления.
Цитирование: Chen, J., Jiang, N., Guo, Z. et al. Machine-learning–guided transcriptomic integration identifies GFM1 as a lactylation-related candidate biomarker in aortic dissection. Sci Rep 16, 9033 (2026). https://doi.org/10.1038/s41598-026-40139-9
Ключевые слова: расслаивающая аневризма аорты, гладкомышечные клетки сосудов, метаболизм лактата, функция митохондрий, поиск биомаркеров