Clear Sky Science · ru
Динамика актина, опосредованная кальдесмоном‑1, необходима для остеогенной дифференцировки интерстициальных клеток аортального клапана
Почему жесткость сердечного клапана имеет значение
С возрастом один из ключевых ворот сердца — аортальный клапан — может постепенно становиться жестким и твердым как камень. Это состояние, называемое аортальным стенозом, заставляет сердце перекачивать кровь с большими усилиями и может привести к сердечной недостаточности. На сегодняшний день единственные надежные методы лечения — хирургическая или чрескожная замена клапана. В приведенном исследовании обсуждается базовый, но важный вопрос: что заставляет мягкую гибкую ткань клапана постепенно превращаться в подобную кости? Выявив ключевой молекулярный фактор этого процесса, работа указывает путь к будущим лекарствам, которые могли бы замедлить или даже предотвратить кальцификацию клапана, а не только заменить поврежденный клапан.
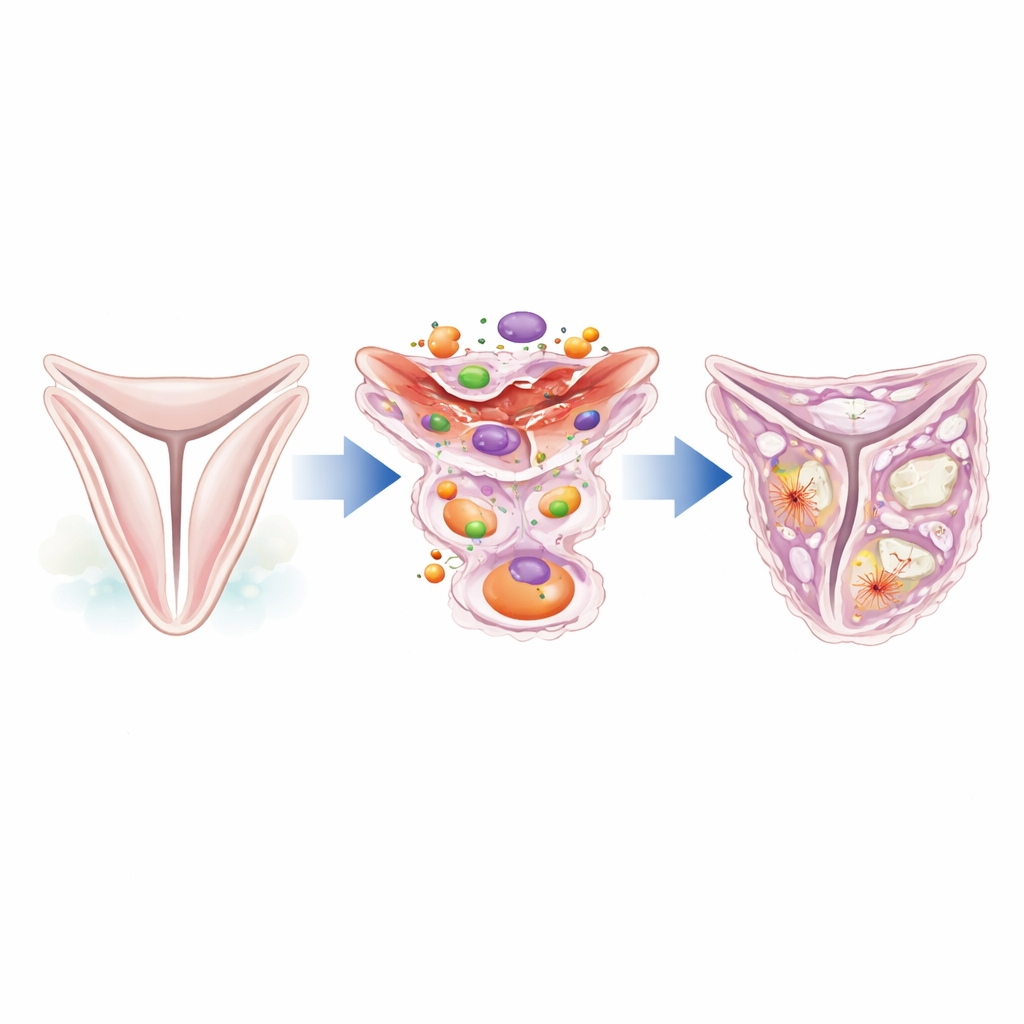
Взгляд на скрытых «работников» клапана
Листки аортального клапана поддерживаются тонким слоем специализированных поддерживающих клеток, известных как интерстициальные клетки клапана. В здоровом клапане эти клетки находятся в спокойном состоянии и помогают поддерживать структуру ткани. Однако при стрессе или повреждении они могут менять свою идентичность и начинать вести себя как клетки, формирующие рубцовую ткань, или даже как клетки, образующие кость. Авторы сосредоточили внимание на белке под названием кальдесмон‑1, который помогает контролировать внутренний каркас клетки, состоящий из актиновых филаментов. Проанализировав имеющиеся данные одиночноклеточного РНК‑секвенирования человеческих клапанов, они обнаружили, что кальдесмон‑1 существенно повышен в клапанах пациентов с аортальным стенозом по сравнению с нормальными клапанами, особенно в интерстициальных клетках, найденных в утолщенных фиброзных областях.
От гибкой ткани к фиброзным и костеподобным участкам
Микроскопические исследования образцов человеческих клапанов показали, что белок кальдесмон‑1 обилен в пораженных створках и коррелирует с маркерами активированных контрактильных клеток и фибробластоподобных клеток, синтезирующих коллаген. Эти богатые кальдесмон‑1 клетки группируются вокруг зон фиброза и ранней кальцификации, что наводит на мысль, что они помогают наращивать внеклеточный матрикс, утолщающий клапан. Дальнейший анализ показал, что эти клетки экспрессируют гены, типичные для клеток, похожих на гладкомышечные, и склонных к остеогенезу типов, и являются основными производителями структурных белков, таких как коллаген I типа. Другими словами, где бы ни происходило уплотнение и рубцевание клапана, интерстициальные клетки, положительные по кальдесмону‑1, присутствуют на месте событий.
Как белок, управляющий формой, подталкивает клетки к остеогенезу
Чтобы установить причинно‑следственную связь, команда выделила человеческие интерстициальные клетки клапана и использовала маленькие интерферирующие РНК для понижения уровня кальдесмона‑1. Без этого белка клетки теряли удлиненную веретенообразную форму и становились более круглыми. Их внутриклеточные актиновые филаменты истончились, а способность делиться и направленно мигрировать снизилась. Когда исследователи подвергали эти клетки остеогенной, стимулирующей образование кости, среде, нормальные клетки легко образовывали кальциевые отложения, тогда как клетки с дефицитом кальдесмона‑1 демонстрировали значительно меньшее накопление минералов. Масштабное РНК‑секвенирование подтвердило, что многие гены, вовлеченные в формирование кости и перестройку ткани, включая хорошо известные остеогенные факторы, такие как RUNX2 и щелочная фосфатаза, сильно активировались при остеогенных условиях, но не увеличивали экспрессию при подавлении кальдесмона‑1.
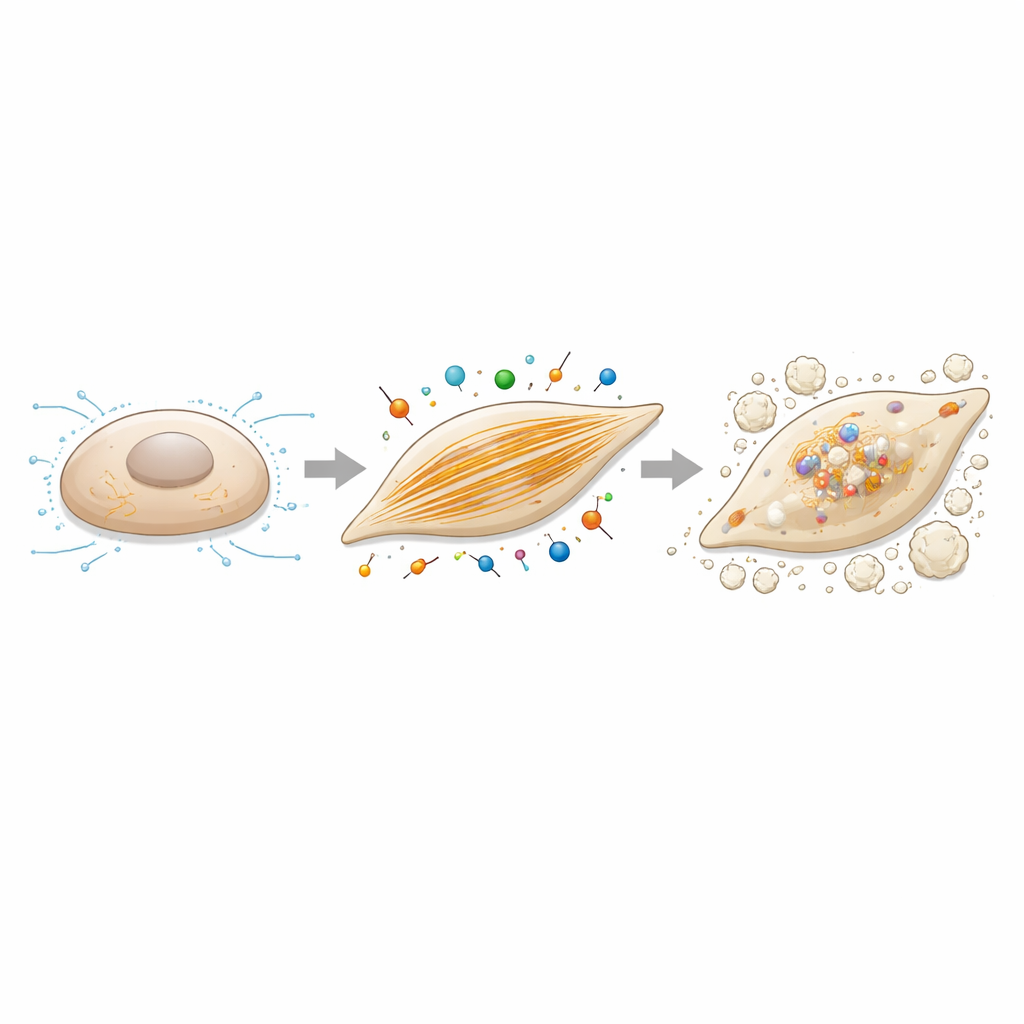
Актиновые филаменты как рычаг контроля кальцификации
Поскольку кальдесмон‑1 регулирует актин, авторы далее спросили, изменит ли само собирательство актина склонность клеток к кальцификации. Они обрабатывали интерстициальные клетки клапана цитохалазирином B, соединением, которое аккуратно нарушает рост актиновых филаментов, при тех же условиях, стимулирующих остеогенез. В дозах, не наносящих серьёзного вреда выживанию клеток, это лечение резко снижало отложение кальция и уменьшало экспрессию генов, связанных с оссификацией, включая кальдесмон‑1 и RUNX2. Вкупе с опытом по снижению экспрессии, эти результаты дают цельную картину: устойчивые сети актиновых филаментов и контрактильные силы, которые они поддерживают, — не просто наблюдатели, а активные драйверы перехода от спокойных поддерживающих клеток к клеткам, образующим кость в клапане.
Что это значит для будущих методов лечения
Для неспециалиста главный вывод в том, что уплотнение аортального клапана — это активный, регулируемый процесс, а не простое «изнашивание». Это исследование выделяет кальдесмон‑1 как центральный координатор, связывающий внутренний скелет клетки с генетической программой по созданию костеподобной ткани. Содействуя тому, что интерстициальные клетки клапана принимают контрактильную, фибротическую и в конечном счете остеогенную идентичность, кальдесмон‑1 прямо способствует накоплению твердых отложений, сужающих клапан. Несмотря на то, что любая терапия, нацеленная на этот белок или динамику актина, потребует тщательной проверки, чтобы избежать нежелательных эффектов в других тканях, пути, опосредованные кальдесмон‑1, теперь выделяются как перспективные кандидаты для разработки препаратов, призванных замедлить или остановить кальцификацию клапана до необходимости хирургического вмешательства.
Цитирование: Komoda, M., Sakaue, T., Nakao, Y. et al. Caldesmon-1–mediated actin dynamics is essential for osteogenic differentiation of aortic valve interstitial cells. Sci Rep 16, 9385 (2026). https://doi.org/10.1038/s41598-026-39938-x
Ключевые слова: кальцификация аортального клапана, кальдесмон‑1, интерстициальные клетки клапана, цитоскелет актина, остеогенная дифференцировка