Clear Sky Science · ru
RBP4 мешает прогрессированию плоскоклеточного рака языка, подавляя сигнальный путь PI3K/AKT и стимулируя поляризацию макрофагов в тип M1
Почему для рака языка нужны новые подходы
Рак языка может лишить человека способности говорить, есть и чувствовать вкус; даже при хирургическом удалении, химио‑ и радиотерапии долгосрочная выживаемость часто оставляет желать лучшего. В этом исследовании изучается неожиданный помощник в нашей крови — белок, переносящий витамин A, называемый RBP4, — и показано, как он одновременно может замедлять рост опухолей языка и мобилизовать собственную иммунную систему организма. Раскрывая, как эта молекула действует внутри раковых клеток и в окружающих иммунных клетках, работа указывает на новые стратегии, которые в перспективе могут сделать лечение более эффективным и менее разрушительным.
Скрытый белок в опухолях языка
Исследователи начали с анализа больших онкологических генетических баз данных, чтобы выяснить, какие иммуноопосредованные гены могут предсказывать исход у пациентов с плоскоклеточным раком языка. Среди сотен кандидатов особенно выделился RBP4 — белок, наиболее известный как переносчик витамина A в крови. При сравнении образцов опухоли с соседней здоровой тканью языка выяснилось, что уровень RBP4 в раке постоянно значительно ниже. Этот паттерн был подтверждён в нескольких независимых наборах данных и в тканях от 20 пациентов, что указывает на то, что потеря RBP4 — распространённая черта этого заболевания.
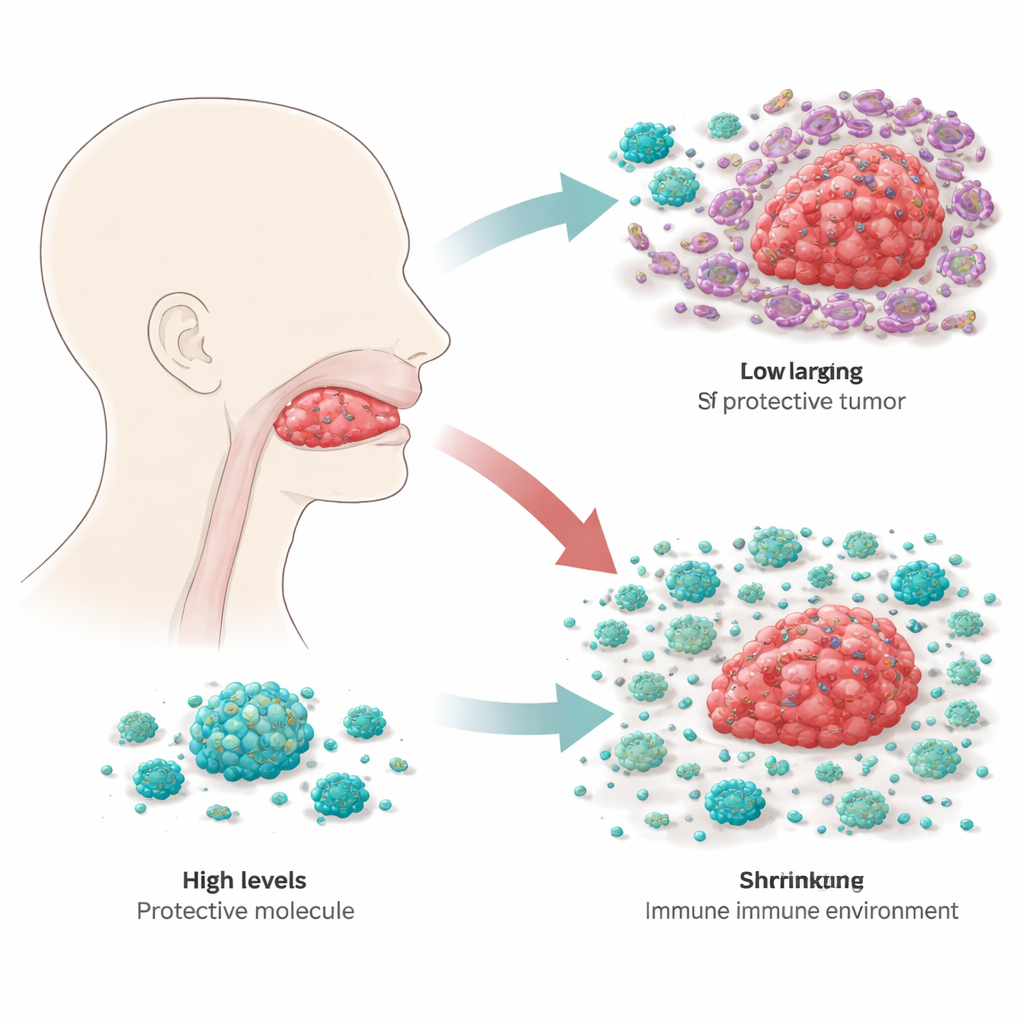
Замедление роста опухоли изнутри
Чтобы узнать, что именно делает RBP4 в раковых клетках языка, учёные создали линии опухолевых клеток, которые либо продуцируют дополнительный RBP4, либо значительно уменьшают его синтез. В культуре клетки с повышенным RBP4 росли медленнее, тогда как клетки с пониженным RBP4 делились быстрее и лучше мигрировали и инвазировали через искусственные мембраны — поведение, связанное с распространением и рецидивом. После имплантации таких модифицированных клеток мышам опухоли с повышенным RBP4 оставались меньшими, в то время как опухоли с пониженным RBP4 росли более агрессивно. Отслеживая ключевые регуляторы роста внутри клеток, команда показала, что RBP4 подавляет главный сигнальный путь роста PI3K–AKT–mTOR, на который многие раки полагаются как на «газ». При высоком уровне RBP4 этот путь работает тише, и раковые клетки менее способны переходить в подвижное, гибкое состояние, которое помогает им мигрировать.
Преобразование иммунных клеток в борцов с опухолью
Опухоль не растёт в изоляции; она существует в окружающей среде иммунных клеток, сосудов и поддерживающих клеток, называемой микроокружением опухоли. Здесь макрофаги — крупные иммунные клетки, которые могут либо атаковать, либо поддерживать опухоль — играют центральную роль. Исследователи заметили, что в опухолях с большим количеством RBP4 чаще встречается тип макрофагов «M1», ассоциированный с воспалением и уничтожением опухолей, а не «M2», который часто способствует росту опухоли. В культурах клеток при экспозиции макрофагов либо очищенным RBP4, либо раковыми клетками языка, запрограммированными на повышенную секрецию RBP4, макрофаги сдвигались в сторону M1, то есть в состояние, направленное против опухоли. Когда RBP4 был снижен в раковых клетках, макрофаги, наоборот, склонялись к более «дружелюбному» для опухоли профилю.
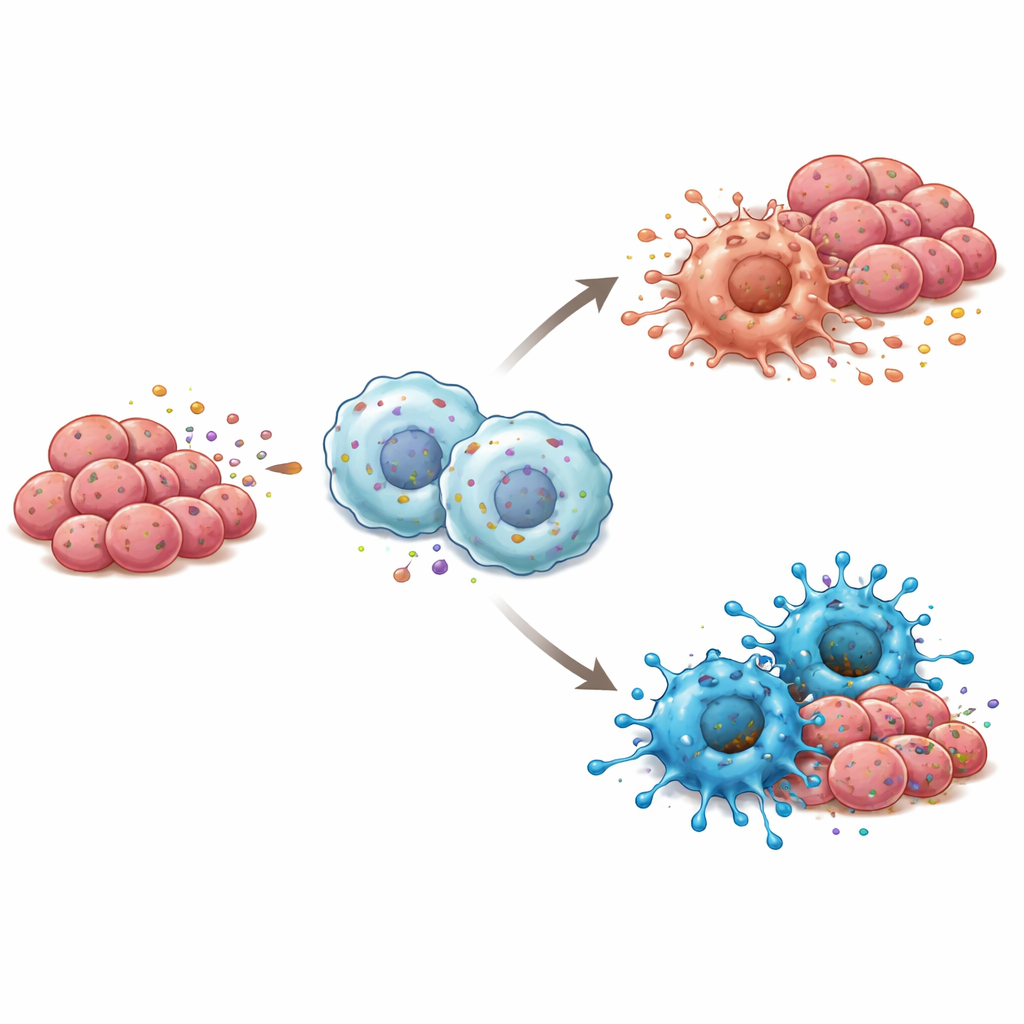
Сигнальные пути, лежащие в основе иммуно‑сдвига
Чтобы понять, как RBP4 подталкивает макрофаги к более враждебному отношению к опухоли, исследователи изучали, какие внутриклеточные «сигнализации» включаются в этих иммунных клетках. Они обнаружили, что RBP4 стимулирует сенсор TLR4 на поверхности макрофага и, в свою очередь, активирует NF-κB — мастер‑переключатель, запускающий воспалительные ответы. Блокирование TLR4 химическим ингибитором прерывало эту цепочку и мешало макрофагам принимать состояние M1, даже в присутствии RBP4. В экспериментах на мышах опухоли, сформированные из клеток языка с высоким RBP4 и смешанные с макрофагами, росли медленнее и содержали больше M1‑макрофагов, а также демонстрировали усиленную активность TLR4 и NF-κB, что подтверждает ключевую роль этого пути в иммунных эффектах RBP4.
Что это может означать для будущего лечения
В целом работа рисует RBP4 как двойной «тормоз» для рака языка: внутри опухолевых клеток он ослабляет гиперактивный контур роста, а в микроокружении опухоли способствует превращению макрофагов в более бдительных защитников. Хотя остаётся много вопросов — например, каким именно образом RBP4 взаимодействует со своими мишенями и как лучше повысить его уровень безопасно — исследование предполагает, что восстановление или имитация действий RBP4 может одновременно замедлить рост опухоли и усилить собственное иммунное давление организма на рак. Для пациентов это открывает перспективу будущих терапий, которые не только удаляют опухоль, но и перенастраивают её внутреннюю «проводку» и местную «экосистему», чтобы предотвратить рецидив.
Цитирование: Yan, Y., Miao, N. & Wang, X. RBP4 interferes with tongue squamous cell carcinoma progression by inhibiting the PI3K/AKT signaling pathway and promoting macrophage M1-type polarization. Sci Rep 16, 9375 (2026). https://doi.org/10.1038/s41598-026-39915-4
Ключевые слова: рак языка, RBP4, микроокружение опухоли, макрофаги, путь PI3K AKT