Clear Sky Science · ru
Мультиомное выявление ключевых мишеней остеогенной дифференцировки костного мозга человека при окислительном стрессе
Почему важны «стрессовые» кости
С возрастом или при хронических заболеваниях, таких как диабет и остеопороз, наши кости теряют способность к самовосстановлению. Главный виновник — «окислительный стресс» — накопление реактивных молекул, повреждающих клетки. В этом исследовании ставится практический вопрос с большими последствиями для лечения переломов и имплантов: что именно идет не так внутри человеческих стволовых клеток костного мозга при воздействии окислительного стресса и можно ли найти молекулярный переключатель, который поможет им продолжать формировать новую кость?
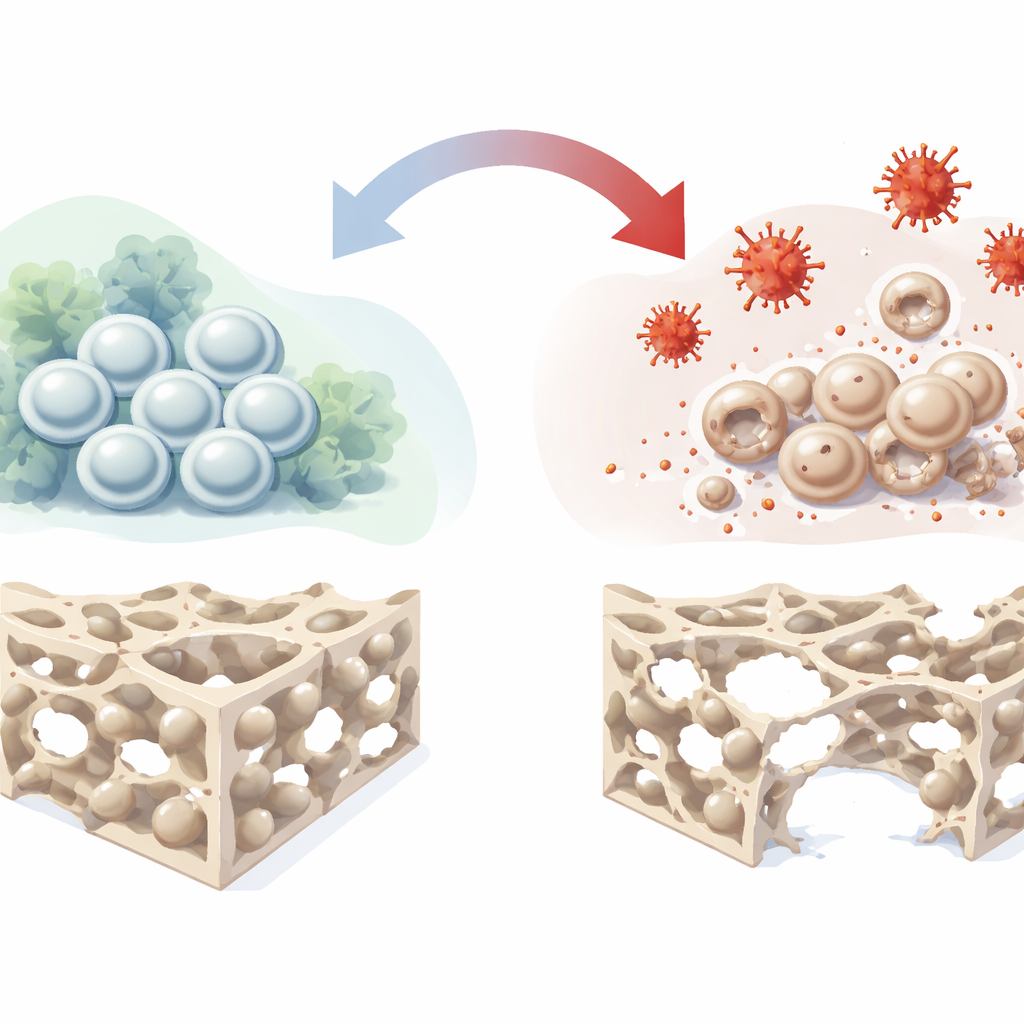
Стволовые клетки, строящие кость
Глубоко внутри наших костей находятся мезенхимальные стромальные клетки костного мозга — разносторонняя популяция, способная самоподновляться и превращаться в остеобласты (клетки, формирующие кость), хондроциты и адипоциты. Поскольку эти клетки естественным образом участвуют в заживлении повреждений, их рассматривают как перспективный инструмент для лечения дефектов кости и остеонекроза. Однако в реальных клинических условиях эти клетки часто оказываются в враждебной среде с плохим кровоснабжением, низким уровнем кислорода, воспалением и окислительным стрессом. В таких условиях их способность превращаться в клетки кости снижается, что ограничивает успех клеточных терапий. Авторы поставили цель воспроизвести эту враждебную среду в лаборатории и подробно проследить, как она нарушает остеогенез.
Воссоздание жестких условий в лаборатории
Исследователи использовали перекись водорода, распространенный источник реактивных кислородных форм, чтобы вызвать окислительный стресс в культурах стволовых клеток костного мозга человека. Они тщательно подбирали дозу, чтобы найти оптимум, при котором клетки испытывали стресс, но не погибали. При концентрациях до 400 микромоляр клетки сохраняли нормальную веретенообразную форму и оставались жизнеспособными, хотя их внутренняя биохимия явно менялась: возрастало содержание реактивных кислородных форм, функционирование митохондрий начинало меняться, а баланс белков, связанных с выживанием и апоптозом, сдвигался в сторону адаптации к стрессу. При более высоких дозах клетки теряли форму и массово погибали. Используя переносимую дозу 400 микромоляр, команда затем индуцировала остеогенез и наблюдала дальнейшие изменения.
Как стресс блокирует построение кости
При окислительном стрессе способность стволовых клеток к остеогенезу снижалась по ряду взаимодополняющих показателей. Ранняя остеогенная активность, отслеживаемая по щелочной фосфатазе, падала с увеличением уровня стресса. На поздних этапах, когда клетки должны были откладывать минеральную матрицу, на культуральных чашках наблюдалось меньше и менее интенсивных кальциевых узелков. Ключевые гены и белки, связанные с образованием кости, такие как RUNX2 и остеопонтин, также оказались понижены. Чтобы заглянуть «под капот», учёные объединили два мощных омных подхода: секвенирование РНК для профилирования активности генов и масштабный анализ белков, чтобы увидеть изменения в их количестве. Совместно эти наборы данных выявили сотни сдвигов в контроле клеточного цикла, поведении хромосом, метаболизме и организации внеклеточного каркаса, рисуя картину стволовых клеток, у которых внутренние таймеры и структурная поддержка нарушены под воздействием окислительного стресса.
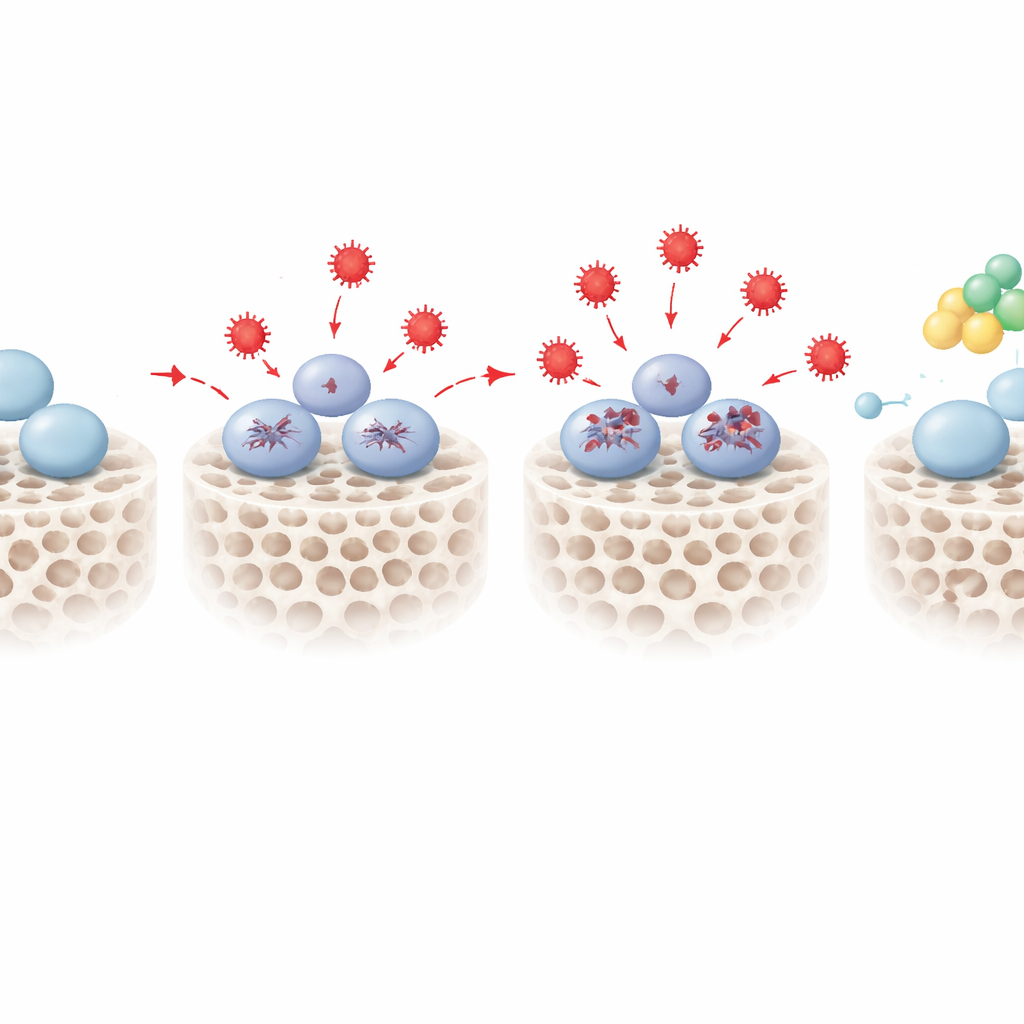
Нахождение защитного переключателя PENK
Наложив данные РНК и протеома, команда сузила круг до 18 молекул, которые последовательно изменялись в стрессовых условиях и были связаны как со стресс-ответом, так и с образованием кости. Особо выделялся проэнкефалин, или PENK, известный прежде всего как предшественник эндогенных опиоидных пептидов. При окислительном стрессе уровень PENK возрастал в зависимости от дозы. Когда исследователи искусственно снижали экспрессию PENK с помощью генетических инструментов, стрессовые стволовые клетки ещё сильнее утратили способность формировать кость: отмечалось ослабление ранней ферментативной активности и меньшее откладывание минералов. При повышении уровня PENK наблюдался обратный эффект: даже в тех же условиях окислительного стресса клетки частично восстанавливали способность строить минерализованную костную матрицу. Дополнительный анализ путей свидетельствовал, что PENK может действовать, настраивая определенные метаболические маршруты, включая метаболизм сфинголипидов, которые связывают редокс‑баланс с решением клетки сохранить потенциал или дифференцироваться в остеогенный путь.
Что это значит для будущего восстановления кости
Это исследование показывает, что один лишь окислительный стресс способен серьёзно подорвать остеогенную способность стволовых клеток костного мозга человека, и идентифицирует PENK как встроенный защитный фактор, помогающий им противостоять этому повреждению. Для неспециалистов вывод прост: успех клеточных терапий для восстановления кости будет зависеть не только от самих клеток, но и от стрессовой среды, в которую их помещают, и от молекулярных переключателей, помогающих им справляться. Выделив PENK как перспективную мишень, работа указывает путь к будущим лекарственным или генно‑ориентированным подходам, которые могли бы укрепить восстановление кости у пациентов, ткани которых погружены в окислительный стресс — от пожилых людей до больных с хроническими метаболическими или воспалительными заболеваниями.
Цитирование: Dong, W., Zheng, Y., Zhou, Y. et al. Multi-omics identification of key targets for the osteogenic differentiation of human bone marrow mesenchymal stromal cells under oxidative stress. Sci Rep 16, 8215 (2026). https://doi.org/10.1038/s41598-026-39818-4
Ключевые слова: регенерация кости, окислительный стресс, мезенхимальные стволовые клетки, остеогенная дифференцировка, PENK