Clear Sky Science · ru
Проектирование универсальной многоопытной вакцины против вируса чикунгунья на основе реверсивной вакцинологии: филогенетические и иммуноинформатические подходы
Почему важна новая идея вакцины
Чикунгунья — это переносимый комарами вирус, который может превратить кратковременную лихорадку в месяцы или даже годы болей в суставах, лишая людей способности работать и создавая нагрузку на системы здравоохранения в тропических и субтропических регионах. Существующие вакцины выглядят перспективно, но у некоторых групп возникали опасения по поводу безопасности, и они могут не обеспечивать полноценной защиты от всех вариантов вируса, циркулирующих в мире. В этом исследовании изучается вакцинная конструкция следующего поколения, разработанная с помощью вычислительных методов: цель — сделать её безопаснее, более широко охраняющей и проще в производстве, что даёт представление о том, как цифровые инструменты могут изменить нашу защиту от быстро эволюционирующих вирусов.
Понимание опасности, переносимой комарами
Вирус чикунгунья широко распространился по Америке, Африке и Азии, вызвав сотни тысяч случаев и смертей, особенно во время вспышек. Помимо начальной лихорадки и сыпи, многие пациенты страдают долгосрочными проблемами с суставами, что снижает качество жизни и увеличивает экономические издержки. Вирус представлен тремя основными генетическими линиями, распространёнными в разных регионах мира. Поскольку он мутирует со временем, вакцина, защищающая лишь от одного местного штамма, может быть малоэффективной в других местах. В то же время одна из недавно лицензированных живых вакцин была приостановлена в ряде стран после сообщений о проблемах с безопасностью у пожилых людей, что подчёркивает необходимость альтернативных подходов.
Создание универсальной карты мишеней
Вместо выращивания целого вируса в лаборатории исследователи обратились к глобальным базам данных вирусных последовательностей и мощным инструментам биоинформатики. Из почти 2800 геномов чикунгуньи команда отобрала более 1400 высококачественных последовательностей и построила подробное родословное древо, показывающее взаимосвязь трёх основных линий. Затем они создали «консенсусную» версию структурных белков вируса — тех частей, что находятся на поверхности вируса и наиболее заметны для иммунной системы. Сравнивая тысячи последовательностей, они выявили участки белков, которые остаются высоко схожими между линиями, даже когда другие участки мутируют. Эти консервативные регионы являются идеальными мишенями, потому что вакцина на их основе должна сохранять эффективность по мере изменений вируса.
Проектирование многокомпонентной вакцины
Из консервативных белков в исследовании использовали специализированные онлайн-инструменты для предсказания небольших фрагментов — эпитопов — которые наиболее вероятно распознает иммунная система человека. Некоторые из этих фрагментов, как ожидается, активируют В-клетки, производящие антитела, другие — цитотоксические и хелперные Т-клетки. Просcreenировав кандидатов на предмет силы ответа, отсутствия токсичности и низкого риска аллергии, в окончательный дизайн вошли 10 ключевых эпитопов, взятых из нескольких вирусных белков. Эти короткие фрагменты были сшиты в одну цепочку с использованием гибких линкеров и дополнены человеческим пептидом бета-дефензином в качестве адъюванта, усиливающего иммунный ответ. Компьютерные модели показали, что полученная молекула, вероятно, будет сворачиваться в стабильную форму и распознаваться широким спектром иммунных типов людей в разных популяциях.
Проверка иммунного ответа в компьютере
Затем команда задала вопрос, будет ли эта виртуальная вакцина действительно «взаимодействовать» с иммунной системой. С помощью молекулярного докинга они смоделировали, как разработанный белок может связываться с ключевым сенсором — Toll-подобным рецептором 3, который помогает иммунным клеткам обнаруживать вирусный материал. Результаты показали плотное и стабильное связывание в активном участке рецептора, что является хорошим признаком того, что конструкция может запустить ранние защитные механизмы. Дополнительные компьютерные симуляции иммунного ответа в течение года при трёх имитируемых дозах показали мощные всплески антител и значительное расширение как В-, так и Т-клеток, включая клетки памяти, сохраняющиеся долгое время после вакцинации. Анализ оптимизации кодонов показал, что вакцину, вероятно, можно эффективно производить в широко используемых бактериальных системах, что является преимуществом для изготовления.
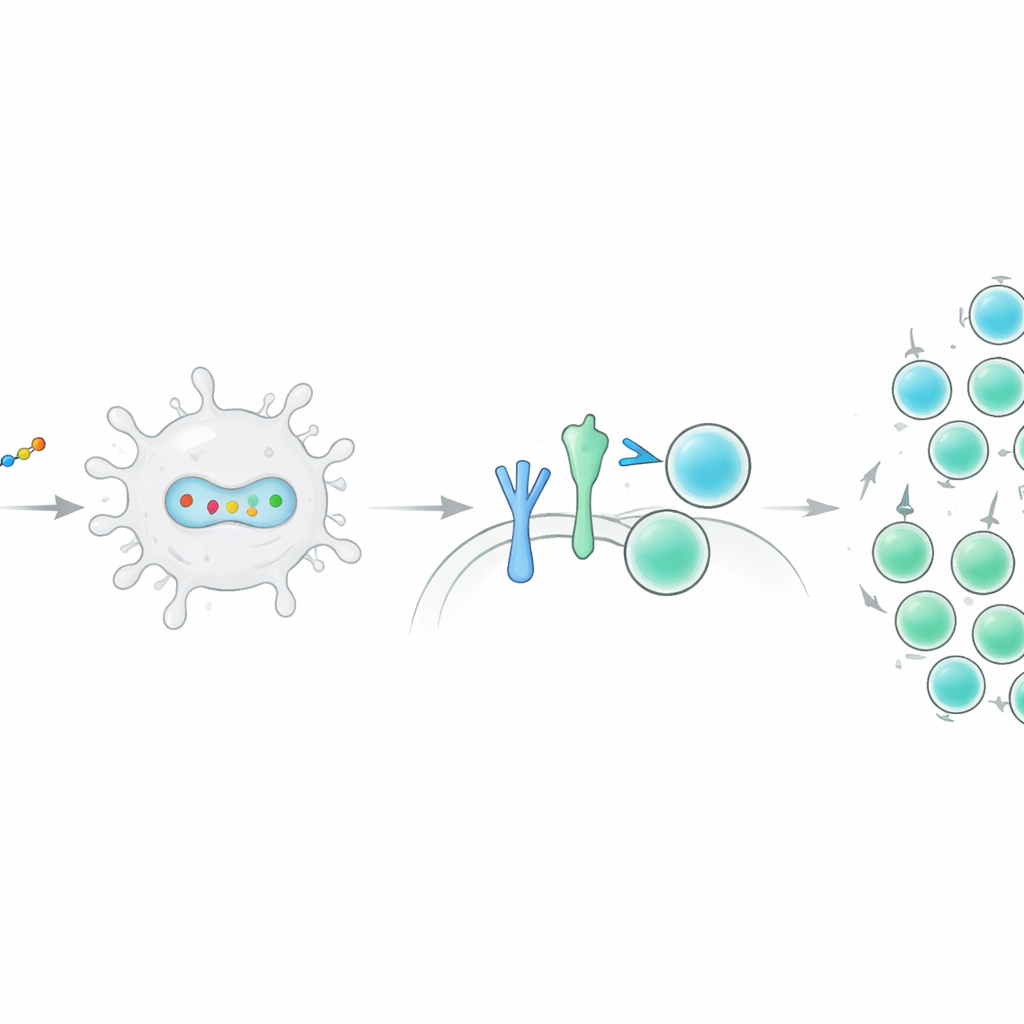
От компьютерного чертежа к защите в реальном мире
В целом исследование представляет тщательно спроектированный план вакцины, нацеленный на консервативные, ценные участки вируса чикунгунья, объединяющий их в одну компактную молекулу и, по данным компьютерных моделей, вызывающий сильные, сбалансированные иммунные ответы в различных популяциях. Для неспециалистов ключевая идея такова: вместо того чтобы полагаться только на традиционные методы проб и ошибок, учёные теперь могут извлекать данные из глобальных вирусных баз и моделировать целые ветви иммунного ответа до выхода в лабораторию. Хотя эта вакцина от чикунгуньи пока существует только в силу и требует строгой проверки в клеточных и животных моделях, она демонстрирует мощный путь к созданию универсальных вакцин, которые остаются эффективными, даже когда вирусы продолжают эволюционировать.
Цитирование: Hakim, M.S. Reverse vaccinology-based design of a universal multiepitope vaccine against chikungunya virus: Phylogenetic and immunoinformatics approaches. Sci Rep 16, 9284 (2026). https://doi.org/10.1038/s41598-026-39790-z
Ключевые слова: вирус чикунгунья, универсальная вакцина, многоопытное проектирование, реверсивная вакцинология, иммуноинформатика