Clear Sky Science · ru
Колонизация опухолей бактериями вызывает активацию иммунитета и усиливает эффективность блокировки контрольных точек
Почему маленькие жильцы в опухолях важны
Лечение рака было преобразовано иммунотерапией, которая освобождает собственные иммунные клетки организма для борьбы с опухолями. Тем не менее многие пациенты по-прежнему получают мало пользы, и предсказать, кто ответит на лечение, трудно. В этом исследовании рассматривается неожиданный фактор, который может изменить расстановку сил: бактерии, живущие непосредственно внутри опухолей. На моделях рака у мышей исследователи показали, что эти микроскопические «жильцы» способны менять поведение иммунной системы в опухоли и вокруг нее и, в конечном счете, влиять на то, сработает ли широко используемая иммунотерапия anti–PD-1 или окажется неэффективной.
Скрытые бактерии внутри опухолей
Много лет основное внимание уделялось триллионам микробов в кишечнике и их влиянию на общую иммунную систему. Более недавно учёные обнаружили, что многие человеческие опухоли также содержат небольшие, но активные бактериальные сообщества. Авторы этого исследования задали два базовых вопроса: содержат ли широко используемые мышиные модели опухолей бактерии и, если да, влияют ли эти бактерии на рост опухолей и ответ на лечение? Они сравнили две модели: MCA-205, тип саркомы, и MOC1, модель рака головы и шеи. Используя методы на основе ДНК, секвенирование и культуру, они обнаружили, что в опухолях MCA-205 постоянно присутствовали живые бактерии, тогда как в MOC1 их не было, даже когда опухоли располагались в богатой бактериями полости рта. В MCA-205 уровни бактерий, как правило, увеличивались по мере роста опухолей, что указывало на то, что растущая опухоль создаёт благоприятную нишу для микробов.
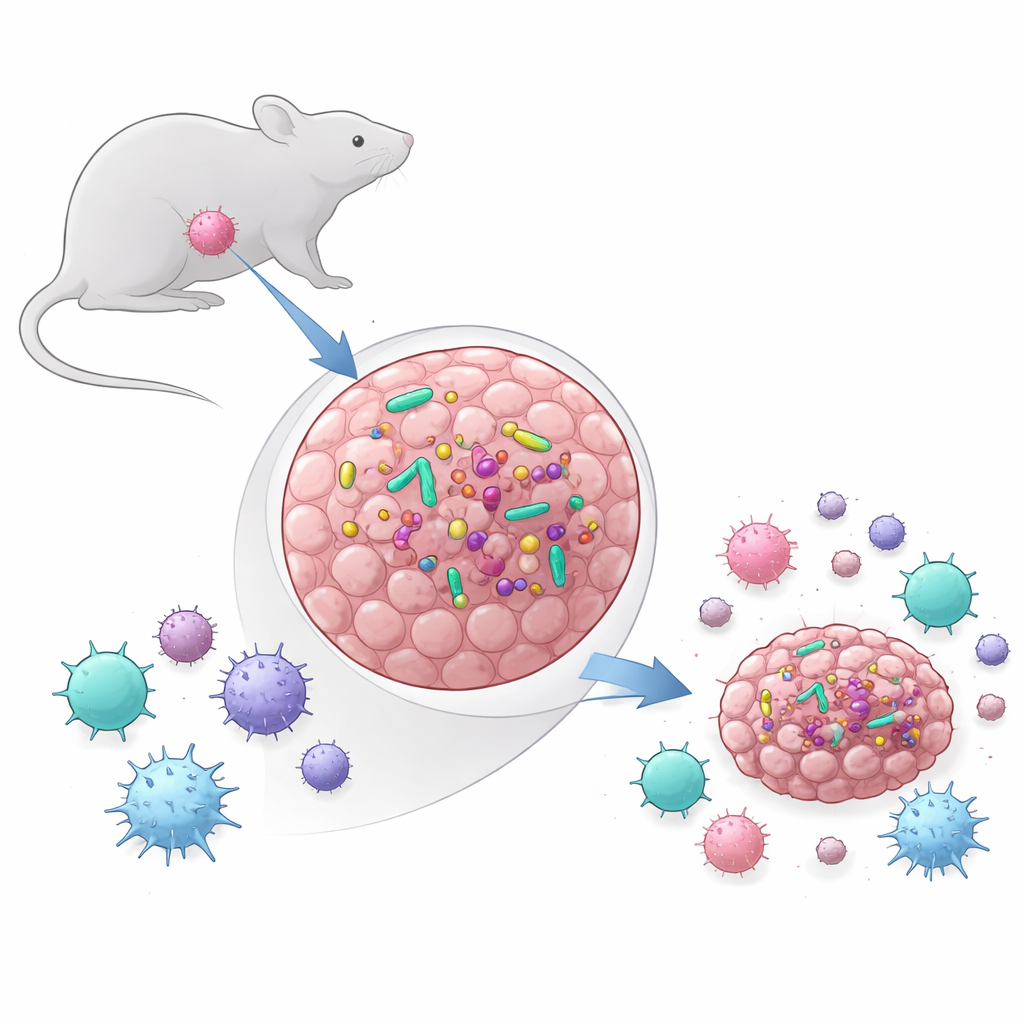
Откуда приходят микробы
Нахождение бактерий внутри опухолей вызвало ещё один вопрос: с кожи, из рта или из кишечника эти захватчики попадают в опухоль? Сравнивая ДНК бактерий в опухолях с образцами стула, соскобами с кожи и ротовой полости, исследователи обнаружили, что внутриотопическое сообщество было проще и менее разнообразно, чем богатые экосистемы в кишечнике и рту. Большинство типов бактерий в опухолях перекрывалось с теми, что наблюдались в желудочно-кишечном тракте, тогда как сравнительно немногие совпадали с кожной микрофлорой. Это указывает на то, что бактерии могут проникать из кишечника или ротовой полости в кровь и затем заселять опухоль, где устойчивая популяция остается лишь у определённых видов. Состав бактериальных групп напоминал тот, что описан в нескольких человеческих раковых формах, что подкрепляет идею о том, что эти мышиные модели можно считать отражением реальных взаимодействий между опухолью и микробами.
Как бактерии в опухоли формируют успех иммунотерапии
Ключевым результатом исследования является то, что бактерии, обитающие в опухоли, могут определять успех терапии anti–PD-1, ингибитора контрольной точки, призванного восстановить активность истощённых киллерных Т‑клеток. Когда команда использовала антибиотики, проникающие в опухоль и уничтожающие местные бактерии при относительно небольшом воздействии на колонизацию кишечника, опухоли MCA-205 стали значительно менее чувствительны к anti–PD-1. Ответы падали ещё больше при широком нарушении кишечной микробиоты. Напротив, в опухолях MOC1, изначально лишённых обнаруживаемых бактерий, антибиотики мало влияли ни на бактериальную нагрузку, ни на исход лечения. В MCA-205 опухоли, которые сокращались в ответ на anti–PD-1, как правило, содержали больше бактерий, чем те, что устойчиво сопротивлялись терапии, связывая высокую внутриотопическую бактериальную нагрузку с лучшим контролем роста.
Внутри иммунного фронта
Чтобы понять, как бактерии смещают иммунный баланс, исследователи изучили иммунные клетки внутри и вокруг опухолей. Когда внутриотопические бактерии удаляли с помощью опухоль-проникающих антибиотиков, в опухоли проникало меньше киллерных CD8 Т‑клеток, а соотношение этих клеток к регуляторным Т‑клеткам смещалось в сторону подавления. Дендритные клетки, «разведчики», захватывающие опухолевый материал и активирующие Т‑клетки, также встречались реже и демонстрировали более низкие признаки активации при отсутствии бактерий. Интересно, что простое добавление дополнительного штамма безвредной E. coli в опухоль или отключение ключевого пути распознавания микробов (MyD88) в основных иммунных клетках не усиливало терапию. Это подразумевает, что важна не любая бактериальная присутствие или простой сигнал тревоги; вероятно требуются специфические сообщества и более тонкая коммуникация с иммунной системой.
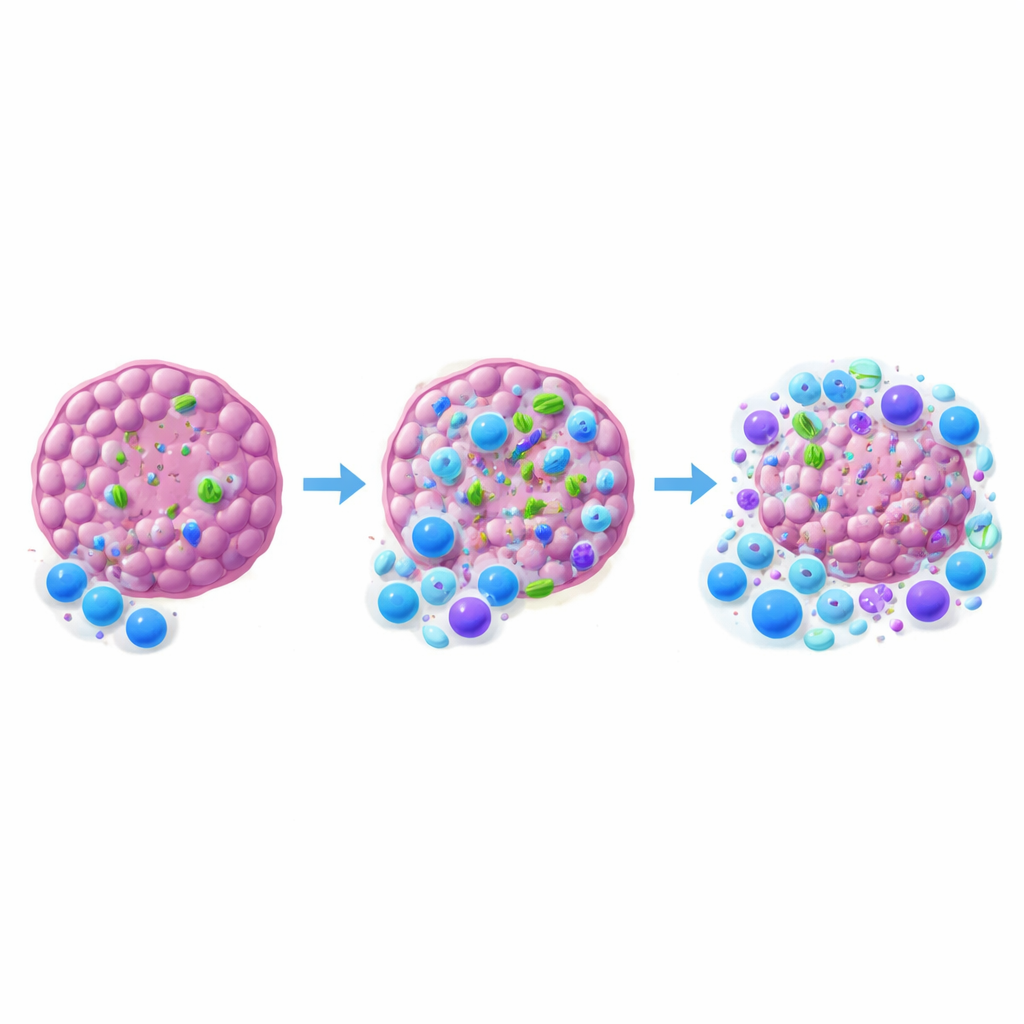
Что это означает для будущего лечения рака
Для неспециалиста вывод таков: бактерии, живущие внутри опухолей, не являются простыми наблюдателями. По крайней мере в некоторых видах рака они помогают привлекать в опухоль нужные иммунные клетки и поддерживать действие препаратов anti–PD-1. Другие опухоли могут оставаться почти свободными от бактерий и отвечать на лечение совсем иначе. По мере того как ученые проектируют и тестируют новые подходы на мышиных моделях, важно знать, содержит ли конкретная модель опухоли бактерии — и какие именно — чтобы правильно интерпретировать результаты и выбирать стратегии, пригодные для переноса в клинику. В долгосрочной перспективе тонкая настройка микросообществ внутри самих опухолей может дополнить лекарства и иммунные клетки как новый инструмент для улучшения раковой иммунотерапии.
Цитирование: Rolig, A.S., Ziglari, T., McGee, G.H. et al. Bacterial colonization of tumors drives immune activation and checkpoint blockade efficacy. Sci Rep 16, 8464 (2026). https://doi.org/10.1038/s41598-026-39758-z
Ключевые слова: внутриотопическая микробиота, раковая иммунотерапия, анти-PD-1, микроокружение опухоли, бактерии и опухоли