Clear Sky Science · ru
Криптическая резервность между PAR1b и PAR1a, двумя членами семейства киназ PAR1, в выживании мышей с нокаутом PAR1b
Как клетки находят запасной план при повреждении ДНК
Наши клетки постоянно сталкиваются с повреждениями ДНК, и когда системы ремонта дают сбой, это может привести к раку или гибели в ходе развития. В этом исследовании изучается неожиданная спасительная стратегия у мышей: когда отсутствует ключевой белок, помогающий известному связанному с раком гену BRCA1 выполнять свою функцию, его место тихо занимает близкий родственник. Работа показывает, как ранние эмбрионы могут перенастроить свои механизмы контроля генов, чтобы выжить, и дает новое понимание того, почему некоторые генетические дефекты смертельны, а другие — неожиданно переносимы.
Семейство организаторов клетки с скрытой ролью
Исследователи сосредоточились на семействе ферментов, называемых киназами PAR1, которые помогают клеткам поддерживать внутреннюю организацию. Один из членов семьи, PAR1b, ранее был показан как направляющий BRCA1 в ядро клетки, где BRCA1 контролирует точный ремонт ДНК и защищает уязвимые участки репликации ДНК. Полное удаление BRCA1 у мышей приводит к ранней эмбриональной гибели, что подчеркивает его важность. Тем не менее, что удивительно, мыши полностью лишенные PAR1b доживают до взрослого состояния, хотя PAR1b действует выше по потоку относительно BRCA1. Это несоответствие наводило на мысль, что другая киназа PAR1 может тихо заместить PAR1b в определенных условиях.
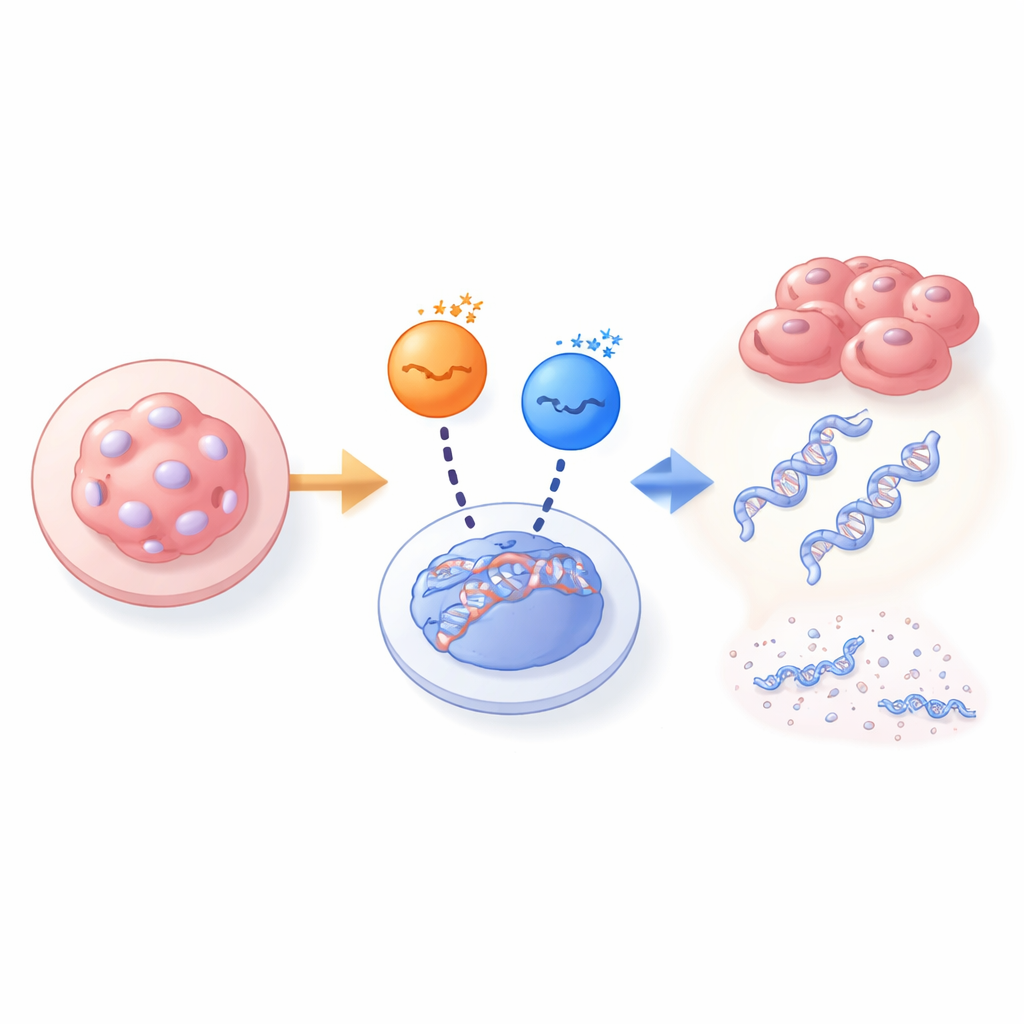
Когда одна киназа выходит из строя, другая вступает в действие
Чтобы пролить свет на эту загадку, команда сравнила эмбриональные фибробласты мышей, полученные от нормальных эмбрионов, с клетками от эмбрионов, полностью лишенных PAR1b. В нормальных клетках подавление PAR1b резко снижало уровень BRCA1 в ядре и вызывало всплеск маркеров разрывов ДНК, что, в свою очередь, блокировало рост клеток. Подавление других киназ PAR1 (PAR1a, PAR1c, PAR1d) практически не влияло на ситуацию. Однако в клетках, полученных от эмбрионов без PAR1b, BRCA1 сохранялся в ядре и ДНК оставалась относительно целой, несмотря на отсутствие PAR1b. В этих клетках с нулевым PAR1b удаление PAR1a стало летальным, тогда как удаление PAR1c или PAR1d — нет. Эта смена зависимости показала, что PAR1a приняла на себя роль PAR1b в доставке BRCA1 в ядро, но только в эмбрионах, которые с самого начала лишались PAR1b.
Ранняя эпигенетическая перенастройка как стратегия выживания
Исследователи предположили, что эта скрытая резервная система связана с эпигенетикой — тем, как ДНК упакована и химически маркирована для включения или выключения генов без изменения последовательности. Используя геномный анализ открытости хроматина, они обнаружили тысячи регионов, где доступность ДНК различалась между нормальными и PAR1b‑нолк клетками. Многие изменения касались генов, контролирующих упаковку и модификацию хромосом, что указывает на широкую перепрограммировку сети регуляции генов. Одним из заметных эффектов стало влияние на ген 53BP1 — белок, который обычно сдвигает клетки в сторону «быстрого и грубого» пути ремонта ДНК, противопоставляемого более точному механизму BRCA1. В клетках без PAR1b участок тела гена 53BP1 оказался более плотно упакованным, а уровни его РНК и белка значительно снизились.
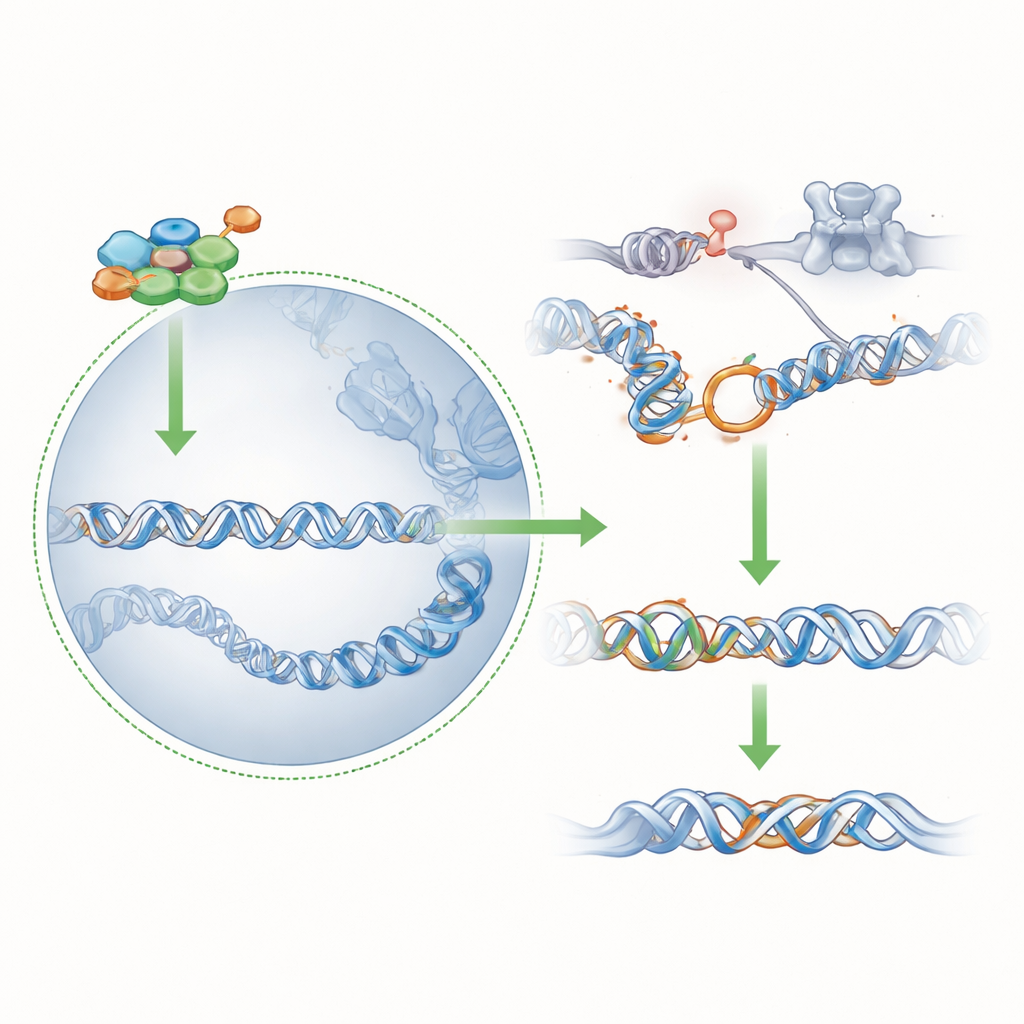
Сдвиг баланса между путями ремонта
Путем понижения уровня 53BP1 эмбрион фактически уменьшает свою зависимость от полной мощности BRCA1: даже скромного количества BRCA1 в ядре, доставляемого PAR1a вместо PAR1b, теперь достаточно, чтобы поддерживать достаточный точный ремонт и сохранить клетки живыми. Эксперименты с бактериальным белком, который отключает все киназы PAR1, подтвердили, что присутствие BRCA1 в ядре у клеток без PAR1b по‑прежнему зависит от активности семейства PAR1, конкретно от PAR1a. В целом результаты рисуют картину, в которой ранняя потеря PAR1b запускает быструю перестройку хроматина и сети ремонта ДНК, подавляя противника BRCA1 (53BP1) и выявляя способность PAR1a замещать PAR1b.
Что это значит для заболеваний и лечения
Эта работа вводит понятие «криптической резервности»: резервной функции, которая существует, но обычно дремлет и проявляется только тогда, когда ключевой компонент теряется очень рано в развитии. У мышей это позволяет эмбрионам пережить утрату PAR1b, в отличие от утраты самого BRCA1. Полученные данные также наводят на мысль, что некоторые люди с поражающими вариантами PAR1b могут выживать благодаря включению подобных резервных механизмов, хотя не без возможных последствий для функции мозга, метаболизма или риска рака. В перспективе понимание того, как ранние эпигенетические настройки подавляют 53BP1 и переключают контроль BRCA1 с PAR1b на PAR1a, может вдохновить стратегии преднамеренного имитирования этих изменений — либо чтобы защитить клетки, потерявшие PAR1b, либо чтобы тонко настраивать пути ремонта ДНК в терапии рака.
Цитирование: Murata-Kamiya, N., Del Valle Lazarte, A.A., Kikuchi, I. et al. Cryptic redundancy between PAR1b and PAR1a, two members of the PAR1 kinase family, in the survival of PAR1b-knockout mice. Sci Rep 16, 5971 (2026). https://doi.org/10.1038/s41598-026-39737-4
Ключевые слова: BRCA1, Ремонт ДНК, резервность киназ, эпигенетическая регуляция, эмбриональное развитие