Clear Sky Science · ru
Разработка интегрированной вычислительно‑экспериментальной среды для прогнозирования силы шлифования и безопасности при операциях ультразвуковым костным скальпелем
Более острые инструменты — более безопасный позвоночник
Операции на позвоночнике часто требуют удаления небольших участков кости на расстоянии всего в несколько миллиметров от спинного мозга и нервов. Хирурги сегодня используют специальные ультразвуковые «костные скальпели», которые быстро вибрируют, чтобы рассекать кость, щадя мягкие ткани; однако при слишком большой нагрузке на кость существует риск повреждения близлежащих нервов или сосудов. В данной работе показано, как компьютерные симуляции и роботизированные эксперименты могут дополнять друг друга для заранее прогнозирования этих сил, помогая врачам и будущим хирургическим роботам выбирать параметры, которые делают операции одновременно эффективными и безопасными.
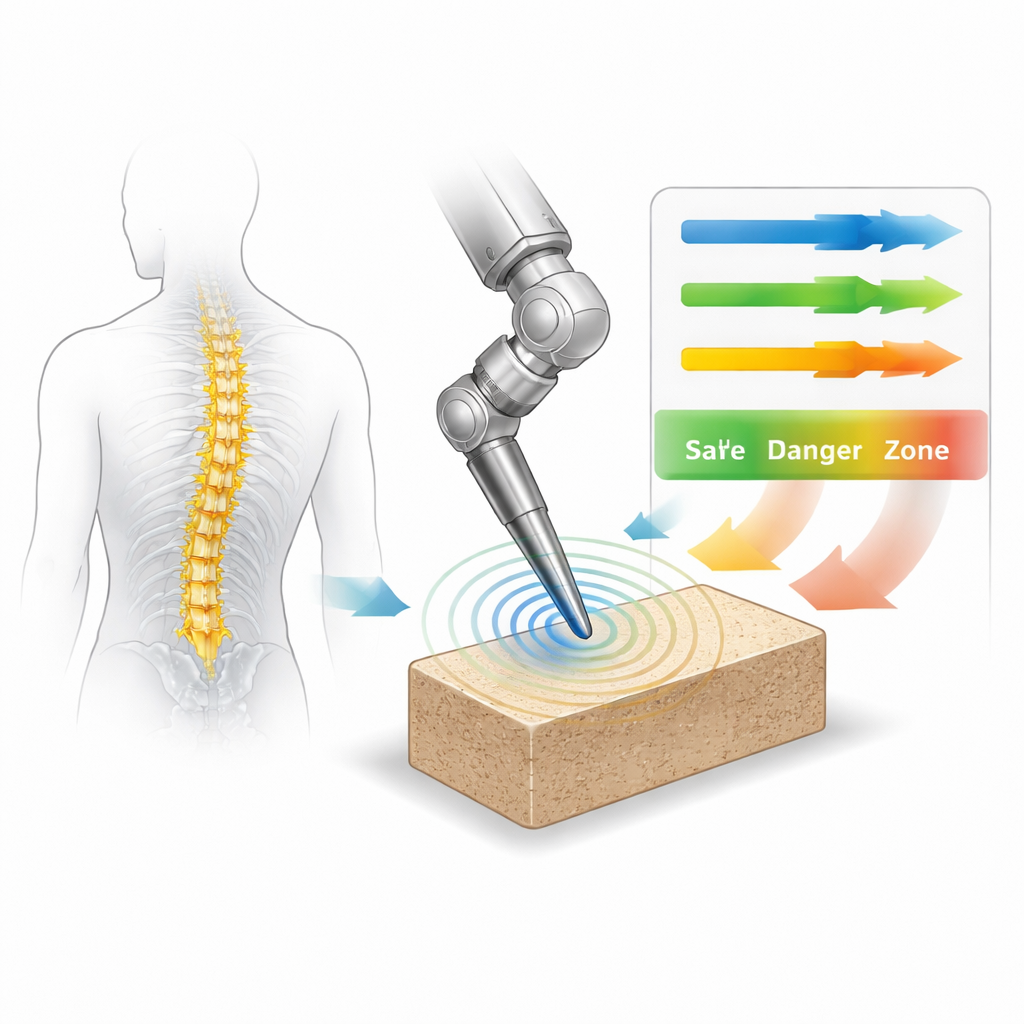
Почему резание кости столь деликатно
Детям с тяжёлыми деформациями позвоночника, такими как геми- или полувертебра, часто требуется сложная операция, при которой удаляют деформированные фрагменты позвонков и восстанавливают форму позвоночного столба. Традиционные высокоскоростные боры в таких условиях трудно контролировать, и они могут создавать непредсказуемые силы на кость. Ультразвуковые костные скальпели, напротив, используют высокочастотную вибрацию и небольшой шлифовальный наконечник, чтобы снимать кость, в значительной мере щадя мягкие ткани. Тем не менее движение мельчайших абразивных частиц на рабочем конце инструмента оказывается удивительно сложным: головка вращается, подаётся вперёд и вибрирует в нескольких направлениях одновременно. Поскольку сама кость варьируется от мягких губчатых областей до очень плотных внешних слоёв, возникающая при шлифовании сила зависит от взаимодействия всех этих движений с конкретной структурой кости.
Построение виртуальной мастерской по обработке позвоночника
Чтобы распутать эту сложность, исследователи создали детальную трёхмерную компьютерную модель процесса шлифования. Они использовали инженерное программное обеспечение для представления как блока материала, похожего на кость, так и вращающегося, вибрирующего цилиндрического инструмента. Движение каждой абразивной точки на инструменте было описано математически и затем перенесено в симуляцию, чтобы виртуальный инструмент двигался так же, как реальный ультразвуковой скальпель. Материал кости моделировали так, чтобы он мог деформироваться, трескаться и крошиться при быстрых нагрузках, имитируя реальные механизмы разрушения при механической обработке. Команда уделила особое внимание уточнению сетки — мельчайших элементов, составляющих виртуальную кость — в зоне контакта, чтобы локальные напряжения и трещины, а значит и силы резания, фиксировались с высокой точностью.
Испытание ключевых «ручек», которыми управляет хирург
Вместо случайной смены параметров команда применила структурированный план эксперимента, чтобы исследовать три практически важные «ручки»: плотность кости, амплитуду вибрации и скорость подачи (насколько быстро продвигается инструмент). С помощью дизайна Бокса–Бенкена они провели 17 тщательно отобранных симуляционных прогонов, эффективно охватив комбинации низких, средних и высоких значений каждого фактора. По результатам этих прогонов они построили гладкую поверхность отклика — математическую карту, предсказывающую силу шлифования для любой настройки в пределах исследуемого диапазона. Карта показала явные закономерности: более плотная кость и большая скорость подачи увеличивали силу, тогда как большая ультразвуковая амплитуда снижала её, поскольку контакт становился более прерывистым, похожим на ударное резание, при котором кость удаляется с меньшим устойчивым сопротивлением.
Проверка модели на роботе
Чтобы понять, выдерживают ли виртуальные прогнозы проверку в реальном мире, команда собрала роботизированную платформу для шлифования. Программируемый роботизированный манипулятор направлял коммерческий ультразвуковой костный скальпель по стандартизированным синтетическим брускам, в то время как шестиковая сенсорная система измеряла силу шлифования. Параметры варьировали по одному — скорость подачи, амплитуда вибрации или плотность материала — удерживая остальные фиксированными. После фильтрации шумов в сигналах силы они сравнили измеренные значения с теми, что предсказывала их модель поверхности отклика. По всем тестам типичное отклонение было значительно меньше одного ньютона, а худшая относительная погрешность после удаления экстремальных значений составила около 7 процентов, что свидетельствует о том, что комбинированная симуляционно‑экспериментальная среда захватывает доминирующую механику процесса.

Проведение черты между безопасным и рискованным
Имея надёжный инструмент прогнозирования, исследователи затем перевели предел силы из предыдущих работ — 20 ньютонов, уровень, выбранный для защиты чувствительных нервных тканей — в практические рекомендации по работе. С помощью своей модели они вычислили, какие комбинации плотности кости, скорости подачи и ультразвуковой амплитуды приведут к превышению или сохранению этой границы. Результаты они представили в виде цветных тепловых карт, где холодные цвета обозначали безопасные области, а тёплые — опасные. Эти карты показывают, например, что хирурги могут работать быстрее в мягкой губчатой кости, но должны замедляться или увеличивать амплитуду вибрации при обработке плотной корковой кости, чтобы избежать чрезмерных нагрузок.
От плановых карт к более «умным» хирургическим роботам
Проще говоря, эта работа превращает сложное, трудноощутимое взаимодействие между вибрирующим инструментом и живой костью в набор ясных количественных «ограничений скорости» для операций на позвоночнике. Предсказывая, как изменится сила при изменении настроек инструмента или при встрече с разной качественной структурой кости, среда помогает безопаснее планировать процедуру до операции и открывает путь к управлению силой в реальном времени в роботизированных системах. Будущие версии, включающие данные пациентов и более детальную модель поведения кости, могли бы адаптировать эти границы безопасности под каждого человека, направляя как хирургов, так и интеллектуальные роботы к более точным и менее рискованным вмешательствам на позвоночнике.
Цитирование: Li, C., Chen, G., Xu, Y. et al. Development of an integrated computational-experimental framework for predicting grinding force and safety in ultrasonic bone scalpels operations. Sci Rep 16, 9347 (2026). https://doi.org/10.1038/s41598-026-39710-1
Ключевые слова: ультразвуковой костный скальпель, операции на позвоночнике, хирургическая робототехника, конечномерное моделирование, безопасность хирургии