Clear Sky Science · ru
Таргетирование конкретных типов нейронов в мозге нечеловеческих приматов с помощью рекомбинантного иммунотоксина, специфичного к мышиному CD25
Почему это исследование мозга важно
Понимание того, как конкретные группы клеток мозга контролируют движение, эмоции и поведение, ключево для лечения таких расстройств, как болезнь Паркинсона и аутизм. Но мозг — плотный лес переплетённых клеток, и большинство инструментов «срубает» сразу много деревьев. В этом исследовании предложен способ удалить только выбранный тип нейрона в мозге обезьяны с минимальным сопутствующим ущербом, что открывает путь к гораздо более точным экспериментам о том, как отдельные цепи формируют поведение и болезни.
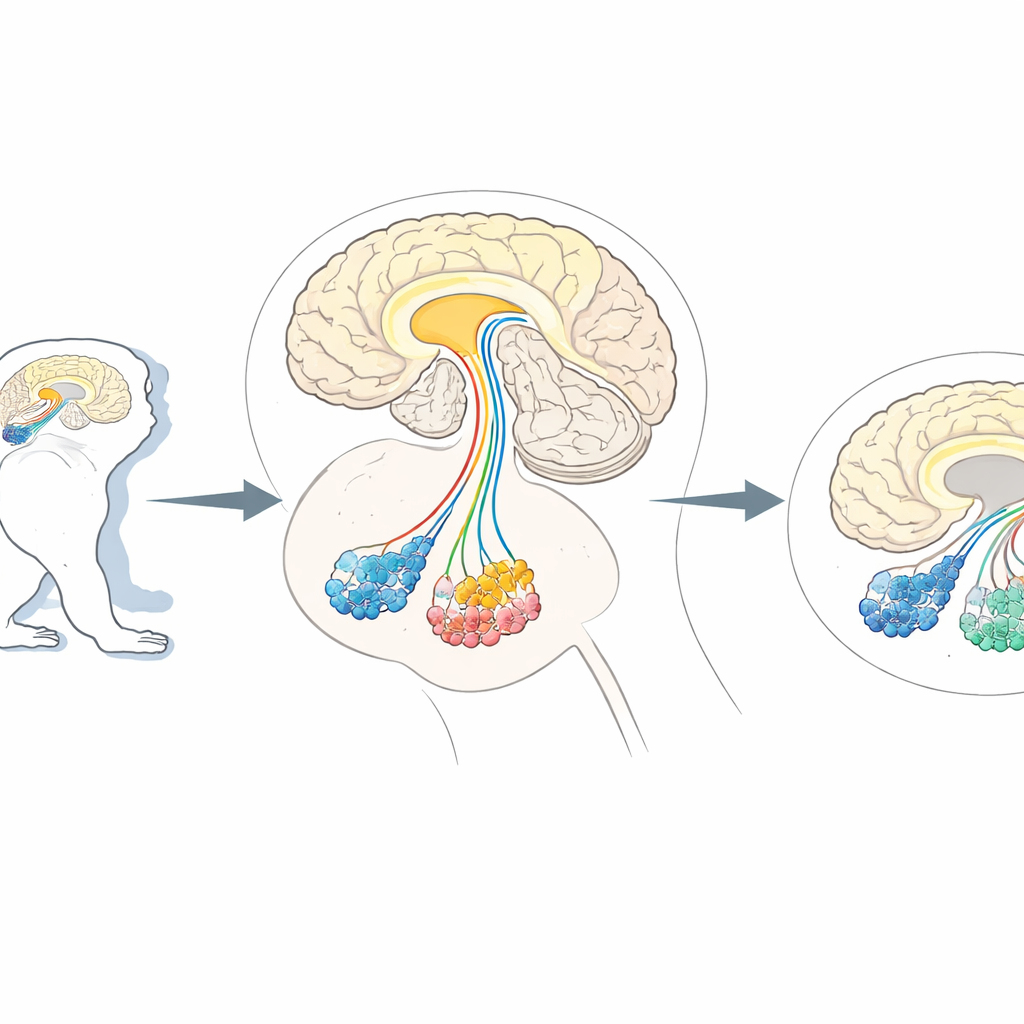
Необходимость точной «обрезки» клеток мозга
Исследователи часто прибегают к нечеловеческим приматам, таким как мармозетки и макаки, поскольку их мозг устроен очень похоже на наш. Эти животные представляют ценную модель состояний, затрагивающих высшие мозговые функции — от паркинсонических нарушений движения до изменений в социальном поведении, напоминающих аутизм. Существующие методы могут отключать или стимулировать определённые пути, но фактически удалить лишь один тип нейронов в этих сложных мозгах, не повредив другие, было трудно. Ранее в мышах применяли трюк: выбранные нейроны генетически модифицировали так, чтобы они экспрессировали человеческий клеточный маркер CD25, который распознаётся дизайнерским токсином, убивающим только отмеченные клетки. Однако этот же маркер естественно встречается в иммунных и, возможно, в некоторых мозговых клетках приматов, что повышает риск того, что токсин нападёт не на те цели в обезьянах.
Проектирование более безопасного молекулярного скальпеля
Авторы поставили цель создать новый молекулярный скальпель, предназначенный для использования у приматов. Вместо того чтобы нацеливаться на человеческую версию CD25, они сосредоточились на мышином варианте, который значительно менее сходен с естественным CD25 у обезьян. Сначала они иммунизировали кролика белком мышиного CD25 и с помощью чиповой технологии отобрали отдельные клетки кролика, производившие антитела, которые прочно связывались с мышиным CD25, но не с человеческим. Из них выделили выдающееся антитело, названное RMAb-52, с очень высокой аффинностью. Затем ключевые фрагменты этого антитела скомбинировали с токсическим фрагментом от бактерии Pseudomonas, чтобы получить единый сконструированный белок — иммунтотоксин под названием anti-mCD25-PE38.
Испытание инструмента в действии
В экспериментах в пробирке новый иммунтотоксин связывался с мышиным CD25 значительно сильнее, чем с человеческим, что подтвердило его селективность. При применении к культурам клеток, генетически несущих мышиный CD25, токсин резко снижал их выживаемость при очень низких дозах, оставляя при этом неповреждёнными клетки с человеческим CD25. Затем команда перешла к живым мармозеткам. С помощью специального вирусного вектора, перемещающегося ретроградно вдоль нервных волокон, они доставили ген мышиного CD25 в дофаминовые нейроны, посылающие сигналы из глубокой области мозга — черного субстанции (substantia nigra) — в стриятум, путь, критичный для контроля движения. После того как вирус успел включить экспрессию маркера в этих нейронах, в целевую область среднего мозга инъецировали белок anti-mCD25-PE38 напрямую.
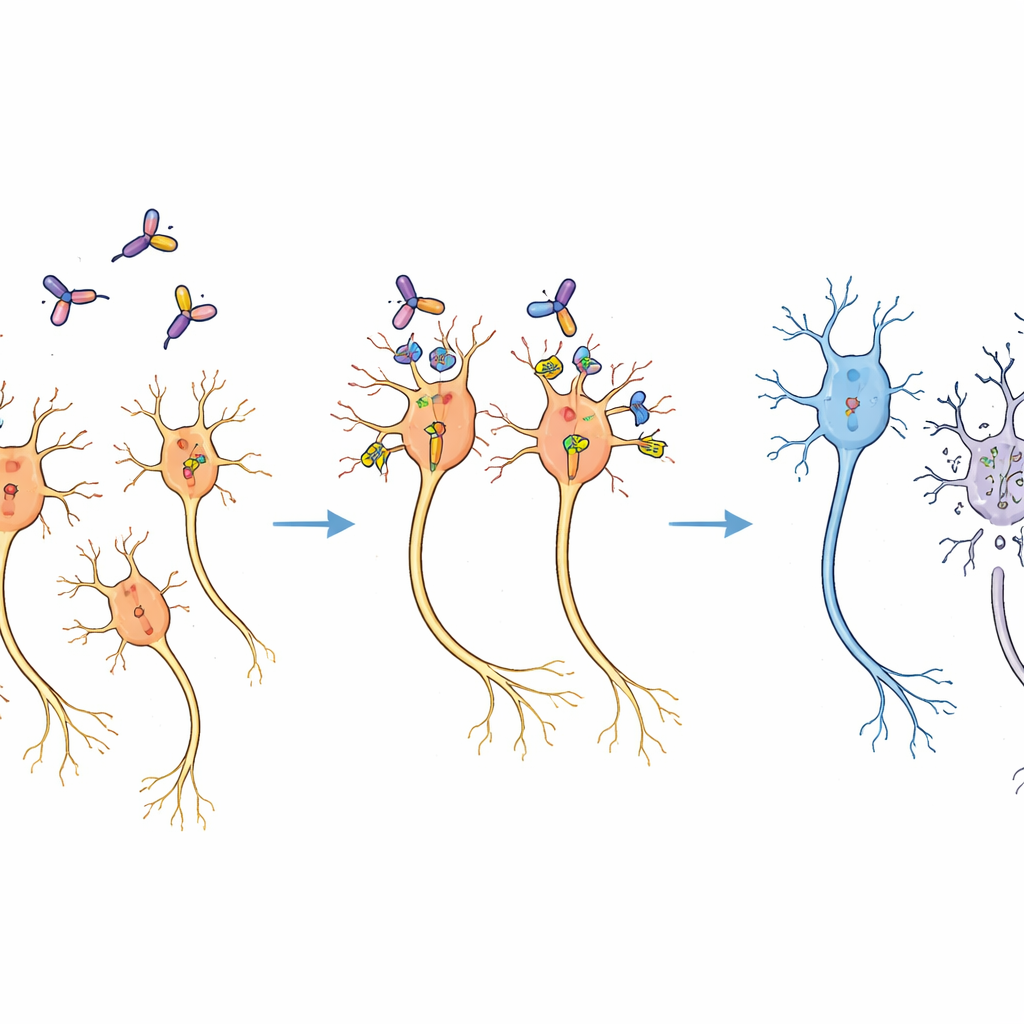
Селективная утрата без широкого повреждения
Две недели после лечения срезы мозга мармозеток показали ясную картину. На стороне, получившей иммунтотоксин, число дофаминовых нейронов снизилось примерно до двух третей от количества на не обработанной стороне, что видно по окраске на фермент, синтезирующий дофамин. В то же время окружающая ткань выглядела нормально под микроскопом, и другие области мозга, подверженные воздействию вирусного вектора, не показали очевидной потери клеток. Пилотные эксперименты заранее определили диапазон доз, избегающий неспецифического повреждения ткани, и выбранная доза находилась в пределах этого безопасного окна. Шаблон утраты соответствовал ожидаемому распространению вируса и токсина, что указывает на то, что нейроны были уничтожены именно потому, что в них был индуцирован мышиный CD25, а не из‑за неспецифического воздействия токсина на клетки.
Что это означает для будущих исследований мозга
Для неспециалиста ключевое сообщение в том, что исследователи создали высокоселективную «кнопку удаления» для выбранных популяций нейронов в мозге приматов. Комбинируя ретроградную вирусную систему доставки с мышиноспецифичным иммунтотоксином, они могут устранить определённые пути — например, дофаминовые цепи, вовлечённые в болезнь Паркинсона — при сохранении соседних клеток. Эта стратегия избегает опасных перекрёстных реакций с собственным CD25 животного и особенно полезна, когда естественный рецептор присутствует или повышен при заболевании. В долгосрочной перспективе такой подход поможет учёным картировать, как отдельные маршруты в мозговой проводящей сети влияют на движение, принятие решений и психиатрические симптомы, приближая нас к таргетным методам лечения, которые корректируют неверные цепи вместо того, чтобы широко воздействовать на весь мозг.
Цитирование: Kobayashi, T., Kato, S., Kimura, S. et al. Targeting of specific neuronal types in the non-human primate brain by using a murine CD25-specific recombinant immunotoxin. Sci Rep 16, 8247 (2026). https://doi.org/10.1038/s41598-026-39662-6
Ключевые слова: нейронаука нечеловеческих приматов, таргетирование иммунотоксином, дофаминовые нейроны, мозговые цепи мармозеток, модели болезни Паркинсона