Clear Sky Science · ru
Разрешение противоречия между моделированием и экспериментальными результатами применения золотых наночастиц в протонной терапии
Почему крошечные частицы золота важны для лечения рака
Протонная терапия — это современный вид лучевой терапии, который может точно нацеливать опухоли, щадя окружающие здоровые ткани. В последние годы учёные пытались сочетать протонную терапию с мельчайшими частицами золота, называемыми золотыми наночастицами, чтобы сделать лечение ещё более губительным для раковых клеток. В экспериментах такая комбинация часто убивает больше опухолевых клеток, чем одни протоны, — однако компьютерные симуляции изо всех сил пытались объяснить, почему. В этой работе рассматривается долгое противоречие и указывается на иной главный механизм, чем тот, который ожидали многие исследователи.
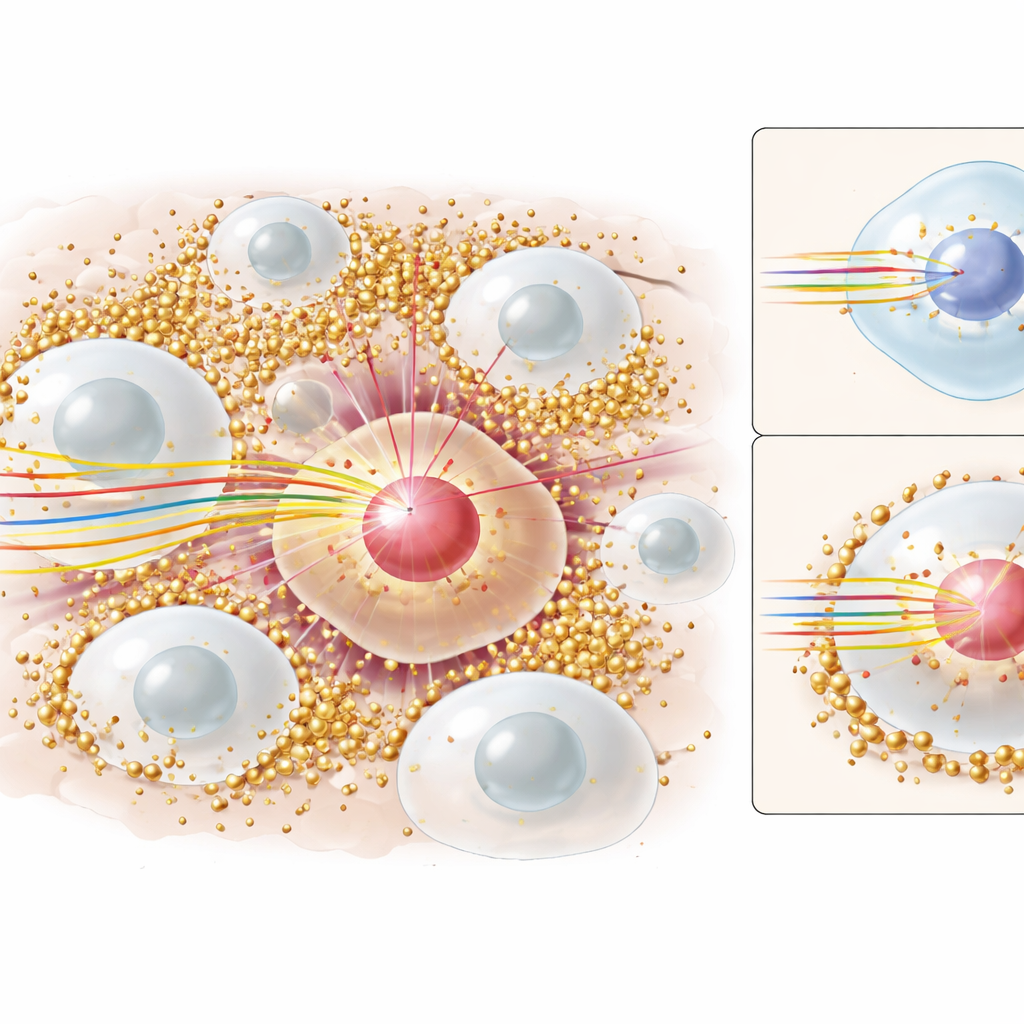
Старая версия: винить быстрые электроны
Золотые наночастицы уже известны в рентгеновой и гамма‑терапии, где они усиливают повреждения в основном за счёт выброса потока энергетических электронов. Эти электроны проходят небольшие расстояния и разрушают ДНК в близлежащих клетках. На протяжении многих лет считали, что в протонной терапии действует та же базовая картина: протоны сталкиваются с золотом, дополнительные электроны вылетают, и клетки терпят ущерб. Но возникала проблема. Подробные компьютерные модели, отслеживающие каждую частицу и её энергию — подобные тем, что использованы в этом исследовании — постоянно предсказывали очень незначительное дополнительное поглощение в ядре клетки от этих электронов, особенно потому, что большинство наночастиц находится во внешней области клетки, а не внутри ядра, где расположена ДНК. В то же время лабораторные эксперименты на клетках показывали явное увеличение гибели клеток и эффективности лечения при наличии золота. Числа просто не сходились.
Новая картина: замедление самих протонов
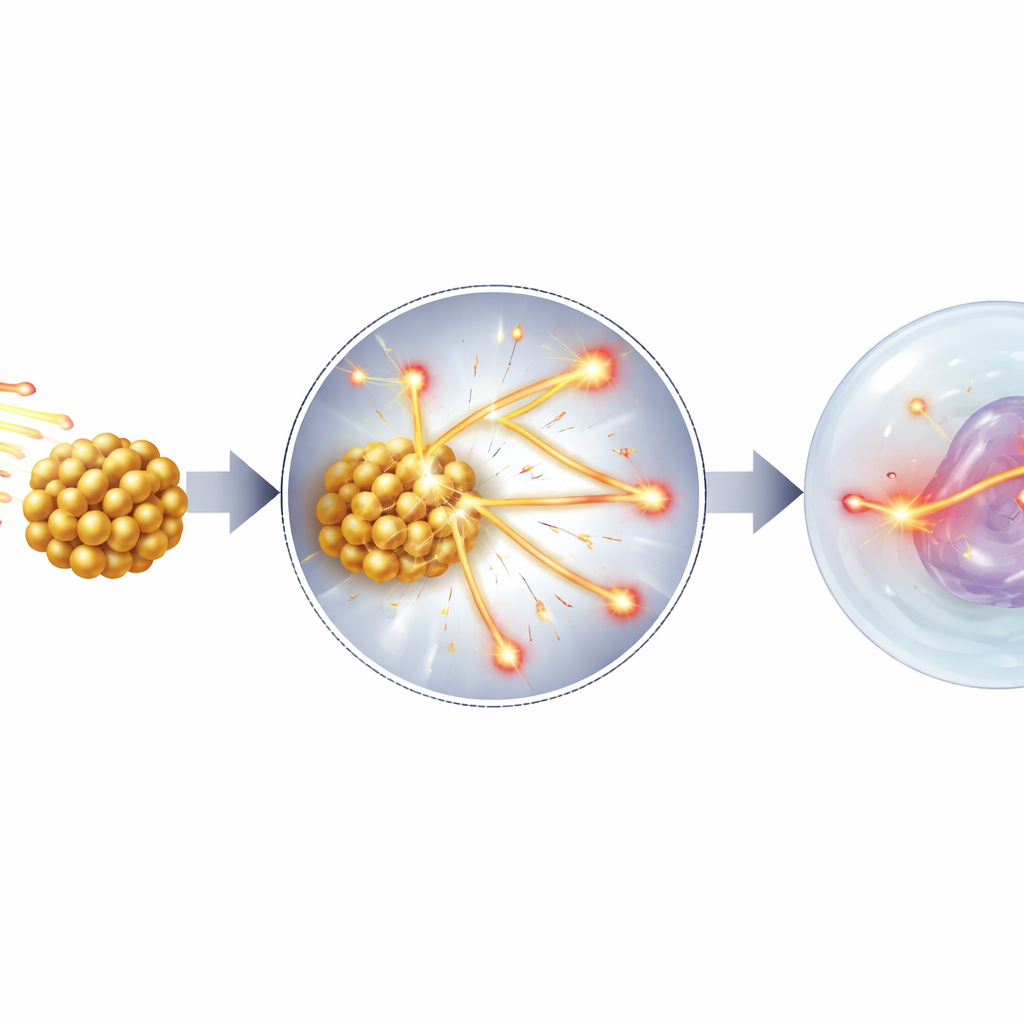
Эта работа предлагает и проверяет иной основной механизм: вместо того чтобы действовать главным образом как источники электронов, золотые наночастицы ведут себя как крошечные «лежачие полицейские» для протонов. Когда протон проходит через область, усыпанную плотными, с высоким атомным номером металлами, такими как золото или железо, он испытывает множество мелких столкновений с тяжёлыми атомами. Каждое столкновение забирает немного больше энергии, чем в обычной ткани, поэтому протон замедляется быстрее, и его потеря энергии на единицу пути — известная в физике как линейная передача энергии (LET) — увеличивается. Трэки с высоким LET особенно опасны для ДНК, потому что они создают плотные кластеры разрывов, которые клетке трудно восстановить. С помощью подробных Монте‑Карло симуляций в Geant4 автор показывает, что золото и другие тяжёлые наночастицы значительно увеличивают число медленных, высоко‑LET протонов, достигающих ядра клетки, хотя общая длина пути составляет микрометры, что существенно больше диапазона традиционно обвиняемых низкоэнергетических электронов.
Согласование симуляций с реальными клеточными экспериментами
Чтобы проверить жизнеспособность этой картины, исследование воспроизводит несколько опубликованных клеточных экспериментов, где опухоли облучали протонными пучками в сочетании с различными наночастицами (золото, железо и платина) разных размеров и концентраций. Для каждого случая симуляции вычисляют, насколько больше дозы получает ядро — суммируя это в коэффициент усиления дозы — а затем подставляют полученные значения в стандартную радиобиологическую формулу, связывающую доставленную дозу с выживанием клеток. Такой подход модифицирует привычную кривую, описывающую, сколько клеток выживает или погибает после данной дозы излучения. Для большинства рассмотренных экспериментов прогнозируемые кривые выживаемости с наночастицами совпадали с измеренными данными довольно точно, часто с погрешностью около одного процента. При этом симуляции показывают, что доза электронов в ядре едва меняется при добавлении наночастиц, тогда как поток более медленных, более разрушающих протонов явно увеличивается. Оставались некоторые рассогласования, которые автор связывает с неопределённостями в том, как были устроены или описаны отдельные эксперименты, но общая тенденция сильно поддерживает объяснение, основанное на замедлении протонов.
Ограничения, исключения и когда золото особенно помогает
В статье также рассматриваются ситуации, где наночастицы, по‑видимому, мало помогают. Для очень низкоэнергетичных протонных пучков, которые останавливаются всего в нескольких слоях клеток, просто не существует достаточного расстояния, чтобы протоны встретили много наночастиц и заметно замедлились, поэтому сильного повышения эффективности не наблюдается. Аналогично, некоторые сложные формы наночастиц или плохо описанные экспериментальные геометрии трудно воспроизвести в симуляциях, что может объяснить несколько выбивающихся данных, где модели и измерения не совпадают. Автор отмечает, что если ультра‑малые частицы действительно проникают в ядро, то выброс электронов и химические реакции с молекулами клетки могут добавлять к эффекту. Тем не менее при многих реалистичных условиях лечения доминирует общий вывод: более сильное замедление протонов в зонах, богатых золотом, приводит к более сконцентрированному повреждению в ядре.
Что это значит для будущей онкологической помощи
Для неспециалистов основная мысль такова: золотые наночастицы в протонной терапии действуют не столько как крошечные электронные пушки, сколько как невидимые тормоза, превращающие быстрые, относительно мягкие протоны в более медленных и мощных «ударников» прямо там, где это наиболее важно — в ДНК опухолевой клетки. Прояснив этот механизм и показав, что он способен точно воспроизводить данные по выживанию клеток, исследование помогает разрешить долгосрочный конфликт между теорией и экспериментом. Это понимание может направить более разумный дизайн наночастичных препаратов — выбор материалов, размеров и концентраций, которые максимально усиливают замедление протонов вблизи ядер опухоли при минимальных побочных эффектах. В долгосрочной перспективе это может сделать протонную терапию более точной и мощной, улучшив результаты лечения пациентов с трудноизлечимыми опухолями.
Цитирование: Tabbakh, F. Resolving the contradiction between simulation and experimental results of using gold nanoparticles in proton therapy. Sci Rep 16, 8012 (2026). https://doi.org/10.1038/s41598-026-39621-1
Ключевые слова: протонная терапия, золотые наночастицы, радиочувствительность, лучевая терапия рака, наномедицина