Clear Sky Science · ru
Модифицированная модель широкого пучка для равномерно сканируемой терапии ионами углерода с учетом неоднородностей поля
Более точные лучи для лечения рака
Терапия ионами углерода — мощный вид радиационного лечения, который позволяет точно нацеливать опухоль и минимизировать повреждение соседних здоровых тканей. Чтобы воспользоваться этим преимуществом в полной мере, врачам и инженерам необходимо точно знать, где и как дозы излучения распределяются в теле. В этой статье представлен новый способ моделирования — математического описания — поведения одного распространенного типа пучка ионов углерода, который делает планы лечения более точными и надежными для пациентов.
Почему эти пучки важны
Многие из ранних центров терапии ионами углерода используют технику, называемую равномерным сканированием. Вместо того чтобы «рисовать» опухоль точка за точкой, система расширяет пучок в широкий, плоский участок, покрывающий всю мишень. Металлические устройства в линии пучка формируют и замедляют частицы так, чтобы наибольшая доза приходилась внутрь опухоли при одновременном сохранении соседних органов. Равномерное сканирование механически просто и надежно, что важно для загруженных клиник, но у этой техники есть недостаток: якобы «плоское» поле на самом деле не является идеально равномерным. Небольшие погрешности в магнитах и аппаратуре делают центр поля чуть более «горячим», чем края, и создают тонкие структуры в распределении пучка. Традиционное программное обеспечение планирования исходно предполагает почти идеально ровное поле и поэтому может неверно оценивать реальную дозу, получаемую пациентом.
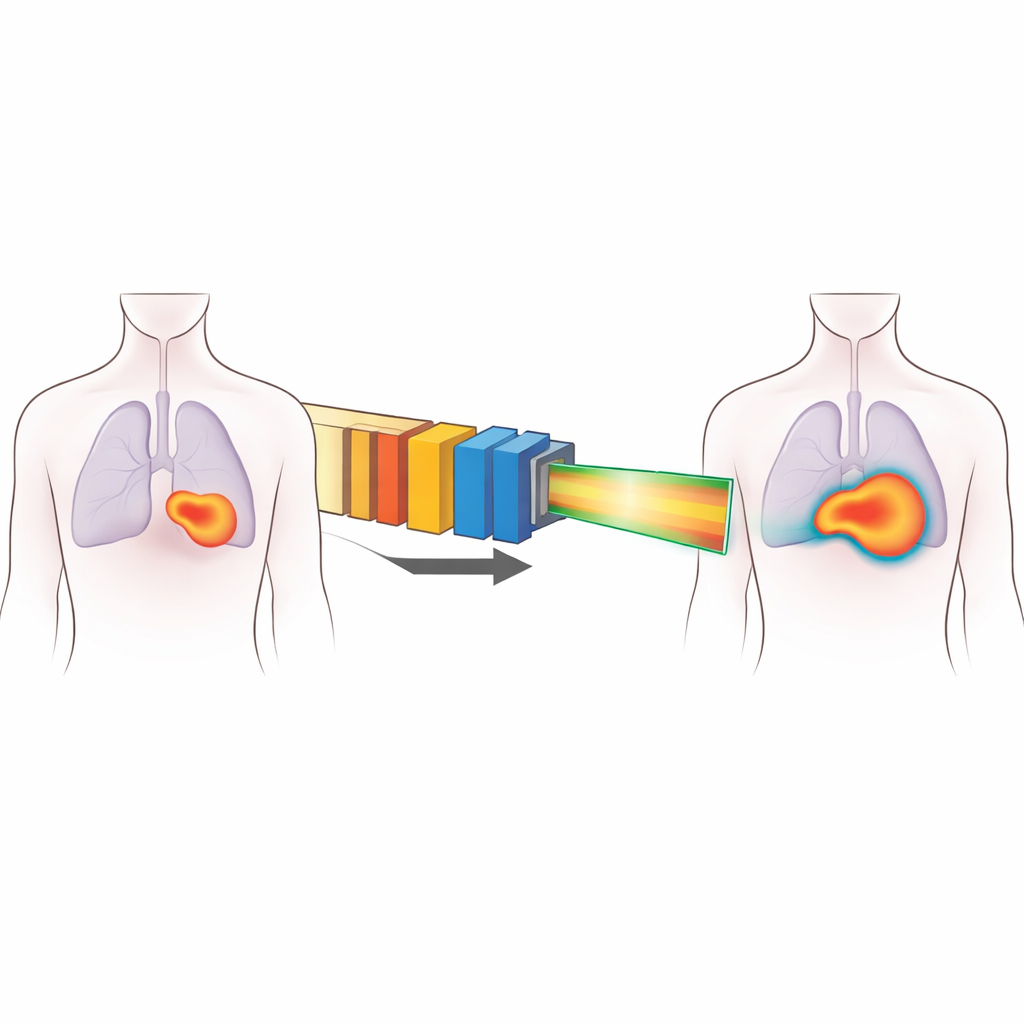
Более точная картина пучка
Чтобы исправить это, автор разработал модифицированную модель «широкого пучка», адаптированную для установок Heavy Ion Medical Machine (HIMM) в Китае. Вместо простого представления пучка как плоского блока с четкими краями, новая модель делит дозу на две части. Одна часть — центральное ядро — учитывает реальную, измеренную неравномерность поля по его ширине. Вторая часть использует пару перекрывающихся колоколообразных компонентов, чтобы описать мягкие «плечи» и длинные хвосты дозы у краев поля. Такой подход сохраняет общую структуру старых моделей, что позволяет интегрировать его в существующие системы планирования, но добавляет достаточную гибкость для воспроизведения того, что реально измеряется в клинике.
От измерений к рабочей модели
Построение этого улучшенного описания потребовало обширных измерений. Для каждой комбинации энергии пучка, настроек фильтра и клинически используемого размера поля команда регистрировала, как меняется доза с глубиной в воде и как она распространяется в боковом направлении на нескольких глубинах. Они также изучали ослабление пучка при прохождении через пластинчатые пластины, изменяющие его диапазон, и проверяли, влияет ли сужение поля с помощью коллимирующих пластин на общий выход. Эти данные затем загружались в автоматизированный компьютерный конвейер, который подгонял простые формулы под измерения и формировал полноценную модель пучка с минимальной ручной настройкой. Специальная двухмерная карта фиксировала характерную картину повышенной дозы в центре и пониженной — к краям для каждой конфигурации поля.
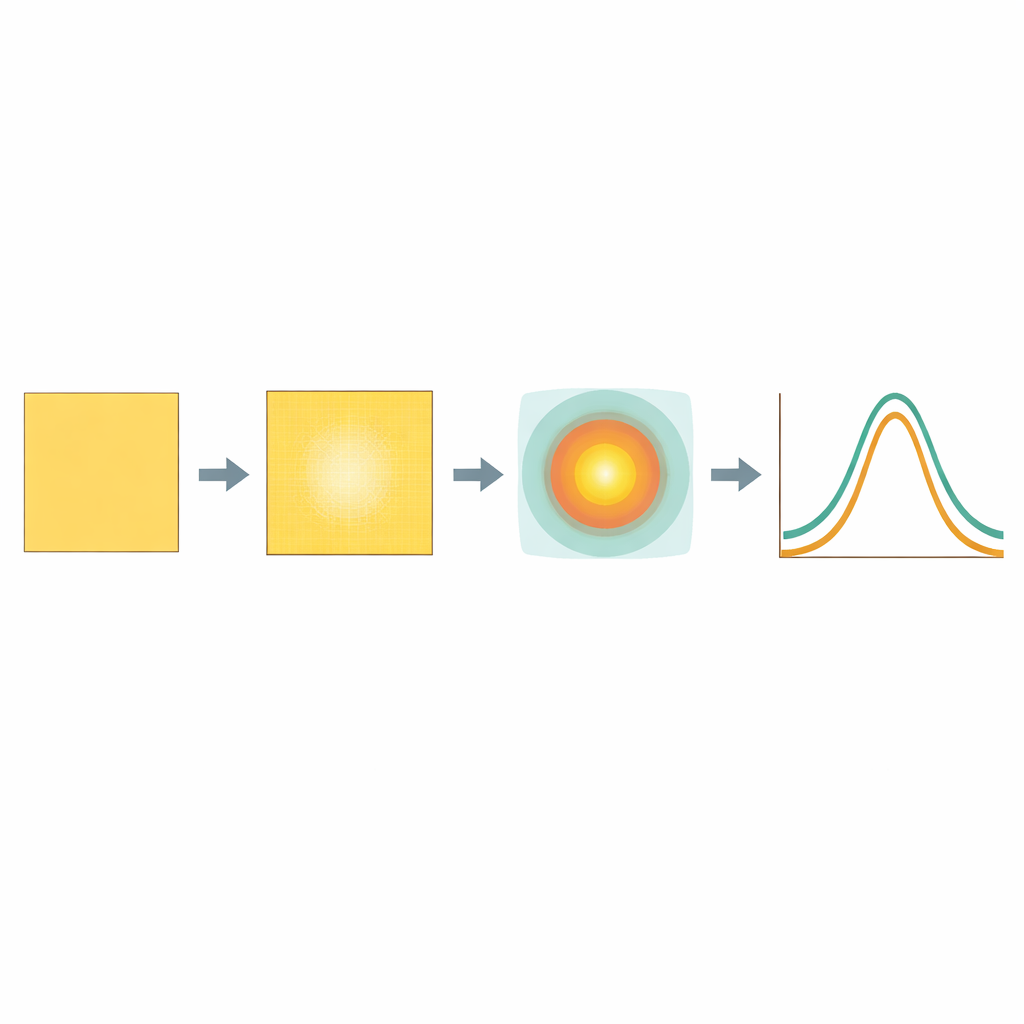
Проверка модели на практике
Ключевой вопрос — предсказывает ли новое описание то, что действительно происходит в ситуациях, приближающихся к лечению. Чтобы выяснить это, автор создал большой набор тестовых планов с разными размерами полей, формами и глубинами, включая более сложные схемы с индивидуальными компенсаторами и наклонными коллиматорами. Эти планы выполняли на трех различных наконечниках лечения в трех разных центрах, и полученные распределения дозы тщательно измеряли. Прогнозируемые и измеренные дозы сравнивали по стандартным клиническим критериям, учитывающим как разницу в дозе, так и пространственное соответствие. По всем планам и на всех трех машинах модифицированная модель последовательно соответствовала принятым критериям, тогда как старая, более простая модель часто давала сбои. Исследование также показало, что единый числовой «клинический фактор» может согласовать биологическую эффективность пучков HIMM с хорошо установленными эталонными данными из Японии.
Что это значит для пациентов
Проще говоря, эта работа дает больницам, использующим равномерное сканирование пучков ионов углерода, более правдивое представление о том, что их аппаратура действительно доставляет. Явно моделируя реальную неравномерность пучка и детализированный спад на его краях, планирование лечения может лучше уравновешивать покрытие опухоли и защиту здоровых тканей. Улучшенное совпадение расчетов и измерений в нескольких центрах указывает на то, что этот подход достаточно устойчив для рутинного использования. В результате пациенты, проходящие терапию ионами углерода в этих учреждениях, могут получить планы лечения, которые лучше отражают реальную дозу внутри их тела.
Цитирование: Xia, Y. A modified broad beam model for uniformly scanned carbon ion therapy accounting for field inhomogeneities. Sci Rep 16, 8793 (2026). https://doi.org/10.1038/s41598-026-39619-9
Ключевые слова: терапия ионами углерода, моделирование дозы облучения, равномерно сканируемые пучки, лучевая терапия рака, системы планирования лечения