Clear Sky Science · ru
Геномная и in vitro характеристика двух лизирующих бактериофагов, инфицирующих многолекарственно-устойчивый штамм Erwinia AnSW2-5
Почему бактерии, губящие посевы, важны для всех
По всему миру фермеры борются с бактериальными болезнями, которые гниют фрукты, усыхают листья и разрушают урожай. Многие из этих вспышек вызваны штаммами, которые больше не реагируют на обычные антибиотики, что угрожает как продовольствию, так и средствам к существованию. В этом исследовании рассматривается обещающая альтернатива: использование вирусов, поражающих бактерии — бактериофагов — для безопасного нейтрализования особо упорного фитопатогена, обнаруженного в почве, связанной с интенсивным применением антибиотиков.
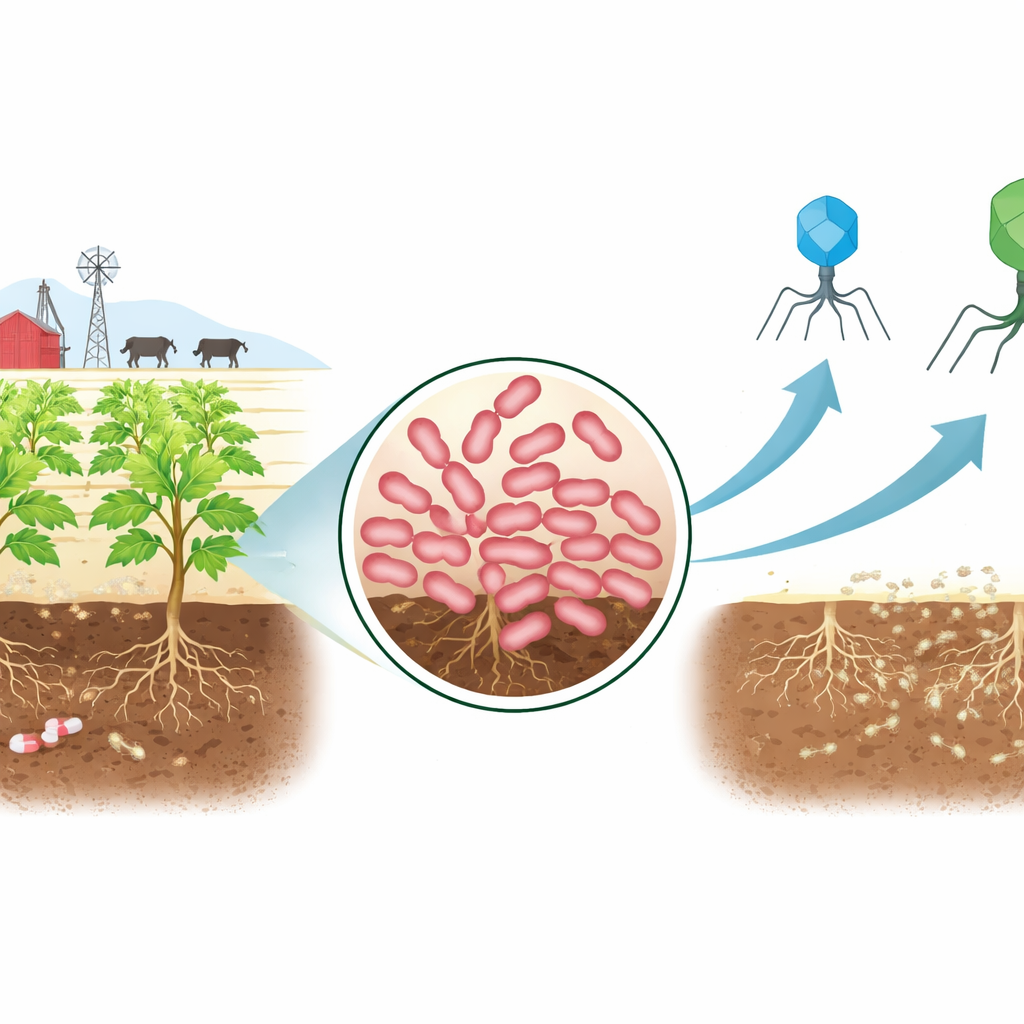
Новый опасный захватчик на ферме
Исследователи начали с отбора проб почвы в загоне для крупного рогатого скота, куда попадали фекалии животных и антибиотики. Из этой сложной среды они выделили штамм Erwinia — группу бактерий, включающую печально известных возбудителей fire blight у яблонь и мягкой гнили у картофеля. Испытания показали, что штамм, названный AnSW2-5, выдерживает несколько крупных семейств антибиотиков, включая препараты широкого спектра действия. Генетический анализ объяснил причину: в его ДНК обнаружены известные гены резистентности и мощные молекулярные насосы, выбрасывающие антибиотики из клетки. Одновременно сравнения геномов показали, что этот штамм отличается от ранее описанных видов Erwinia, что делает его полезной моделью для изучения методов контроля новых трудноизлечимых фитопатогенов.
Два крошечных хищника с разными сильными сторонами
Чтобы найти естественных врагов этой многолекарственно-устойчивой бактерии, команда обратилась к пресной воде с того же участка и обогатила её фагами, способными инфицировать AnSW2-5. Они выделили двух перспективных кандидатов, обозначенных как P-A и P-K. Под электронным микроскопом P-A выглядел компактным с коротким хвостом — конструкция, связанная с быстрым и прямым инфицированием. P-K, напротив, имел более длинный сократительный хвост со сложной базовой структурой, что указывает на более мощный механизм проникновения в хозяина. Секвенирование их геномов показало, что оба фага строго лизируют: они вторгаются, реплицируются и разрывают клетку, а не интегрируются в бактериальную ДНК. Тем не менее их генетические наборы значительно отличаются — упрощённый геном P-A поддерживает быстрый захват, тогда как более крупный геном P-K кодирует более сложные структурные и репликационные механизмы.
Как действует вирусная команда
Когда учёные отслеживали жизненный цикл каждого фага в лаборатории, они обнаружили, что P-A действует быстро: ему требуется всего около 20 минут, прежде чем начинают появляться новые вирусные частицы, и каждая инфицированная бактерия выпускает примерно 70 потомков. P-K действует дольше — около 35 минут до начала продуктивной фагогенезы — но каждая инфицированная клетка даёт примерно 110 новых частиц. В тестах со смешанными культурами, где бактерии и фаги выращивали вместе в течение трёх дней, оба фага по отдельности замедляли рост бактерий, но не предотвращали его полностью. Со временем бактерии восстановили численность, что отражает появление устойчивых выживших. Однако при сочетании P-A и P-K в одном коктейле популяция бактерий сократилась более чем на 80% и оставалась подавленной на весь 72-часовой эксперимент.
Не дать резистентности укрепиться
Одним из наиболее заметных результатов было то, как пара фагов повлияла на появление устойчивых мутантов. При воздействии только P-A или только P-K небольшая доля бактерий — примерно от одной к миллиону до одной к десяти миллионам — сумела избежать и продолжить рост несмотря на фаговую атаку. Но при совместном применении обоих фагов устойчивые колонии стали настолько редкими, что оказались ниже предела обнаружения эксперимента. Это указывает на то, что два вируса, вероятно, прикрепляются к разным мишеням на поверхности бактерии или поражают клетку комплементарными способами. Чтобы одна клетка выжила, ей пришлось бы одновременно преодолеть оба механизма — событие с чрезвычайно низкой вероятностью. В практическом плане это делает коктейль гораздо более устойчивым к эволюционным ухищрениям, которые часто делают антибиотики бесполезными.
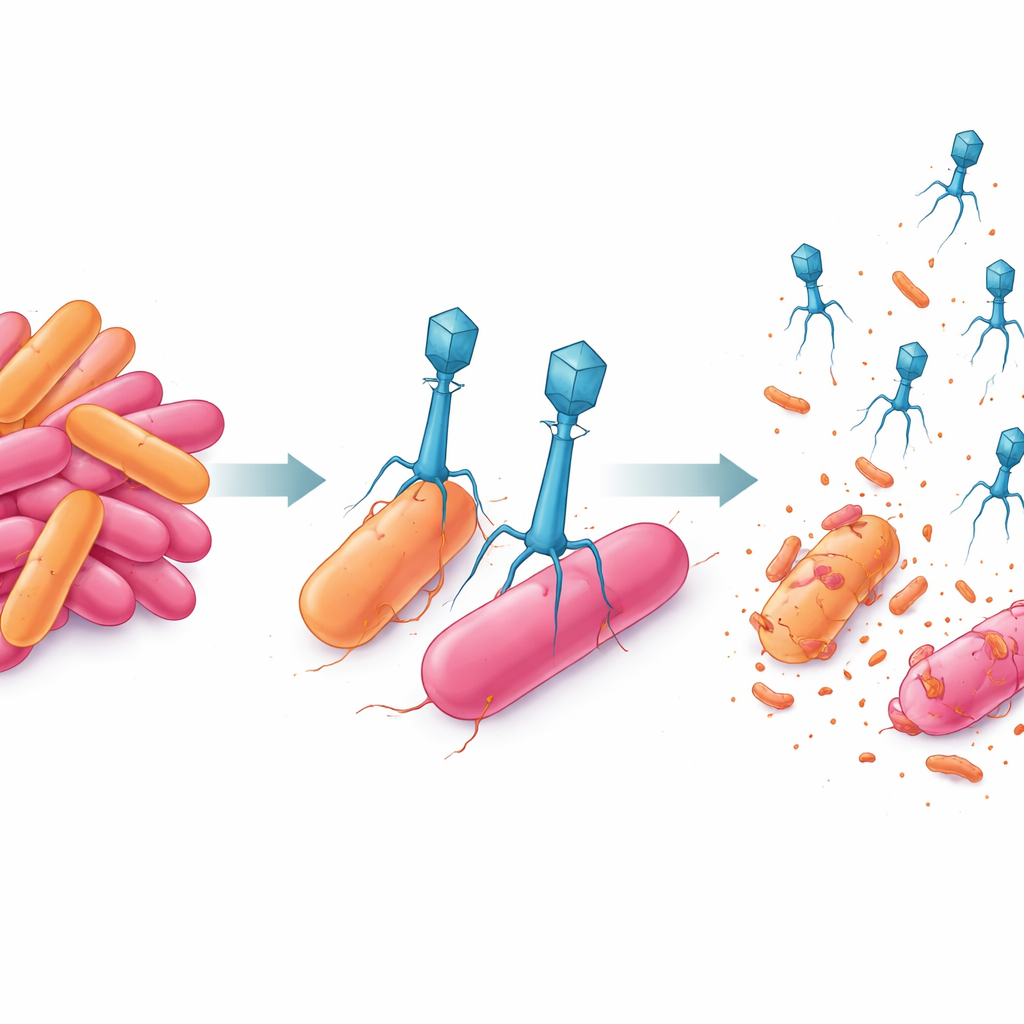
Что это может значить для будущих урожаев
В совокупности работа показывает, что тщательно подобранные пары бактериофагов могут не только снижать численность опасных фитобактерий, но и ограничивать их способность эволюционировать резистентность. Комбинируя быстро действующий фаг с тем, который производит большее число потомков, исследователи создали вирусную команду, удерживавшую многолекарственно-устойчивый штамм Erwinia под контролем в течение нескольких дней и не допустившую обнаруживаемых вариантов-уклонистов. Хотя эти испытания проводились в лабораторных условиях, а не в садах или полях, они указывают на будущее, в котором таргетные фаговые смеси станут частью стандартного интегрированного управления вредителями, помогая фермерам защищать культуры с гораздо меньшей зависимостью от традиционных антибиотиков.
Цитирование: Baek, K., Goh, J. & Choi, A. Genomic and in vitro characterization of two lytic bacteriophages infecting multidrug-resistant Erwinia sp. strain AnSW2-5. Sci Rep 16, 8172 (2026). https://doi.org/10.1038/s41598-026-39563-8
Ключевые слова: биоконтроль бактериофагами, бактериальные болезни растений, антибиотикорезистентность в сельском хозяйстве, фаговая терапия Erwinia, фаговые коктейли