Clear Sky Science · ru
Структурное моделирование и докинг-анализ канонических и новых миссенс-мутаций, связанных с резистентностью, в штаммах Escherichia coli из Судана
Почему это важно для повседневного здоровья
Инфекции, устойчивые к антибиотикам, уже не редкие медицинские курьёзы; они всё чаще ставят под угрозу обычные процедуры — лечение мочевых инфекций, операции и уход в реанимации. В этом исследовании подробно изучают штаммы Escherichia coli из Судана и задают конкретный вопрос: как небольшие генетические изменения в белках бактерий меняют действие привычных антибиотиков? Используя компьютерное структурное моделирование вместо дорогих лабораторных экспериментов, авторы выявляют скрытые паттерны резистентности, которые стандартные тесты и глобальные базы данных могут пропускать — особенно в условиях с ограниченными ресурсами, где резистентность растёт быстрее всего. 
Заглядывая в «инструментарий» бактерии
Исследователи сосредоточились на «миссенс»-мутациях — однонуклеотидных изменениях, которые заменяют одну аминокислоту в белке на другую. Они проанализировали полные геномы 55 изолятов E. coli, собранных в Судане, и детально рассмотрели белки, являющиеся прямыми мишенями основных классов антибиотиков, включая фторхинолоны, макролиды и рифампицин. К таким целям относятся ферменты, изменяющие укладку ДНК (гираза и топоизомераза IV), рибосома, отвечающая за синтез белка, и РНК-полимераза. Из 71 обнаруженной мутации 19 были отмечены несколькими предикторами как вероятно нарушающие функцию белка, и, что примечательно, большинство этих вариантов, по-видимому, ранее не были занесены в глобальные базы данных резистентности.
Новые «проблемные зоны» в привычных мишенях
Часть наиболее значимых изменений сосредоточилась в рибосомальном белке L22, который участвует в формировании туннеля, через который выходят вновь синтезированные белки. Эта область также служит сайтом прикрепления для макролидных антибиотиков, таких как эритромицин. В исследовании выявлен плотный набор ранее не описанных мутаций в L22, многие из которых встречались в одном штамме; они располагаются вдоль туннеля и в точках контакта с рибосомной РНК. Компьютерные анализы показали, что несколько из этих изменений дестабилизируют локальную структуру или делают её более гибкой, что потенциально изменяет форму туннеля и снижает плотность прилегания молекул макролидов. В то же время в белках, участвующих в обработке ДНК — ParC и ParE — и в РНК-полимеразе обнаружились знакомые «канонические» мутации резистентности, подтверждая, что суданские штаммы разделяют некоторые глобальные маркеры резистентности, но при этом содержат и собственные локальные варианты.
Как изменение формы ослабляет удержание антибиотика
Команда пошла дальше списков последовательностей и изучила, как эти мутации могут изменить трёхмерное соответствие между антибиотиками и их мишенями. С помощью молекулярного докинга они сравнили связывание различных препаратов с нормальными и мутировавшими белками. Для топоизомеразы IV (ParC) ключевые мутации вблизи сайта контакта с лекарством существенно ослабляли предсказанное связывание фторхинолона тровафлоксацина, что отражает более слабое удержание на стыке фермент–ДНК–лекарство. В родственном белке ParE мутации умеренно снижали связывание новобиоцином. Напротив, новая мутация в гиразе GyrA, по-видимому, дестабилизировала структуру фермента, не меняя заметно силы связывания фторхинолона моксiflоксцина, что указывает на то, что резистентность иногда появляется за счёт тонких нарушений работы фермента, а не лишь за счёт прямого вытеснения препарата. 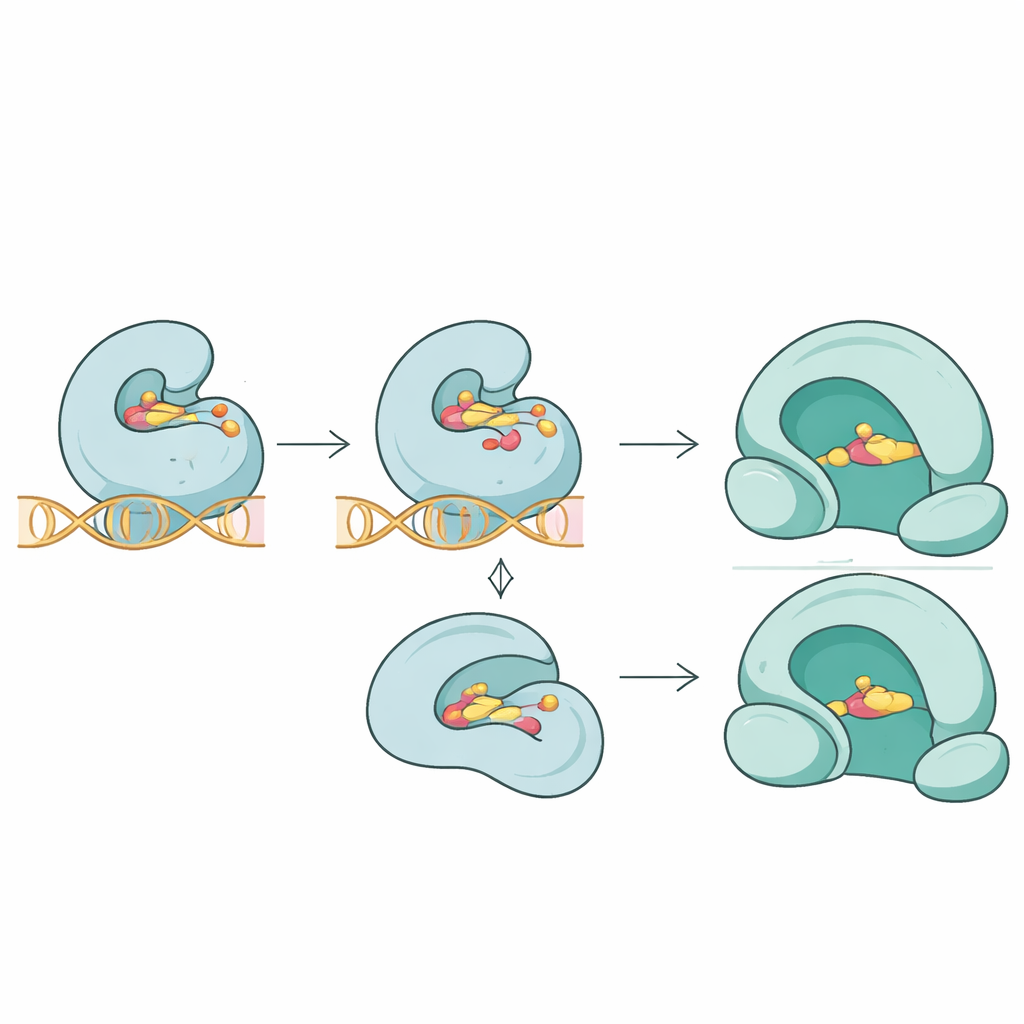
Разные эффекты для разных препаратов
Не все мутации оказывали одинаковое влияние. Классические изменения, дающие резистентность к рифампицину в белке РНК-полимеразы RpoB, мало нарушали связывание нового структурно отличного ингибитора, таргетирующего соседний участок, что говорит о том, что будущие препараты можно спроектировать так, чтобы обходить существующие механизмы резистентности. Для рибосомного белка L22 докинговые исследования с эритромицином показали смешанные результаты: некоторые мутации ослабляли связывание, некоторые мало влияли, а одна даже немного улучшала предсказанное прилегание. Эти результаты подчёркивают, что резистентность редко бывает чёрно‑белой; каждая мутация смещает стабильность белка, его гибкость и связывание с препаратом в ту или иную сторону, а итоговый эффект на лечение зависит от того, как эти изменения комбинируются в живой бактериальной клетке.
Что это значит для пациентов и надзора
С точки зрения практической значимости ключевое послание в том, что бактерии в таких регионах, как Судан, развивают резистентность как по хорошо известным, так и по менее изученным путям. Известные пути включают классические мутации, уже отслеживаемые международными программами, но это исследование показывает: многие дополнительные, локально обогащённые мутации также могут вносить вклад в ослабление действия антибиотиков более тонкими способами. Нанесение этих изменений на подробные белковые структуры даёт короткий список мутаций, которые следует проверить в лаборатории и учесть в региональных диагностических панелях. Практически это означает, что грамотное компьютерное моделирование может помочь странам с ограниченными лабораторными возможностями лучше отслеживать появляющуюся резистентность, что в конечном счёте поддержит более надёжный выбор терапии и вдохновит разработку препаратов, опережающих бактериальную эволюцию.
Цитирование: Sage, E.E., Ibrahim, S.A.E., Firdaus-Raih, M. et al. Structural modeling and docking analysis of canonical and novel resistance-associated missense mutations in Sudanese Escherichia coli. Sci Rep 16, 8995 (2026). https://doi.org/10.1038/s41598-026-39491-7
Ключевые слова: антибактериальная резистентность, Escherichia coli, миссенс-мутации, структурная биоинформатика, Судан