Clear Sky Science · ru
Комплексная оценка эффективности BMIA-12A — системы для количественного анализа клеток костного мозга в образцах нормального и гематологически поражённого материала
Почему важно подсчитывать клетки костного мозга
При постановке диагноза кровных онкологий, таких как лейкемия или множественная миелома, врачи тщательно изучают мазки костного мозга под микроскопом и вручную пересчитывают тысячи клеток. Эта медленная, кропотливая работа влияет на судьбоносные решения по диагнозу, лечению и прогнозу. В статье представлена и строго протестирована новая система на базе искусственного интеллекта BMIA-12A, предназначенная для автоматизации значительной части подсчёта — что потенциально делает результаты быстрее, более воспроизводимыми и менее зависящими от конкретного эксперта, читающего препарат.
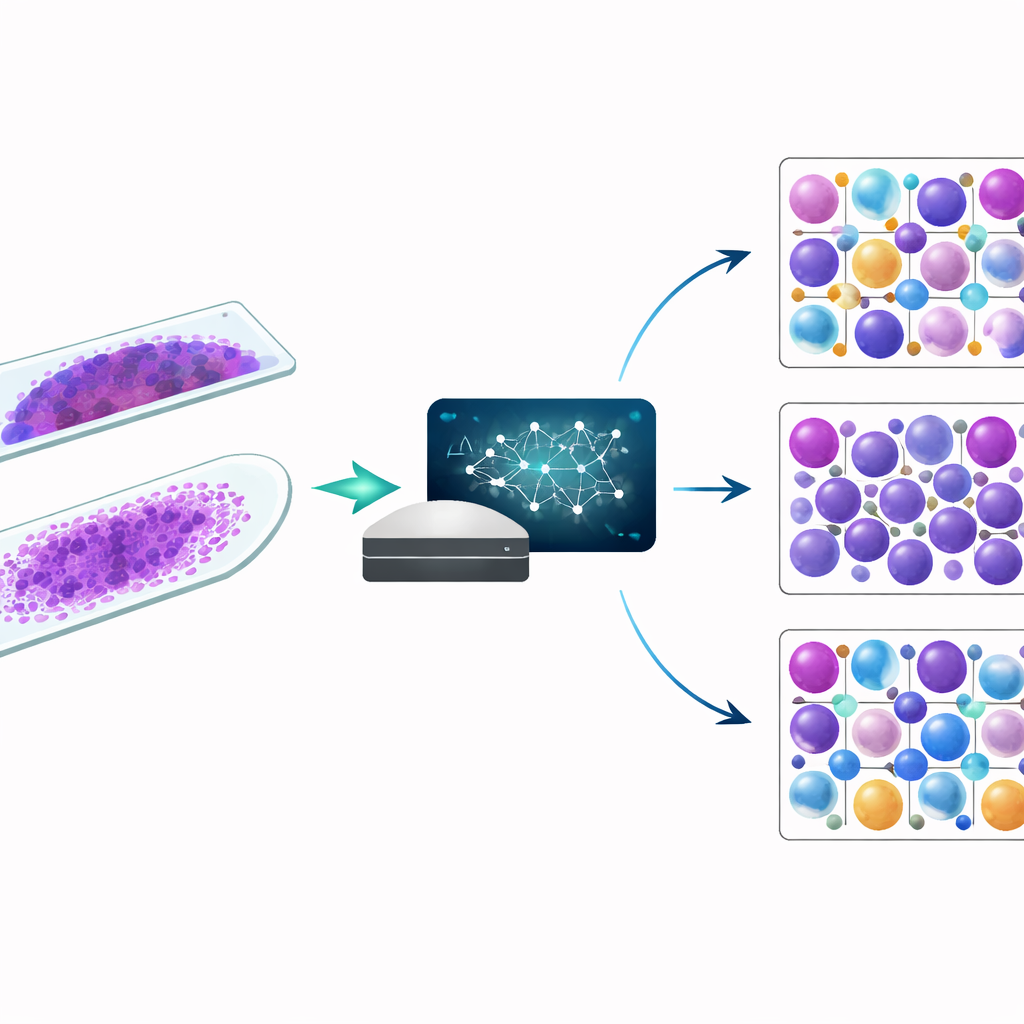
Новый цифровой помощник для микроскопа
Система BMIA-12A обрабатывает оцифрованные изображения мазков костного мозга и с помощью алгоритмов глубокого обучения распознаёт и классифицирует клетки по 16 основным типам, включая ранние «бласты», которые важны для определения лейкемий, и плазматические клетки, ключевые при множественной миеломе. В исследовании проанализировали 298 мазков костного мозга от 149 человек, охватив нормальные образцы, нарушения плазматических клеток и несколько форм острых лейкозов. Для каждого мазка сравнивали три подхода: полностью автоматизированный подсчёт ИИ, подсчёт ИИ с проверкой и коррекцией специалистами, и традиционный ручной подсчёт под световым микроскопом. Также исследовали два распространённых метода приготовления препаратов — «вэ́дж» (wedge) и «сквош» (squash), чтобы понять, как качество препарата влияет на работу ИИ.
Насколько система распознаёт нормальные клетки
В костном мозге людей без злокачественных процессов система ИИ показала впечатляющие результаты. Она правильно классифицировала примерно 95% из почти 38 000 клеток в обоих типах препаратов, при этом для 14 из 16 типов клеток чувствительность (recall) превышала 90%. Вэ́дж-препараты — где материал равномерно распределён по стеклу — дали немного лучшую точность для ключевых диагностических клеток, таких как плазматические клетки, бласты и редкие базофилы. Большинство ошибок ИИ случалось между клеточными типами, которые выглядят очень похоже, например между соседними стадиями созревания лейкоцитов или между реактивными лимфоцитами и бластами. При сравнении частот появления каждого типа клеток в целом по образцам результаты ИИ и экспертной ревизии хорошо совпадали, тогда как традиционные ручные подсчёты были заметно более вариабельны, что отражает субъективность и ограниченность выборки при ручной работе.
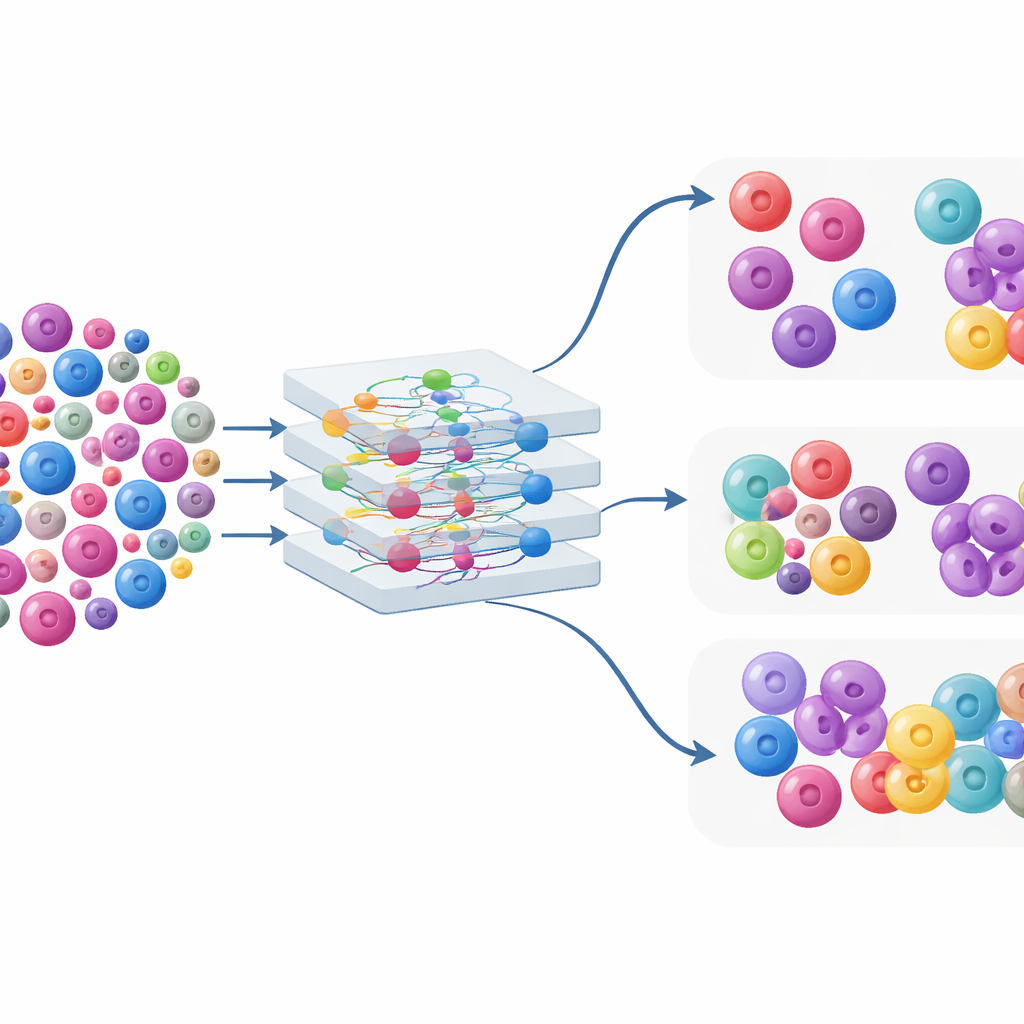
Что происходит при миеломе и лейкозе
В случаях заболеваний производительность системы была более неоднородной. При нарушениях плазматических клеток ИИ демонстрировал высокую точность в идентификации плазматических клеток, но пропускал примерно четверть из них, особенно при множественной миеломе, где костный мозг заполнен атипичными плазматическими клетками, отличающимися по форме от учебных образцов, на которых обучался алгоритм. В результате ИИ склонен был недооценивать процент плазматических клеток по сравнению с ручными и экспертно скорректированными подсчётами, особенно при высокой нагрузке опухоли. Похожая картина наблюдалась при острых лейкемиях: в целом ИИ неплохо выявлял бласты, особенно на вэ́дж-препаратах, но часто относил атипичные бласты к похожим категориям, таким как моноциты или ранние миелоидные клетки. Ручные подсчёты последовательно давали более высокие проценты бластов, чем либо автоматизированные, либо экспертно откорректированные цифровые результаты, причём наибольшие расхождения отмечались в некоторых генетических подтипах, например при ОМЛ с мутацией NPM1 и B‑клеточном ОЛЛ с фузией BCR::ABL1, где морфология бластов особенно необычна.
Почему важны метод приготовления препарата и генетика
Исследование показало, что способ приготовления мазка и молекулярно‑генетические особенности заболевания оба влияют на работу ИИ. В сквош‑препаратах, где фрагменты костного мозга аккуратно сдавливают между стеклами, возникают искажения, размывающие тонкие ядерные детали, что усиливает путаницу между соседними стадиями созревания и между бластами и другими молодыми клетками. Вэ́дж‑препараты лучше сохраняют структуру, обеспечивая более высокую чувствительность и точность, поэтому авторы рекомендуют их как стандартный формат для анализа с поддержкой ИИ. С биологической стороны, бласты при определённых генетических подтипах часто имеют характерные, порой деформированные ядерные формы или другие атипичные признаки. Поскольку современные системы ИИ обычно обучаются преимущественно на нормальных клетках, эти неопластические варианты могут «приписываться» к ближайшей нормальной категории, что приводит к систематическому занижению оценки опухолевого поражения у тех пациентов, для которых точные пороговые значения особенно важны.
Как это меняет работу лаборатории сегодня
В совокупности результаты позволяют считать, что BMIA-12A уже достаточно надёжен, чтобы служить мощным инструментом скрининга и сортировки, особенно для нормальных образцов костного мозга и рутинных дифференциальных подсчётов. Он способен быстро анализировать десятки тысяч клеток на одном препарате и даёт стабильные, воспроизводимые результаты, которые хорошо согласуются с экспертной оценкой. В то же время четкие и иногда существенные расхождения с ручными подсчётами при лейкемиях и плазмоцитарных неоплазмах показывают, что для окончательной интерпретации по‑прежнему необходимы люди‑специалисты, особенно вблизи диагностических порогов и у генетически определённых высокорисковых подтипов. Авторы подчёркивают, что лаборатории, внедряющие такие инструменты ИИ, должны тщательно валидавать их для своих методов приготовления препаратов и выстраивать рабочие процессы так, чтобы ИИ давал объективную отправную точку, которую эксперты уточняют, а не заменял экспертное суждение.
Цитирование: Kim, H.N., Lee, J.H., Jung, Y. et al. Comprehensive performance assessment of the BMIA-12 a system for bone marrow cell quantification in normal and hematological malignancy samples. Sci Rep 16, 8798 (2026). https://doi.org/10.1038/s41598-026-39443-1
Ключевые слова: искусственный интеллект в гематологии, цитология костного мозга, диагностика лейкемии, множественная миелома, цифровая микроскопия