Clear Sky Science · ru
Генно-ориентированная аналитическая модель обучения для точной диагностики рака молочной железы
Почему это исследование важно для пациентов и их семей
Рак молочной железы в настоящее время является наиболее часто диагностируемым видом рака у женщин во всем мире, и пациенты с внешне похожим заболеванием могут иметь весьма разные исходы. В этом исследовании показано, как сочетание паттернов в тысячах генов и тщательно спроектированной системы искусственного интеллекта может помочь врачам более надежно определять, есть ли у пациента рак и насколько он выражен — используя только реальные данные пациентов и компактный набор ключевых генов.
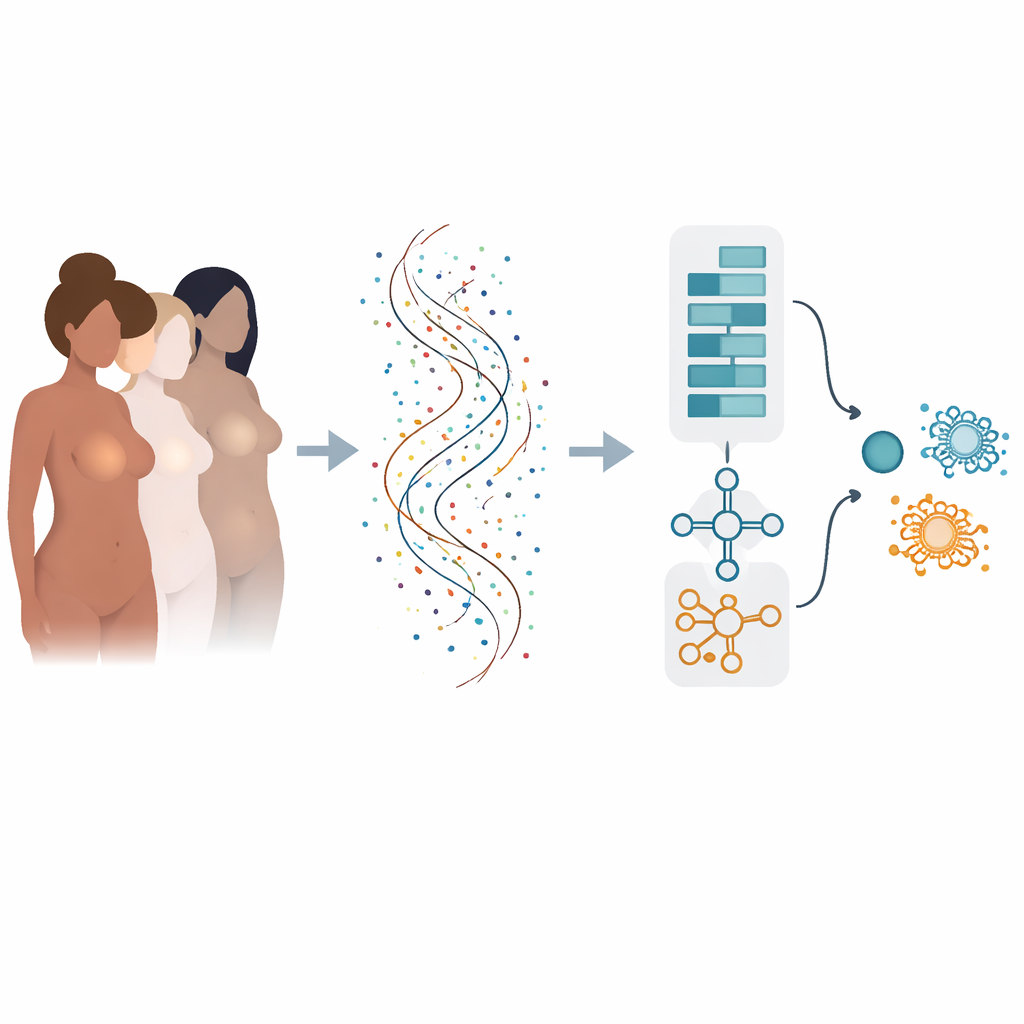
От множества факторов риска к языку генов
Риск развития рака молочной железы формируется под влиянием множества факторов: наследственных изменений в генах, гормонов, массы тела, образа жизни и других. Как только опухоль возникает, её поведение определяется тем, какие гены «включены» или «выключены» в каждой ткани. Современные методы секвенирования умеют измерять активность десятков тысяч генов одновременно, но превратить этот океан чисел в четкие ответы «да» или «нет» для диагностики и прогноза непросто. Традиционные вычислительные подходы часто рассматривают гены поодиночке и могут не замечать, как группы генов действуют совместно, либо демонстрируют хорошую работу только на одном наборе данных и дают сбои при проверке на других выборках.
Обучение двойного «мозга» распознавать генетические паттерны
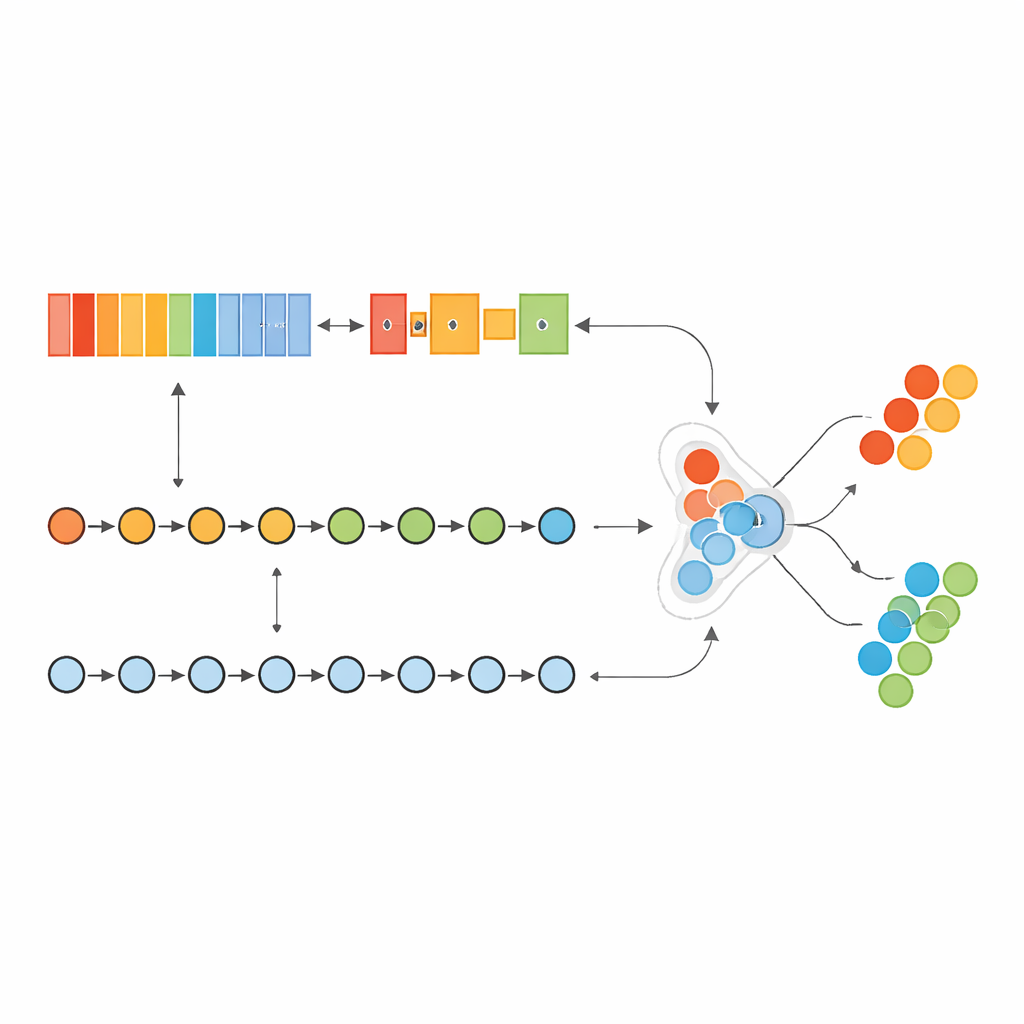
Авторы создали «гибридную» модель глубокого обучения, которая действует как два специализированных мозга, работающих вместе. Одна часть, вдохновлённая анализом изображений, просматривает упорядоченный список генов, чтобы обнаруживать локальные паттерны — кластеры генов, совокупная активность которых сигнализирует о наличии рака. Другая часть рассматривает те же гены как последовательность, изучая, как ранние «водительские» гены и последующие «вторичные» гены влияют друг на друга вдоль списка. Комбинируя эти два представления, модель способна улавливать как краткодействующие, так и дальнодействующие взаимосвязи в генетическом отпечатке опухоли.
Нахождение стабильного ядра сигнальных генов
Вместо того чтобы подавать в модель все 17 815 измеренных генов, команда разработала строгий «безпротечный» конвейер отбора, чтобы оставить только наиболее информативные. Используя стандартную меру корреляции в повторяющихся циклах перекрёстной проверки, они многократно ранжировали гены по тому, насколько сильно их активность коррелировала со статусом рака. Затем оставляли лишь те гены, которые стабильно попадали в верхние позиции во всех тренировочных разбиениях, что привело к устойчивому сигнатурному набору из 236 генов. Исследователи также сопоставили, как эти гены взаимодействуют друг с другом, показав, что многие образуют плотно связанные сети, связанные с ростом опухоли, метаболизмом, иммунитетом и окружающей тканевой средой — доказательство того, что выбранный набор отражает реальную биологию, а не случайный шум.
Проверка модели на практике
Гибридная система была обучена и настроена на образцах рака молочной железы из базы The Cancer Genome Atlas, а затем протестирована на полностью отдельном наборе данных METABRIC. Чтобы учесть тот факт, что образцов рака намного больше, чем нормальных образцов, авторы не создавали искусственные данные; вместо этого они скорректировали степень «веса» ошибок для более редкого класса. После автоматического поиска оптимальных параметров модель достигла почти идеальных показателей на основном наборе данных, правильно отмечая почти все случаи рака и допуская практически не было ложных срабатываний. Важно, что производительность оставалась крайне высокой и очень стабильной даже при применении модели к внешней когорте METABRIC, что говорит о том, что подход может обобщаться вне границ одного исследования или больницы.
Что это означает для будущей помощи пациентам
Проще говоря, эта работа представляет тонко настроенную двухчастную ИИ-систему, которая читает компактный код из 236 генов, чтобы с выдающейся точностью и стабильностью отличать раковые от нераковых образцов молочной железы, даже в условиях шума. Хотя текущее исследование рассматривает только активность генов и использует ретроспективные данные пациентов, его методы закладывают основу для будущих инструментов, которые могли бы объединять несколько типов данных — например, изображения тканей и дополнительные молекулярные уровни — и предоставлять понятные объяснения того, какие гены определяют каждое предсказание. После дальнейшей валидации в проспективных клинических исследованиях такая система могла бы стать универсальной основой для прецизионной диагностики рака молочной железы, помогая врачам подбирать лечение на основе генетической «подписи» опухоли каждого пациента.
Цитирование: Hesham, F., Abbassy, M.M. & Abdalla, M. Gene driven analytical learning model for accurate breast cancer diagnosis. Sci Rep 16, 8155 (2026). https://doi.org/10.1038/s41598-026-39430-6
Ключевые слова: диагностика рака молочной железы, экспрессия генов, глубокое обучение, CNN-BiLSTM, прецизионная онкология