Clear Sky Science · ru
Открытие потенциальных противовирусных соединений и ускорение разработки препаратов против вируса оспы обезьян
Почему это исследование важно именно сейчас
Оспа обезьян, ныне часто называемая mpox, превратилась из редкой тропической инфекции в глобальную проблему: в последние годы вспышки регистрировались на нескольких континентах. В отличие от COVID-19, до сих пор не создано ни одного препарата, разработанного специально для остановки этого вируса. В этом исследовании используются современные компьютерные инструменты для поиска новых малых молекул, которые могли бы лишить вирус его ключевого преимущества: способности скрываться от нашей иммунной системы. Если эти кандидатные соединения подтвердятся в лаборатории, они могут стать отправной точкой для нового класса противовирусных препаратов.
Как вирус прячетcя от нашей защиты
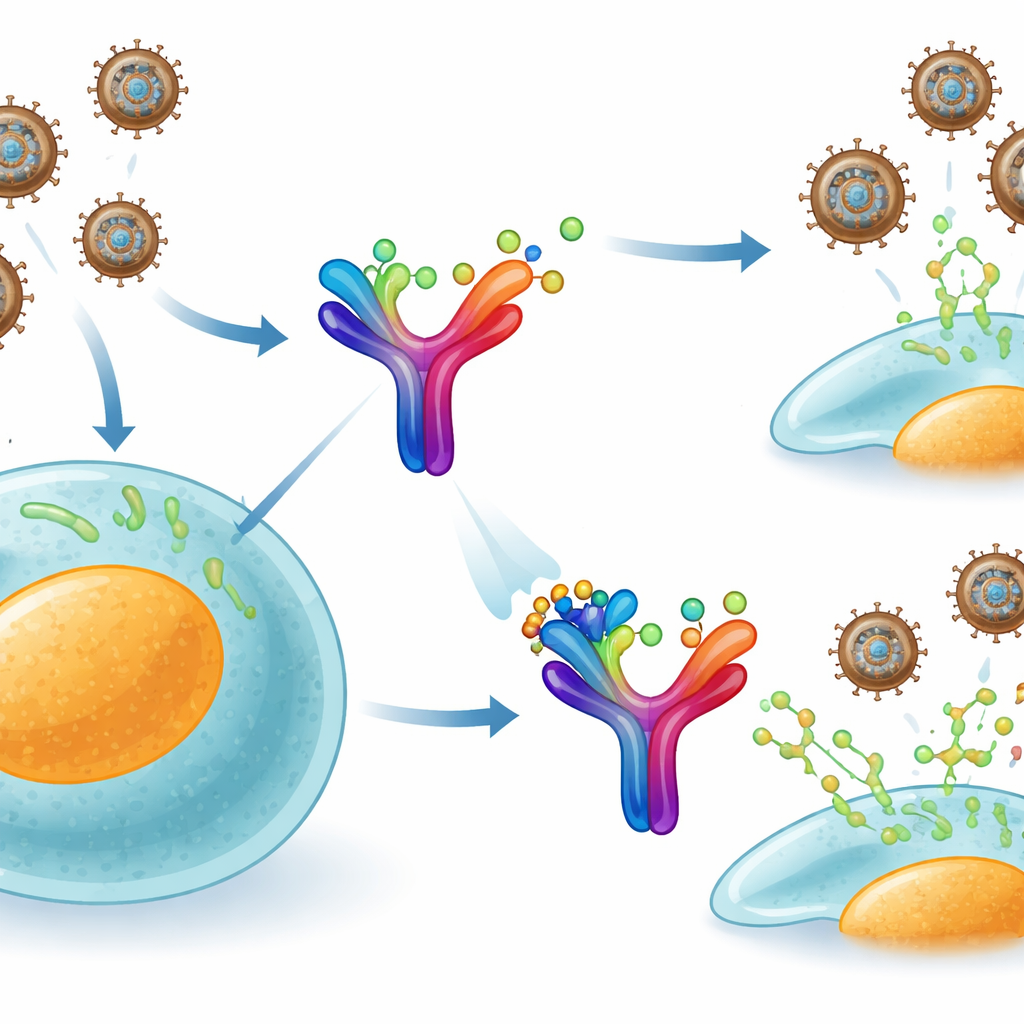
Оспа обезьян относится к той же широкой семье, что и оспа, и использует хитрый трюк, чтобы ускользнуть от иммунной системы. Наши клетки выделяют сигнальный белок, называемый интерфероном-гамма, который обычно предупреждает соседние клетки и включает противовирусные механизмы. Однако вирус вырабатывает собственный секретируемый белок B8R, который плавает вне заражённых клеток. B8R тесно имитирует наш собственный рецептор интерферона-гамма и перехватывает эти иммунные сигналы до того, как они достигнут их настоящей цели. По сути, он действует как губка, впитывая сигналы тревоги организма и препятствуя полной противовирусной реакции.
Использование компьютеров для разработки более умных терапий
Традиционная разработка лекарств может занимать многие годы и требовать огромных ресурсов. В данном случае исследователи обращаются к вычислительному дизайну лекарств, чтобы ускорить процесс. Поскольку экспериментальная трёхмерная структура белка B8R отсутствовала, сначала они использовали инструменты на базе AlphaFold для предсказания его атомной формы и тщательно проверили качество полученной модели. Имея надёжную 3D-структуру, они виртуально просеяли химическую библиотеку из 5000 малых молекул. Правила, описывающие свойства «таблеткоподобного» лекарства (такие как размер, форма и растворимость), применялись для отсева неподходящих кандидатов, в результате чего для детального тестирования против модели белка B8R осталось 2890 перспективных соединений.
Нахождение перспективного химического «ключа»
Следующим шагом было выяснить, какие молекулы смогут плотно войти в важный карман на поверхности B8R, где он обычно взаимодействует с интерфероном-гамма. Команда использовала молекулярный докинг — метод, который перебирает миллиарды возможных положений молекулы в кармане белка и оценивает, насколько прочно она будет связываться. Выделились три основных кандидата, каждый из которых, по предсказаниям, образует прочные взаимодействия с ключевыми аминокислотами в кармане. Один из соединений особенно показал наибольшую энергию связывания и установил несколько стабилизирующих контактов с критическими остатками, что свидетельствует о его высокой эффективности в блокировании активности B8R.
Наблюдение за движением молекул во времени
Белки и лекарственные молекулы не являются жёсткими; они движутся, изгибаются и «дышат» в водной среде. Чтобы учесть это, исследователи провели длительные молекулярно-динамические симуляции — виртуальные «фильмы» продолжительностью сотни наносекунд — чтобы увидеть, как каждая пара белок–соединение ведёт себя со временем. Эти симуляции показали, что наилучшее соединение оставалось глубоко закопанным в кармане B8R, при этом белок слегка подстраивался вокруг него, оставаясь структурно стабильным. В отличие от него, другие два соединения больше смещались, уходили в альтернативные карманы или демонстрировали большие флуктуации, что указывает на более слабое или менее надёжное связывание. Дополнительные анализы гибкости, энергии и крупномасштабных движений подтверждали тот же вывод: одно соединение последовательно формировало наиболее стабильный и энергетически выгодный комплекс.
Что это может означать для будущих методов лечения
Исследование не претендует на открытие готового препарата, и эксперименты на клеточных или животных моделях ещё не проводились. Вместо этого оно предоставляет сильную, основанную на данных отправную точку: конкретную малую молекулу, которая по форме выглядит как идеальный «замок» для белка B8R вируса оспы обезьян и потенциально способна восстановить интерфероновую систему оповещения организма. Нацеливание на стратегию уклонения вируса от иммунитета, а не на его репликационный механизм, открывает новый угол атаки в антивирусной терапии. Авторы утверждают, что ведущий кандидат теперь должен быть протестирован в лаборатории, где можно будет непосредственно измерить его способность блокировать B8R и сдерживать инфекцию mpox. Если эти тесты окажутся успешными, это может проложить путь к целевому лечению, которое поможет иммунной системе лучше обнаруживать и останавливать вирус.
Цитирование: Ahmad, F., Navid, A., Irfan, M. et al. Discovery of potential antiviral compounds and accelerating the therapeutic discovery against monkeypox virus. Sci Rep 16, 8306 (2026). https://doi.org/10.1038/s41598-026-39427-1
Ключевые слова: противовирусный препарат против оспы обезьян, уклонение от иммунитета, поиск лекарств, компьютерное моделирование, сигнализация интерферона