Clear Sky Science · ru
Оптимизация моноцитов THP-1‑CAR с использованием сигнальной фагоцитоза CD32a для антиген‑специфической активации Т‑лимфоцитов
Обучая иммунную систему новым трюкам
Современные клеточные терапии уже перепрограммируют иммунные клетки для распознавания и уничтожения рака, но большинство из них опираются на Т‑клетки, которые в суровой среде солидных опухолей действуют не всегда эффективно. В этом исследовании авторы обращаются к другому мощному защитнику — макрофагам, «профессиональным поедателям» организма, — и изучают, как их перенастроить так, чтобы они не только эффективнее поглощали вредные клетки или вирусы, но и привлекали Т‑клетки для более длительной и прицельной атаки. Работа выявляет правила проектирования химерных антиген‑распознающих рецепторов (CAR) для макрофагов, которые могут применяться как при инфекциях, например COVID‑19, так и при трудноизлечимых солидных опухолях.
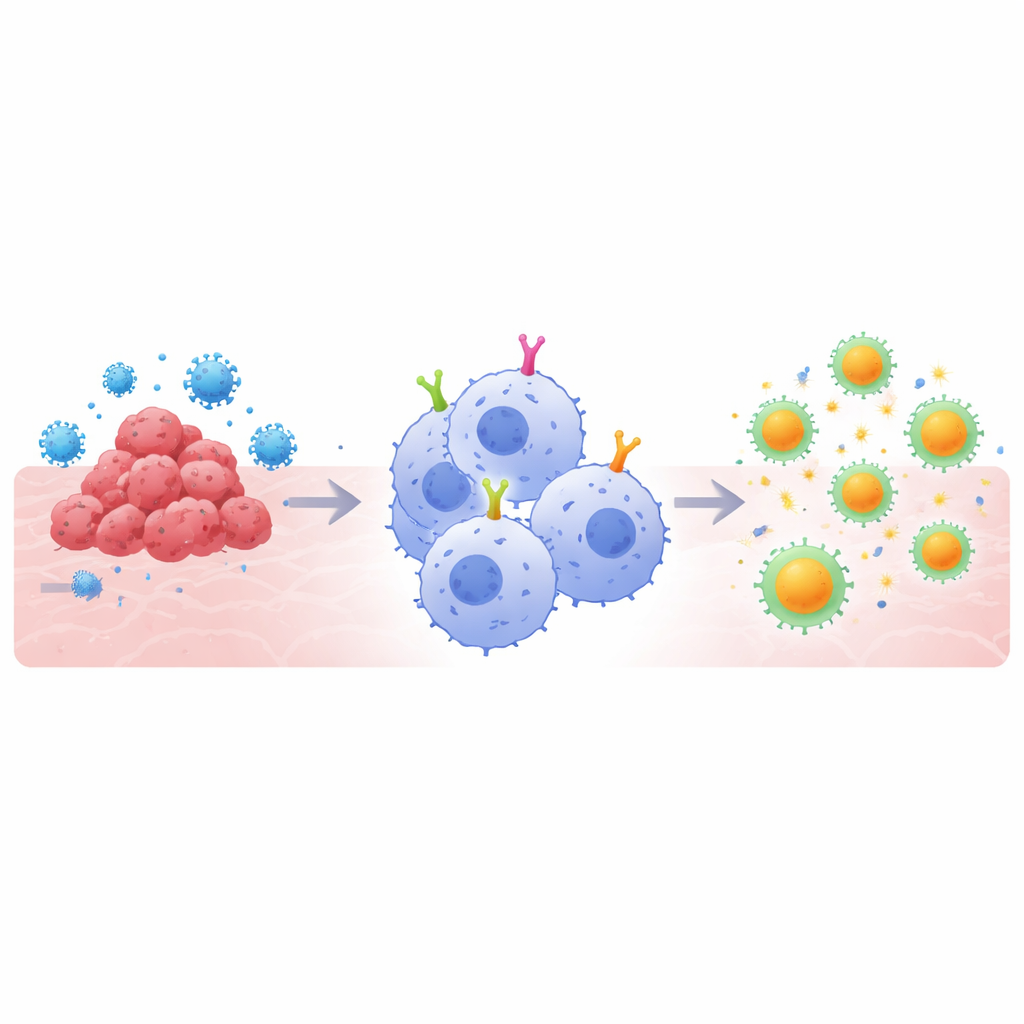
Почему супераппетитные клетки важны
Терапии на базе CAR работают путем оснащения иммунных клеток искусственными поверхностными рецепторами, распознающими выбранную мишень, например опухолевый белок или спайк‑белок вируса. Варианты на основе Т‑клеток преобразили лечение некоторых злокачественных заболеваний крови, но они сталкиваются с препятствиями при работе с солидными опухолями и при некоторых инфекциях. Макрофаги предлагают иной подход: они естественно захватывают угрозы и расщепляют их на фрагменты, которые затем демонстрируются Т‑клеткам, связывая «врожденный» и «адаптивный» отделы иммунитета. Однако большинство дизайнов CAR изначально разрабатывали для Т‑клеток, а не для макрофагов. Авторы пришли к выводу, что чтобы в полной мере использовать сильные стороны макрофагов, внутренние сигнальные компоненты CAR — участки, которые говорят клетке, что делать после связывания мишени — нужно адаптировать специально для этих «поедателей».
Поиск оптимальной внутренней проводки
Команда систематически сравнила несколько внутренних сигнальных доменов в CAR, введённых в линию человеческих моноцитов THP‑1, которые можно превратить в макрофаги. Они сосредоточились на доменах, взятых из рецепторов, которые обычно регулируют фагоцитоз и воспаление: CD3ζ (классический модуль Т‑клеток), CD32a (рецептор, связывающий мишени, покрытые антителами), компоненты CR3 — CD11b и CD18 (ключевые рецепторы комплемента), и TLR4 (сенсор микробной опасности). С помощью частиц и псевдовирусов, покрытых спайк‑белком SARS‑CoV‑2, они оценивали, насколько хорошо каждая конструкция CAR позволяла клеткам поглощать мишени, вырабатывать воспалительные молекулы и затем активировать человеческие CD8 Т‑клетки с памятью на вирус. Затем наиболее перспективные дизайны перенесли в CAR, нацеленные на мезотелин — белок, избыточно экспрессируемый во многих солидных опухолях, — чтобы проверить, сохраняются ли те же правила в онкологическом контексте.
Создание лучших «поедателей» и усилителей сигналов
Вычленилась ясная закономерность: CAR на основе CD32a последовательно обеспечивали более сильный и быстрый фагоцитоз, чем конструкции с традиционным доменом CD3ζ, несмотря на то, что CD3ζ содержит больше обычных мотивов активации. Иначе говоря, «совместимость» сигнала с механизмами макрофага оказалась важнее чистой силы сигнала. Добавление фрагментов, происходящих от CR3 (CD11b или CD18), поверх CD32a в большинстве условий не увеличивало способность к поглощению, но повышало уровни ключевых воспалительных цитокинов, таких как TNF‑α и IL‑1β. Комбинации с TLR4 ещё сильнее усиливали воспалительные сигналы и маркер поверхности CD86, связанный со способностью стимулировать Т‑клетки; однако это сопровождалось компромиссами: более низким уровнем CAR на поверхности клетки и некоторым снижением фагоцитоза.
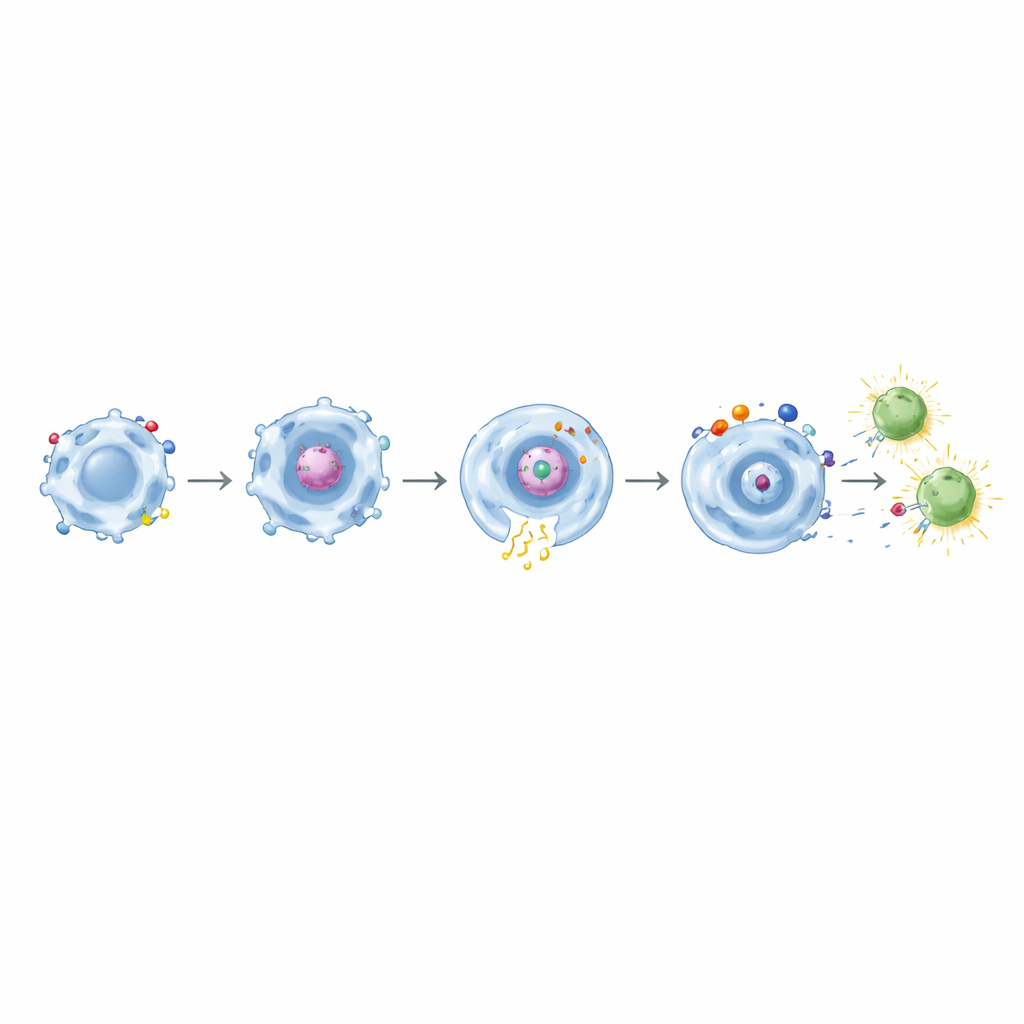
От поедания — к обучению Т‑клеток
Критически важно, что после поглощения спайк‑белка макрофагами с CAR на основе CD32a они смогли активировать память CD8 Т‑клеток от людей, ранее вакцинированных против COVID‑19. Эти Т‑клетки включали ранние маркеры активации и продуцировали эффекторные молекулы, такие как интерферон‑γ и TNF‑α. Эффект усиливался в конструкциях с двумя доменами, которые сочетали CD32a с CD11b, CD18 или TLR4. При тестировании аналогичных дизайнов, нацеленных на мезотелин, против модифицированных опухолевых клеток вновь наблюдалась точная, зависящая от мишени фагоцитозная активность в сочетании с усиленной воспалительной сигнализацией. Среди них сочетание CD32a+TLR4 выделялось как мощная «тканевая тревога», наиболее эффективно усиливая секрецию цитокинов и экспрессию CD86 при сохранении специфичного поедания опухолевых клеток.
Что это может значить для будущих терапий
Для неспециалиста это исследование показывает, что конструирование макрофагов — это не задача «одного размера для всех». Манипулируя и комбинируя внутренние сигнальные модули, учёные могут формировать клетки, которые либо ориентируются на эффективную очистку поражённых клеток, либо действуют как усилители иммунитета, меняя подавляющую среду опухоли и рекрутируя Т‑клетки. CAR на основе CD32a показали себя прочной основой для таких конструкций, превосходя традиционные Т‑клеточные модули в макрофагах и работая как против вирусных, так и против опухолевых мишеней. Хотя эти результаты получены в лабораторных моделях и требуют подтверждения в первичных человеческих клетках и на животных моделях, они дают чертёж для терапии следующего поколения на базе CAR‑макрофагов, которая может лучше бороться с солидными опухолями и персистирующими инфекциями, сочетая быстрое поглощение с точной активацией Т‑клеток.
Цитирование: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
Ключевые слова: CAR‑макрофаги, сигнализация CD32a, фагоцитоз, иммунотерапия солидных опухолей, активация Т‑клеток