Clear Sky Science · ru
Интегративный мультимомикс-анализ выявляет ген, связанный с повреждением ДНК — CLSPN, как биомаркер при раке желудка
Почему это исследование важно
Рак желудка остаётся одним из самых смертоносных видов рака в мире во многом потому, что часто обнаруживается на поздних стадиях и не имеет надёжных ранних признаков. В этом исследовании подробно изучают «царапины» на ДНК — следы повреждений — и выявляют ген CLSPN как перспективный маркер, который может помочь врачам обнаруживать рак желудка раньше, оценивать его агрессивность и, возможно, точнее подбирать лечение.
Поиск сигналов опасности в опухолях желудка
Исследователи исходили из простой идеи: если повреждение ДНК способствует развитию рака желудка, то гены, участвующие в ответе на такие повреждения, могут нести важную информацию о том, кто заболевает и как протекает болезнь. Чтобы проверить это, они объединили несколько крупных наборов данных. Сюда вошли bulk RNA-seq, измеряющий среднюю активность генов в образце опухоли; single-cell RNA-seq, изучающий тысячи отдельных клеток поодиночке; и spatial transcriptomics, сопоставляющий активность генов с местоположением на тканевом срезе. Также собрали обширный список генов, уже связанных с повреждением ДНК. Используя эти ресурсы, они выясняли, какие гены, связанные с повреждением ДНК, сильнее всего коррелируют с раком желудка и выживаемостью пациентов.
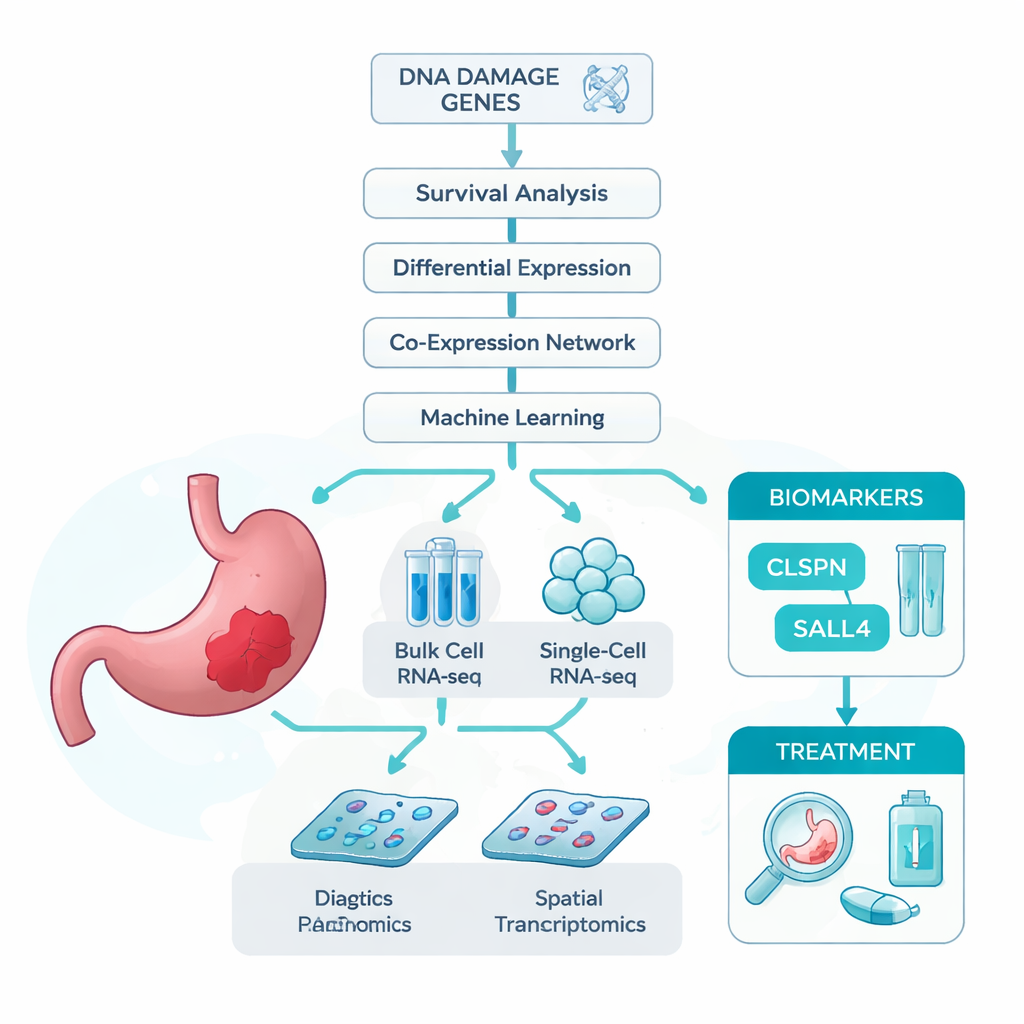
Использование умных алгоритмов для поиска ключевых генов
Поскольку в раке изменяются тысячи генов, команда применила набор статистических и методов машинного обучения, чтобы сузить круг. Сначала отобрали гены, которые были одновременно дизрегулированы в опухолях и однозначно связаны с продолжительностью жизни пациентов. Затем сгруппировали гены по схожим паттернам экспрессии и пересекли результаты со списком генов, связанных с повреждением ДНК. Эта многоступенчатая фильтрация дала 13 сильных кандидатов. Чтобы понять, какие из них наиболее информативны для отличия опухоли от нормальной ткани, они обучили семь различных моделей машинного обучения, каждая ранжировала гены по их вкладу в классификацию. Во всех моделях два гена — CLSPN и SALL4 — стабильно выходили в лидеры, с точностью около или выше 97% и площадью под ROC-кривой более 0.96, что указывает на их высокий диагностический потенциал.
Углублённое изучение CLSPN внутри опухоли
Из двух ведущих генов CLSPN выделялся как наиболее информативный в целом, поэтому авторы исследовали его подробнее. В данных single-cell, охватывающих более 30 000 клеток, активность CLSPN была значительно выше в опухолевых клетках по сравнению с соседними нормальными или стромальными клетками, что указывает на опухоль-специфическую роль. Пространственное картирование срезов пациентов показало аналогичную картину: экспрессия CLSPN концентрировалась в областях, которые патологи признавали как раковые. При разделении опухолевых клеток на группы с «высокой» и «низкой» экспрессией CLSPN, группа с высокой экспрессией проявляла усиленную активность путей, связанных с репликацией ДНК, делением клеток и репарацией — процессами, которые при гиперактивации или неправильной регуляции могут способствовать неконтролируемому росту. Анализ псевдовремени, реконструирующий изменения клеток по условной временной шкале, показал, что по мере прогрессирования опухолевых клеток уровни CLSPN, как правило, повышаются, что намекает на то, что повышение экспрессии CLSPN может быть частью перехода к более злокачественному состоянию.
Связи с иммунной системой и ответом на лечение
Исследование также рассмотрело связь CLSPN с микроокружением опухоли и с потенциальными терапиями. Опухоли с более высокой экспрессией CLSPN демонстрировали иной состав иммунных клеток, особенно макрофагов и отдельных подтипов Т- и NK-клеток, что позволяет предположить, что CLSPN может способствовать формированию иммунодепрессивного микросреды. Моделирование чувствительности к препаратам показало, что опухоли с более высоким уровнем CLSPN могут быть более уязвимы к ряду химио- и таргетных препаратов: повышение CLSPN ассоциировалось с более низкими предсказанными дозами, необходимыми для ингибирования роста. Важно, что при иммуногистохимическом окрашивании реальных тканевых образцов от 70 пациентов уровни белка CLSPN были заметно выше в раковой ткани по сравнению с нормальным желудком и коррелировали с большими размерами опухоли, более глубокой инвазией, поражением лимфатических узлов и более короткой общей выживаемостью.
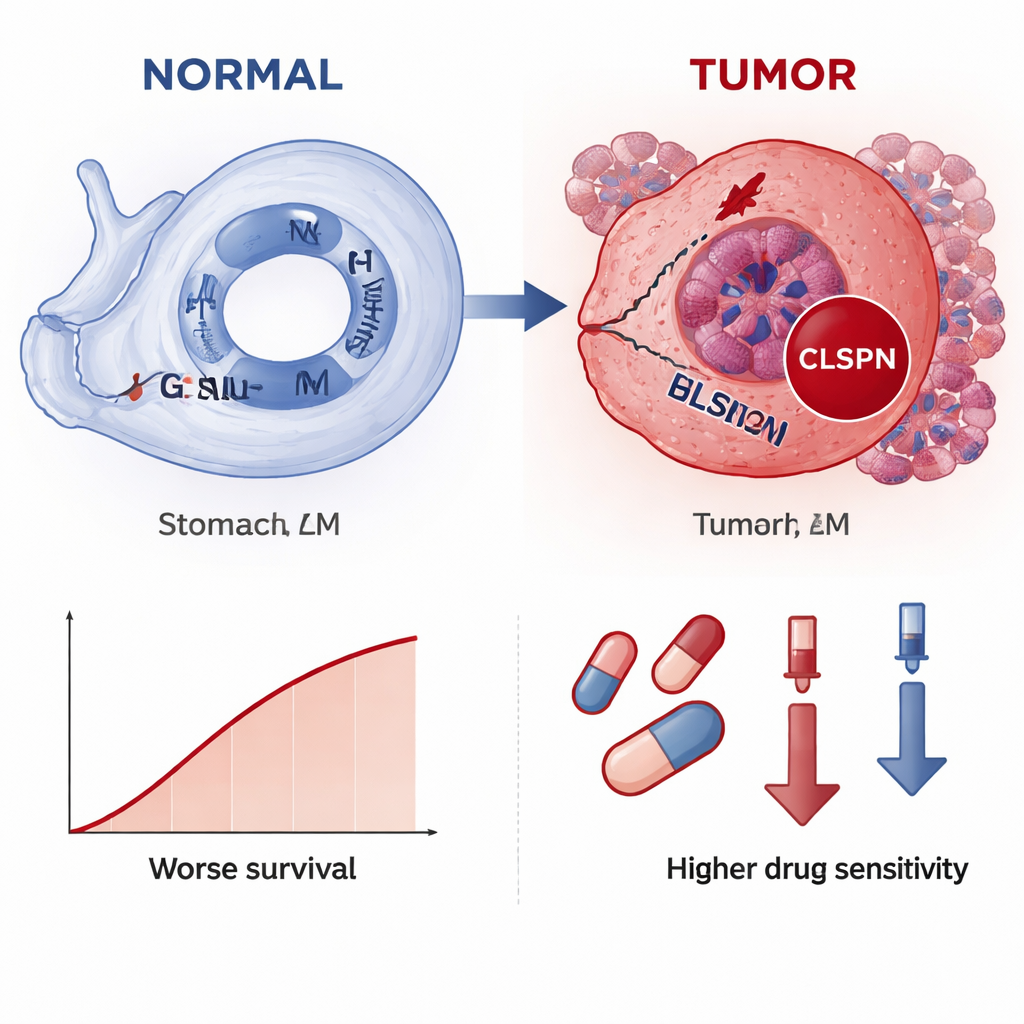
Что это может означать для пациентов
Проще говоря, исследование показывает, что CLSPN ведёт себя как красный предупреждающий индикатор при раке желудка: он включается преимущественно в опухолевых клетках, становится ярче при более продвинутой болезни и сигнализирует о более высоком риске неблагоприятного исхода. Поскольку CLSPN можно выявлять как на уровне РНК, так и стандартными методами окрашивания в клинических лабораториях, он имеет потенциал стать практичным биомаркером для подтверждения диагноза рака желудка, стратификации пациентов по риску и, возможно, для подбора терапии. Хотя прежде чем применять его рутинно потребуется дополнительная клиническая валидация, эта работа демонстрирует, как анализ следов повреждения ДНК на нескольких уровнях данных может выявлять новые инструменты для более ранней диагностики и персонализированного лечения рака желудка.
Цитирование: Ma, Q., Yang, X., Sun, N. et al. Integrating multi-omics analysis identifies DNA damage-related gene CLSPN as a biomarker in gastric cancer. Sci Rep 16, 7789 (2026). https://doi.org/10.1038/s41598-026-39387-6
Ключевые слова: рак желудка, повреждение ДНК, CLSPN, биомаркер, анализ одиночных клеток