Clear Sky Science · ru
Выявление общих генов и связанных с ними микроРНК, метаболитов и путей при ишемическом инсульте и эпилепсии
Почему инсульт и судороги — часть одной истории
Инсульт и эпилепсия обычно рассматриваются как отдельные состояния: один прерывает кровоснабжение мозга, другой вызывает внезапные вспышки аномальной активности мозга. Тем не менее многие пережившие ишемический инсульт впоследствии развивают судороги — осложнение, известное как послеинсультовая эпилепсия. В этом исследовании поставлен простой, но важный вопрос: имеют ли инсульт и эпилепсия общие биологические корни в наших генах и химии крови, и могут ли эти общие сигналы помочь врачам предсказывать и в конечном счёте предотвращать судороги после инсульта?
Поиск общих сигналов в крови
Чтобы исследовать связь, авторы обратились к большим публичным базам данных с образцами крови людей с ишемическим инсультом и людей с эпилепсией и сравнили их со здоровыми контролями. Вместо того чтобы фокусироваться на отдельных генах, они использовали сетевые методы анализа, группирующие гены, которые склонны включаться или выключаться синхронно. Из тысяч генов, которые вели себя по-разному у пациентов и контролей, они построили кластеры, связанные с каждым заболеванием, и затем поискали зоны пересечения. Это выявило 38 генов, изменяющихся в схожем направлении при обоих состояниях, что указывает на общие механизмы болезни, а не на отдельные совпадения. 
Сужение круга до потенциального ключевого игрока
Обнаружение десятков общих генов — лишь первый шаг; задача — выяснить, какие из них важны наиболее существенно. Команда проанализировала, как эти 38 генов взаимодействуют с другими белками клетки, построив сеть белок–белковых взаимодействий и применив несколько математических инструментов для выделения наиболее влиятельных «узловых» генов. Выделились три: IL10RA, CD2 и C3AR1. Когда исследователи проверяли, насколько активность каждого гена отличает пациентов от здоровых людей в нескольких наборах данных, все три показали обещающую диагностическую силу. Однако только один — C3AR1 — стабильно повышался и при инсульте, и при эпилепсии в независимых группах пациентов, что сделало его наиболее устойчивым общим сигналом.
От генов к малым РНК и мозговым химическим веществам
Гены редко действуют в одиночку, поэтому далее исследование спросило, что регулирует C3AR1 и как он может влиять на химию мозга. Команда изучила микроРНК — крошечные фрагменты РНК, тонко регулирующие активность генов — и выявила конкретную микроРНК, называемую let-7b-5p, связанную и с инсультом, и с эпилепсией и предположительно контролирующую C3AR1. Параллельно они провели нетаргетированное исследование малых молекул в крови (метаболомика) на образцах детей с эпилепсией. Это выявило 139 молекул, отличающихся у детей с эпилепсией по сравнению со здоровыми сверстниками. Когда эти сдвиги в метаболизме отобразили на известные биохимические пути, C3AR1 неоднократно обнаруживался в цепях, связанных с нервной сигнализацией, особенно в путях, включающих нейромедиатор ацетилхолин, который помогает регулировать коммуникацию между нервными клетками.
Как изменённая мозговая сигнализация может способствовать судорогам
Объединив данные по генам и метаболитам, исследователи построили более широкую сеть, связывающую C3AR1 с несколькими путями мозговой сигнализации, включая цикл синаптических везикул (как нервные клетки упаковывают и высвобождают химические мессенджеры), холинергическую сигнализацию (пути, управляемые ацетилхолином), сигналы, связанные со вкусом, и пути, ассоциированные с никотином. В крови детей с эпилепсией уровни ацетилхолина были снижены, а C3AR1 располагался в стратегических точках путей, где этот молекула оказывает своё действие. Авторы выдвигают гипотезу, что сдвиги в активности C3AR1, возможно управляемые let-7b-5p, могут нарушать ацетилхолин-зависимую сигнализацию и высвобождение нейромедиаторов в синапсах. Со временем такие дисбалансы могут повышать возбудимость мозговых цепей после инсульта, подталкивая их к судорожной активности. 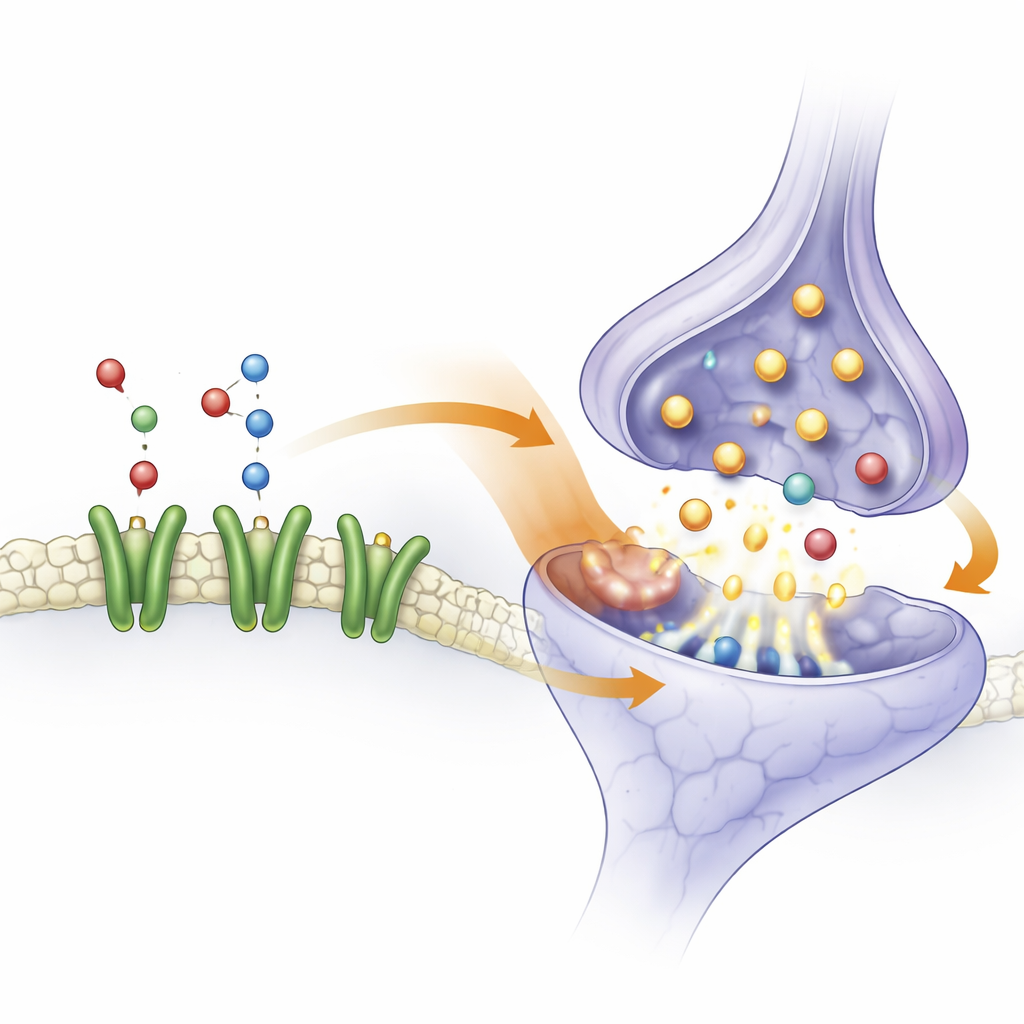
Что это может значить для пациентов
В совокупности результаты указывают, что инсульт и эпилепсия разделяют не только клинические взаимосвязи, но и биологическую основу, включающую ген C3AR1, его регуляторную микроРНК let-7b-5p и нейромедиатор ацетилхолин. Хотя эти выводы в основном основаны на анализе данных и относительно небольшой группе детей с эпилепсией, они поднимают возможность того, что маркеры в крови однажды помогут выявлять выживших после инсульта с высоким риском развития судорог. Авторы предупреждают, что C3AR1 в одиночку вряд ли станет идеальным предиктором; более надёжными могут быть панели генов, микроРНК и метаболитов. Тем не менее работа указывает на будущее, в котором простой анализ крови мог бы направлять персонализированный мониторинг и стратегии лечения людей, живущих в тени и инсульта, и эпилепсии.
Цитирование: Chen, Y., Man, S., Li, Q. et al. Identifying the shared genes and their related microRNAs, metabolites, and pathways in ischemic stroke and epilepsy. Sci Rep 16, 8166 (2026). https://doi.org/10.1038/s41598-026-39299-5
Ключевые слова: ишемический инсульт, послеинсультовая эпилепсия, биомаркеры, C3AR1, метаболомика