Clear Sky Science · ru
Интегративная структура для обнаружения рака через интегро-дифференциальные уравнения с использованием методов глубокого обучения
Почему важны более умные сканы
Ранняя диагностика рака может спасти жизни, но чтение медицинских снимков, таких как маммограммы, сложно, занимает много времени и подвержено человеческим ошибкам. Врачам приходится различать слабые признаки болезни на фоне нормальных тканей и шумов изображения, часто в условиях ограниченного времени. В этой работе предложен новый подход, который помогает: сложные изображения молочной железы преобразуются в упрощённые одномерные сигналы, после чего для решения задачи о наличии рака используются как математические модели, так и методы искусственного интеллекта. Цель не заменить врачей, а дать им более ясные и надёжные подсказки, скрытые в каждом скане.
Преобразование изображений в сигналы
Авторы начинают с переосмысления представления медицинского изображения. Вместо того чтобы рассматривать маммограмму как огромную сетку пикселей, её преобразуют в один «линейный» сигнал, суммирующий изменения яркости по всей груди. Сначала изображение очищают: переводят в оттенки серого, удаляют шум и выравнивают интенсивность, чтобы темные и светлые области были сопоставимы. Края и текстуры подчёркиваются стандартными фильтрами, а общая картина светлых и тёмных участков анализируется с точки зрения частот (аналогично разложению аудио на басы и высокие частоты). Затем значения пикселей усредняют по строкам или столбцам, получая гладкую одномерную кривую. Пики этой кривой соответствуют плотным тканям или подозрительным областям; впадины — более пустым участкам. Хотя некоторая мелкая детализация теряется, на выходе получается компактный сигнал, сохраняющий крупные структуры, наиболее важные для диагноза. 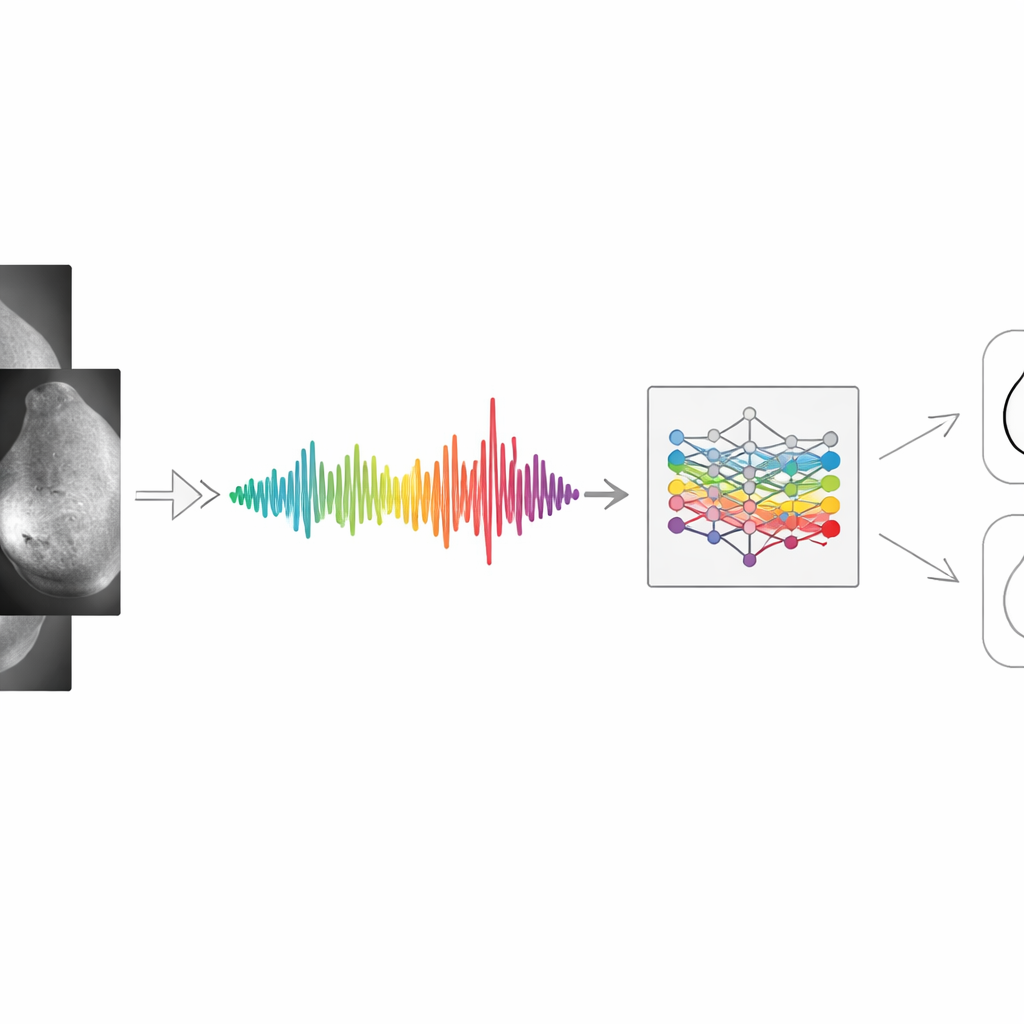
Добавление биологического уровня с помощью уравнений
Многие современные системы глубокого обучения работают напрямую с изображениями и часто критикуются как «чёрные ящики», дающие мало понимания о том, как опухоли действительно развиваются. Чтобы это исправить, авторы встраивают математические модели роста опухоли в свою конвейерную обработку сигналов. Они используют интегро-дифференциальные уравнения — уравнения, которые описывают изменение во времени с учётом прошлого — чтобы моделировать размножение раковых клеток, их распространение и формирование кровоснабжения. В уравнения включены члены, отвечающие за скорость роста, ограничение из‑за скученности, движение клеток и неоваскуляризацию. Симулируя, как опухоль может развиваться и влиять на распределение яркости на маммограмме, рамочная модель генерирует дополнительные признаки, основанные на известной биологии, а не только на распознавании шаблонов. Эти обогащённые сигналы призваны сделать финальные предсказания более интерпретируемыми для клиницистов.
Обучение компактной нейросети для принятия решения
После того как изображение превращено в математически обогащённый сигнал, упрощённая одномерная свёрточная нейронная сеть (CNN) выполняет классификацию. Эта сеть прокатывает небольшие фильтры по сигналу, чтобы обнаруживать информативные формы — резкие скачки, плавные наклоны или повторяющиеся рябь — которые могут указывать на аномальную ткань. Модель обучали на общедоступных наборах маммограмм (INbreast и MIAS), разделяя данные на обучающую, валидационную и тестовую части, чтобы избежать переобучения. Авторы расширяли данные и тщательно настраивали параметры модели для повышения устойчивости. Чтобы дополнительно раскрыть «чёрный ящик», они применили инструменты объяснимости, которые выделяют участки сигнала, наиболее повлиявшие на решение, связывая их с областями на исходном изображении груди, где изменялась плотность ткани или границы.
Насколько хорошо это работает на практике
В испытаниях на этих реальных коллекциях маммограмм интегративная структура правильно разделяла злокачественные и незлокачественные случаи примерно в 96,4% случаев, превосходя стандартные CNN, машины опорных векторов, деревья решений и несколько современных базовых методов глубокого обучения. Она также показала высокую чувствительность — большинство раков было успешно обнаружено — и высокую специфичность — здоровые пациенты реже отмечались ошибочно. Поскольку система работает с 1D сигналами, а не с полными изображениями, ей требуется меньше памяти и она может выдавать предсказания быстрее, чем многие тяжёлые сетевые модели для изображений, что важно для загруженных клиник или на скромном железе. Добавленное математическое моделирование, по-видимому, уточняет важные признаки, повышая точность без экстремальных вычислительных затрат.
К чему это может привести дальше
Авторы приходят к выводу, что сочетание преобразования изображения в сигнал, математических моделей роста опухоли и глубокого обучения предлагает перспективный путь к более точным и понятным инструментам скрининга рака. Их подход пока на ранней стадии: он в основном валидирован на изображениях молочной железы, и при преобразовании в сигнал могут теряться некоторые тонкие визуальные детали. В будущей работе метод будут проверять на других типах рака, добавлять более подробные объяснения для врачей и интегрировать дополнительные данные, такие как гистологические срезы, клинические маркеры и генетическая информация. При более широкой валидации такая математически обоснованная ИИ-система в конечном счёте может поддерживать системы принятия решений в реальном времени, помогая рентгенологам обнаруживать рак раньше и с большей уверенностью.
Цитирование: Gopisairam, T., Thota, S. & Bikku, T. Integrative framework for cancer detection via integro-differential equations using deep learning techniques. Sci Rep 16, 9714 (2026). https://doi.org/10.1038/s41598-026-39283-z
Ключевые слова: обнаружение рака, медицинская визуализация, глубокое обучение, математическое моделирование, маммография молочной железы