Clear Sky Science · ru
Мета-анализ выявляет драйверные гены и характеризует молекулярную эпидемиологию колоректального рака
Почему это исследование важно для повседневного здоровья
Колоректальный рак — один из самых распространённых видов рака в мире, но ни одна опухоль не бывает полностью идентичной другой. В этом исследовании задан простой, но ключевой вопрос: если объединить генетические данные тысяч пациентов из разных стран, удастся ли, наконец, получить более чёткую карту тех изменений в ДНК, которые действительно движут это заболевание, как они различаются между типами опухолей и что это значит для диагностики и выживаемости? Ответы могут повысить точность скрининга, направить разработку лекарств и помочь объяснить, почему люди разного возраста, пола и с опухолями в разных участках кишечника имеют разные риски и исходы.
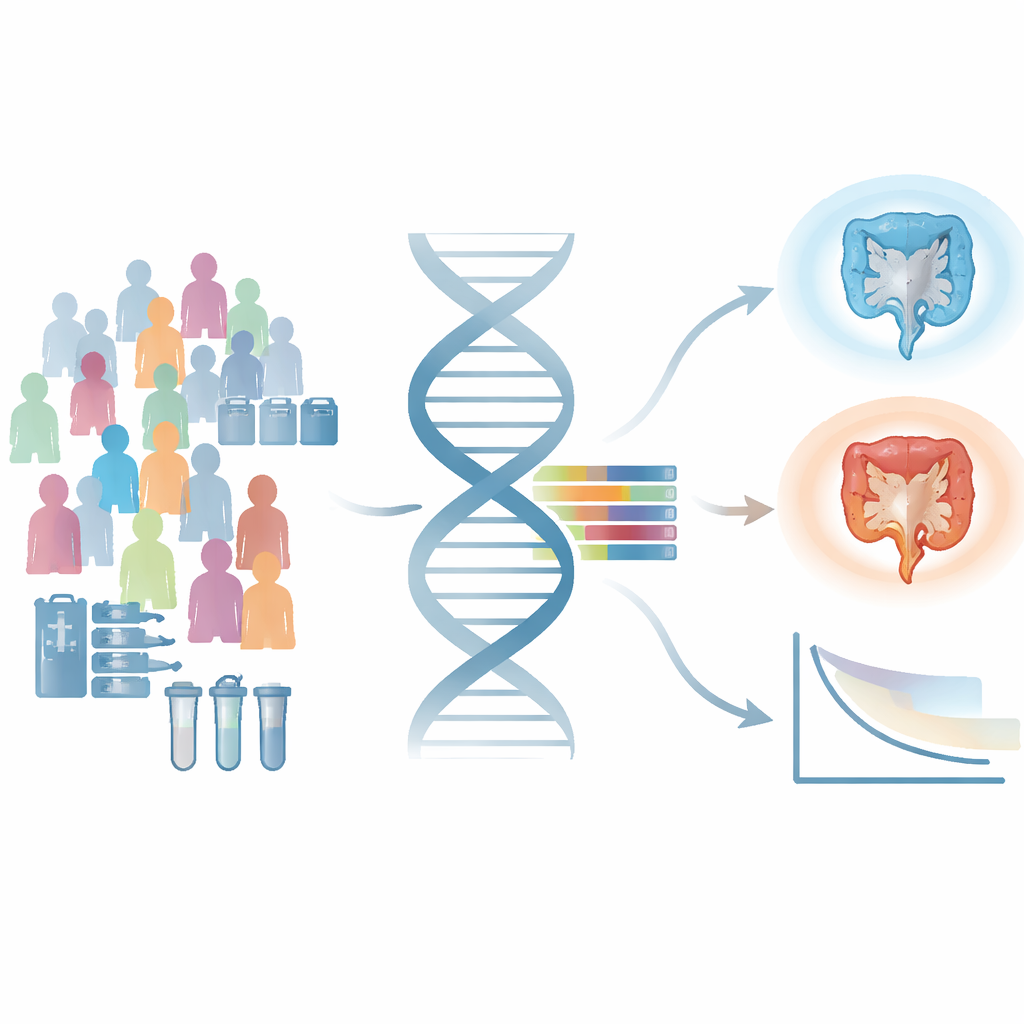
Объединение многих исследований
Исследователи объединили новые генетические данные более чем 2 100 исландских случаев колоректального рака с данными о мутациях более чем 9 000 опухолей, ранее изученных в США, Европе и Азии. Вместо анализа каждого набора отдельно они рассматривали совокупную коллекцию как единый большой проект и использовали статистические инструменты, специально разработанные для объединения результатов между исследованиями. Важным шагом стало разделение опухолей на две основные группы: «микрoсателлит-стабильные» (MSS), которые мутируют с более типичной частотой, и «микрoсателлит-нестабильные» (MSI), имеющие очень большое число изменений в ДНК. Поскольку эти две группы по-разному проявляются в клинике, команда анализировала их отдельно на каждом этапе.
Нахождение ядра драйверных генов рака
С помощью методов, сравнивающих вредоносные мутации с нейтральными внутри каждого гена, учёные искали признаки «положительного отбора» — то есть изменений, которые опухоли повторно приобретают, потому что они дают преимущество в росте. Этот мета-анализ выделил 112 генов как сильных драйверов колоректального рака, многие из которых ранее не соответствовали строгим статистическим критериям у человека. Некоторые гены хорошо известны по их ролям в других видах рака, другие входят в устоявшиеся пути, контролирующие рост и межклеточную коммуникацию, такие как WNT, RAS/MAPK и сигнальный путь TGF‑beta. Важно, что десятки этих драйверных генов были пропущены или имели слабую поддержку в ранних сводных каталогах, что показывает: гораздо большие размеры выборки могут выявить новых участников и подвергнуть сомнению некоторых прежних подозреваемых.
Два типа опухолей — пересекающиеся, но разные
Сравнение MSS и MSI показало, что обе группы разделяют множество драйверных генов, но при этом имеют явные предпочтения. Например, определённые гены, помогающие опухолям уклоняться от иммунной системы, сильно отбираются в MSI‑опухолях, которые уже несут много мутаций и более заметны для иммунных клеток. Напротив, несколько генов, контролирующих, как читается ДНК и как включаются или выключаются гены, более характерны для MSS‑опухолей. Даже внутри одних и тех же путей разные члены чаще затрагиваются в каждом подтипе: некоторые гены WNT и RAS чаще изменены в MSS, тогда как другие участники тех же путей чаще поражаются в MSI. Эти закономерности указывают на то, что два типа опухолей следуют родственными, но различными эволюционными путями по мере роста.
Связи с внешним видом опухоли и характеристиками пациентов
Большой объединённый набор данных также позволил команде выйти за рамки генов и связать мутации с тем, кто получает какие опухоли и как эти опухоли выглядят под микроскопом. Было обнаружено, что некоторые ключевые мутации варьируют в зависимости от пола, возраста и точного местоположения опухоли в кишечнике, и что эти паттерны могут идти в противоположных направлениях в MSS и MSI. Одно заметное открытие касается «муцинозных» опухолей, которые производят большое количество желеобразного вещества. Среди MSS‑опухолей муцинозные опухоли значительно чаще несут мутации в нескольких генах пути TGF‑beta. В MSI‑опухолях почти все опухоли уже имеют изменения в этом пути, что может частично объяснить, почему муцинозный рост так часто встречается в этой группе.
Генетические подсказки к выживаемости
Поскольку несколько когорт включали длительное наблюдение, исследователи могли проверить, связаны ли конкретные драйверные гены с общей выживаемостью с учётом стадии опухоли и других факторов. Для MSS‑опухолей мутации в гене APC ассоциировались с лучшими исходами, тогда как изменения в BRAF и ещё одном гене, RNF43, прогнозировали худшую выживаемость. Ни один отдельный ген не показал сильного эффекта на выживаемость в MSI‑опухолях после применения строгих статистических поправок, что вновь подчёркивает необходимость рассматривать эти два типа рака отдельно при интерпретации генетических результатов.
Что это значит для пациентов и медицины
Объединив данные более чем 11 000 случаев колоректального рака, это исследование даёт одну из самых ясных карт ядра генов, способствующих возникновению этих опухолей, способов их различия между двумя основными типами и того, как они связаны с внешним видом опухоли и выживаемостью пациентов. Для неспециалистов главный вывод таков: колоректальный рак — не единое заболевание, а совокупность родственных эволюционных путей, формируемых нашей биологией и окружающей средой на протяжении многих лет. Более точный список действительно важных драйверных генов и лучшее понимание того, как они взаимодействуют с типом опухоли и характеристиками пациента, может помочь в будущих стратегиях скрининга, уточнении прогноза и указать путь к более целенаправленным и персонализированным методам лечения.
Цитирование: Olafsson, S., Thorarinsson, T., Gudjonsson, S.A. et al. A meta-analysis identifies driver genes and characterizes the molecular epidemiology of colorectal cancer. Sci Rep 16, 9427 (2026). https://doi.org/10.1038/s41598-026-39255-3
Ключевые слова: генетика колоректального рака, онкогенные драйверные гены, микрoсателлитная нестабильность, эволюция опухоли, прогноз при раке