Clear Sky Science · ru
Динамика митохондриальной функции периферических мононуклеарных клеток крови в ранней фазе сепсиса у пациентов отделений интенсивной терапии
Почему «электростанции» наших клеток важны при смертельной инфекции
Сепсис, угрожающее жизни чрезмерное реагирование на инфекцию, ежегодно отправляет в отделения интенсивной терапии сотни тысяч людей и убивает миллионы во всём мире. Врачи знают, что при сепсисе даёт сбой множество органов, но скрытая роль крошечных «электростанций» внутри иммунных клеток — митохондрий — была труднее для понимания. В этом исследовании пациенты с сепсисом в отделении интенсивной терапии наблюдались в течение первой недели пребывания, чтобы узнать, как меняется выработка энергии ключевыми клетками крови со временем и связаны ли эти изменения с выживанием.
Взгляд внутрь крови при сепсисе
Исследователи сосредоточились на периферических мононуклеарных клетках крови, крупной группе лейкоцитов, которые участвуют в воспалении и борьбе с микроорганизмами. Поскольку они циркулируют по всему организму и легко поддаются забору, эти клетки дают удобное окно в состояние иммунной системы. Команда сравнила 40 взрослых пациентов с сепсисом или септическим шоком в нидерландском отделении интенсивной терапии с 30 тщательно подобранными госпитальными контрольными пациентами сопоставимого возраста и пола, не имевшими сепсиса и иными метаболически здоровыми. У пациентов с сепсисом кровь брали трижды — в первые двое суток после поступления в ОИТ и затем примерно на 3–4 и 5–6-й дни — в то время как у контрольной группы забор выполнялся единожды. Из каждой пробы выделяли иммунные клетки, помещали их в стандартизованный питательный раствор и измеряли, с какой скоростью их митохондрии потребляют кислород в разных условиях — прямой показатель того, насколько интенсивно работают «электростанции» клеток. 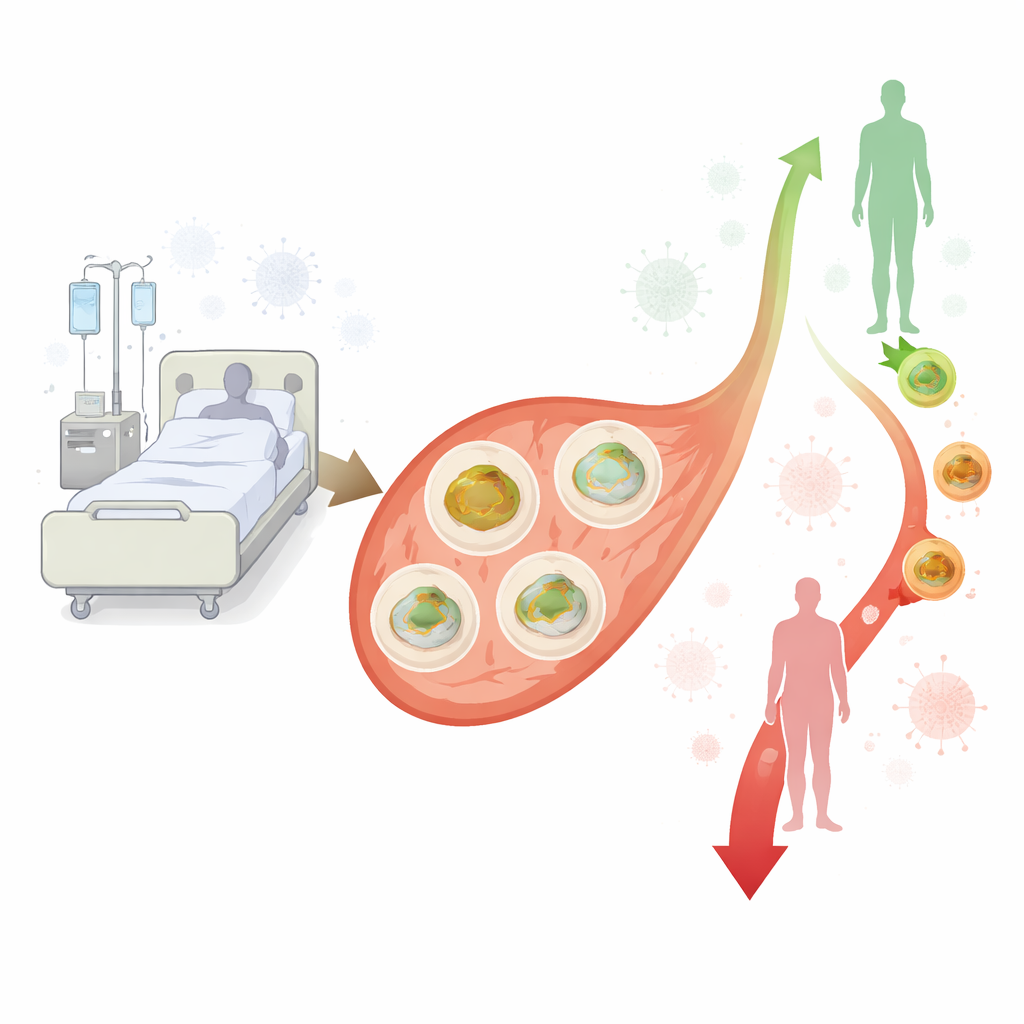
Двигатели иммунных клеток работают на повышенных оборотах
Вопреки представлению о том, что при сепсисе клеточная выработка энергии просто «выключается», команда обнаружила, что митохондриальная активность в иммунных клетках у пациентов с сепсисом была стабильно выше, чем у контролей. На всех временных точках базальное дыхание (основное потребление кислорода в покое) было повышено. Компоненты, связанные с продуктивным образованием энергии — дыхание, связанное с синтезом АТФ, — а также максимальная дыхательная способность митохондрий также, как правило, были выше, особенно в более поздние дни первой недели. Даже протонная утечка, форма «пустого» расходования топлива, при которой энергия расходуется без её образования, была увеличена. В совокупности эти данные указывают на то, что по крайней мере в циркулирующих иммунных клетках энергетический механизм скорее разгоняется, чем останавливается в раннем сепсисе — возможно, отражая высокие потребности активированной иммунной реакции.
Генные сигналы, соответствующие повышенной активности
Чтобы проверить, поддерживается ли более высокая скорость «дыхания» на молекулярном уровне, исследователи изучили активность ряда генов, кодирующих ключевые элементы митохондриальной системы. У подгруппы из 10 пациентов с сепсисом и 10 сопоставленных контролей они измеряли экспрессию генов для компонентов окислительного фосфорилирования — белковых комплексов, превращающих топливо в АТФ. Два гена в частности, SDHB (часть комплекса II) и ATP5F1A (часть комплекса V, АТФ-синтазы), были значимо более активны у пациентов с сепсисом в нескольких временных точках, с приростом примерно на 40–50% по сравнению с контролями. Это молекулярное «повышение передачи» в ядре машинерии хорошо согласуется с функциональными данными и усиливает идею о том, что митохондрии иммунных клеток подвергаются повышенной нагрузке при сепсисе, а не полностью разрушаются. 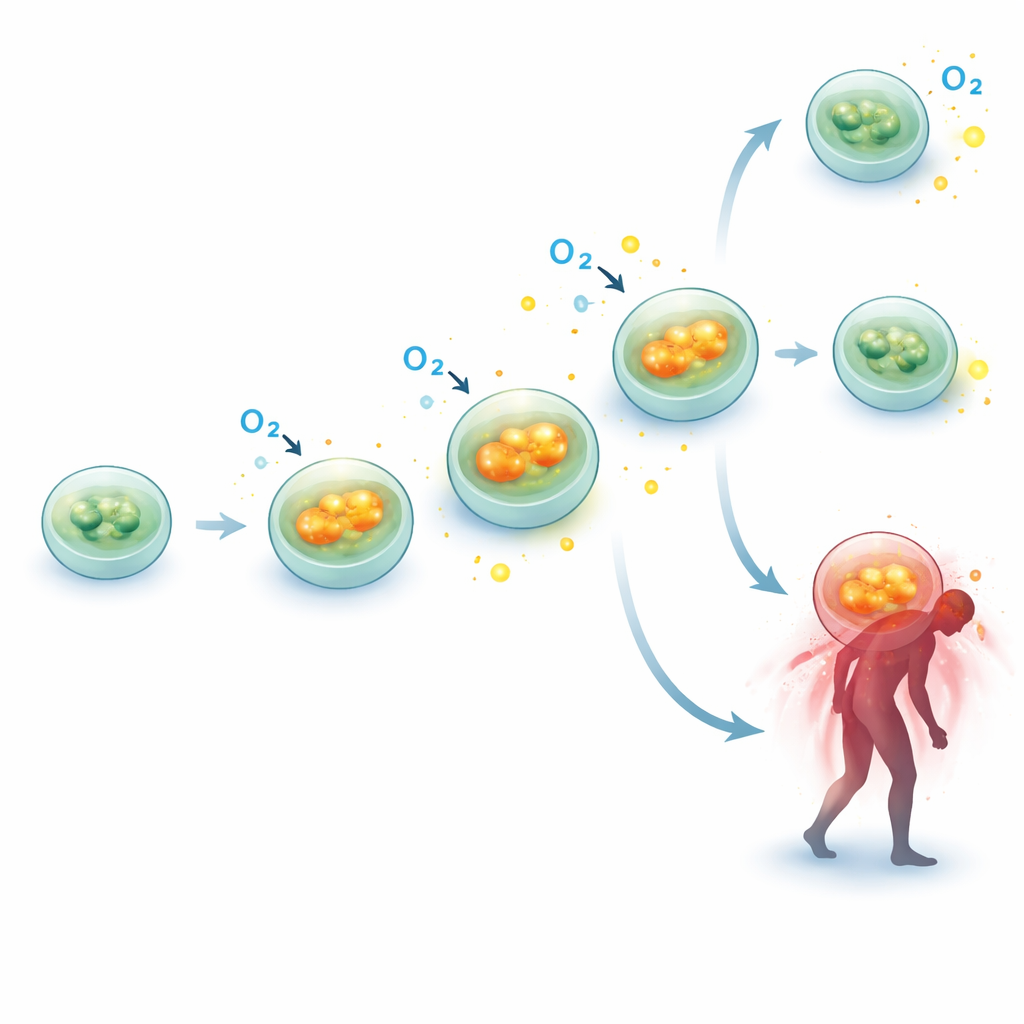
Энергетические изменения связаны с выживаемостью
Наиболее тревожным оказалось то, как эти митохондриальные изменения соотносились с исходами. При сравнении выживших и невыживших в течение трёх месяцев существенных отличий в митохондриальной функции на самом первом измерении не выявили. Однако направление изменений в течение первой недели рассказало другую историю. У выживших митохондриальное дыхание в иммунных клетках имело тенденцию слегка снижаться или оставаться стабильным. У пациентов, которые впоследствии умерли, те же показатели — базальное, связанное с АТФ, максимальное дыхание и резервная ёмкость — в течение недели ещё более возрастали. Статистический анализ показал, что более выраженное увеличение базального дыхания между первым и последним измерениями было связано с повышенным риском смерти в течение трёх месяцев, даже с учётом оценок тяжести заболевания. Поскольку число смертей было невелико, авторы подчёркивают, что эта связь носит исследовательский характер и требует подтверждения, но она наводит на мысль, что постоянно нарастающий метаболический драйв в иммунных клетках может быть признаком риска.
Что это значит для пациентов с сепсисом
Для неспециалиста основное послание такое: в раннем сепсисе «электростанции» в циркулирующих иммунных клетках не просто отказывают; напротив, они, по-видимому, переходят на режим форсажа. Это дополнительное усилие может помогать питать раннюю борьбу организма с инфекцией, но у некоторых пациентов активность продолжает расти вместо того, чтобы стабилизироваться, и такая стойкая гиперактивность в клетках крови ассоциируется с худшей выживаемостью. Исследование ещё не показывает, полезен ли этот митохондриальный «разгон», вреден ли он или может быть и тем, и другим на разных этапах, но подчёркивает, что сепсис — это во многом болезнь энергетического баланса организма, наряду с инфекцией и воспалением. В будущем внимательное отслеживание и, возможно, мягкая корректировка этого клеточного потребления энергии могут стать частью оценки риска и индивидуализации лечения пациентов с сепсисом в ОИТ.
Цитирование: Moonen, H.P.F.X., Slingerland-Boot, R., de Jong, J.C.B.C. et al. Progression of peripheral blood mononuclear cell mitochondrial function during the early phase of sepsis in intensive care unit patients. Sci Rep 16, 8828 (2026). https://doi.org/10.1038/s41598-026-39202-2
Ключевые слова: сепсис, митохондрии, клетки иммунной системы, критическое состояние, клеточный метаболизм