Clear Sky Science · ru
Диагностика острого синдрома аорты с помощью ИИ на основе мульти‑модального слияния информации
Почему это важно для людей с болью в груди
Острый синдром аорты — это неотложное состояние, при котором главная артерия организма может внезапно разорваться; при пропуске диагноза смерть может наступить в течение нескольких часов. Симптомы часто маскируются под инфаркт, растяжение мышц или даже несварение желудка, поэтому заболевание легко ошибочно принять за что‑то другое. В этом исследовании описана новая система искусственного интеллекта, которая объединяет данные КТ‑ангиографии и анализов крови, чтобы помочь врачам распознавать эти скрытые артериальные катастрофы раньше и точнее, а также отметать сомнительные случаи, требующие повторной оценки.
Опасный разрыв, который прячется на виду
Острый синдром аорты (ОСА) включает несколько взаимосвязанных повреждений стенки аорты: классическое расслаивание, интрамуральную гематому и проникающие язвы. Объединяющая их опасность в том, что кровь проникает в или через стенку сосуда, что может быстро привести к разрыву или потере кровоснабжения жизненно важных органов. Риск особенно высок в первые сутки–двое после появления симптомов, когда без быстрой помощи смертность может приближаться к 70%. Врачи используют КТ‑ангиографию для визуализации аорты и анализы крови, такие как D‑димер и маркеры воспаления, чтобы оценить свертываемость и иммунную активность. Но жалобы пациентов часто расплывчаты, физикальное обследование может выглядеть нормально, а КТ‑изображения — едва заметными или искаженными движением и артефактами, поэтому примерно в одной трети случаев при обычной практике диагноз первоначально пропускают.
Чего не хватает современным ИИ‑инструментам
В последние годы появились мощные системы распознавания изображений, способные сканировать КТ или рентген на предмет признаков разрывов аорты. Однако большинство таких инструментов анализируют только изображения и игнорируют данные лабораторий, либо просто соединяют разные потоки данных без реального обучения их взаимному влиянию. Это расходится с клиническим мышлением: врачи мысленно связывают то, что видят на скане, с лабораторными значениями и анамнезом. Простейшее «склеивание» признаков изображения и чисел лабораторий может даже ухудшить ситуацию, поскольку данные анализов часто шумные, неполные и математически взаимосвязанные. Многие модели ИИ также работают как черные ящики, вынося вердикт без объяснения логики, что затрудняет их использование в экстренной медицине, где на кону — жизнь пациента.
Новый подход к слиянию сканов и анализов крови
Авторы разработали модель мультимодального многомасштабного слияния (MMMF), призванную имитировать рассуждения опытных радиологов и кардиологов. Сначала двухветвевой кодировщик изображений анализирует КТ‑ангиографию на двух уровнях детализации: крупные патчи улавливают общую форму и ход аорты, а мелкие патчи сосредоточены на тонких деталях, например на небольших интимальных разрывах или локальных скоплениях крови в стенке. Параллельно ключевые показатели крови — включая D‑димер и набор маркеров воспаления, выведенных из количества лейкоцитов и тромбоцитов — преобразуются в числовые признаки. Эти признаки изображения и лабораторные признаки становятся узлами в графоподобной структуре, где продвинутая графовая нейронная сеть передаёт «сообщения» между ними, обучаясь тому, как определённые паттерны в крови усиливают или противоречат тонким находкам на изображениях.
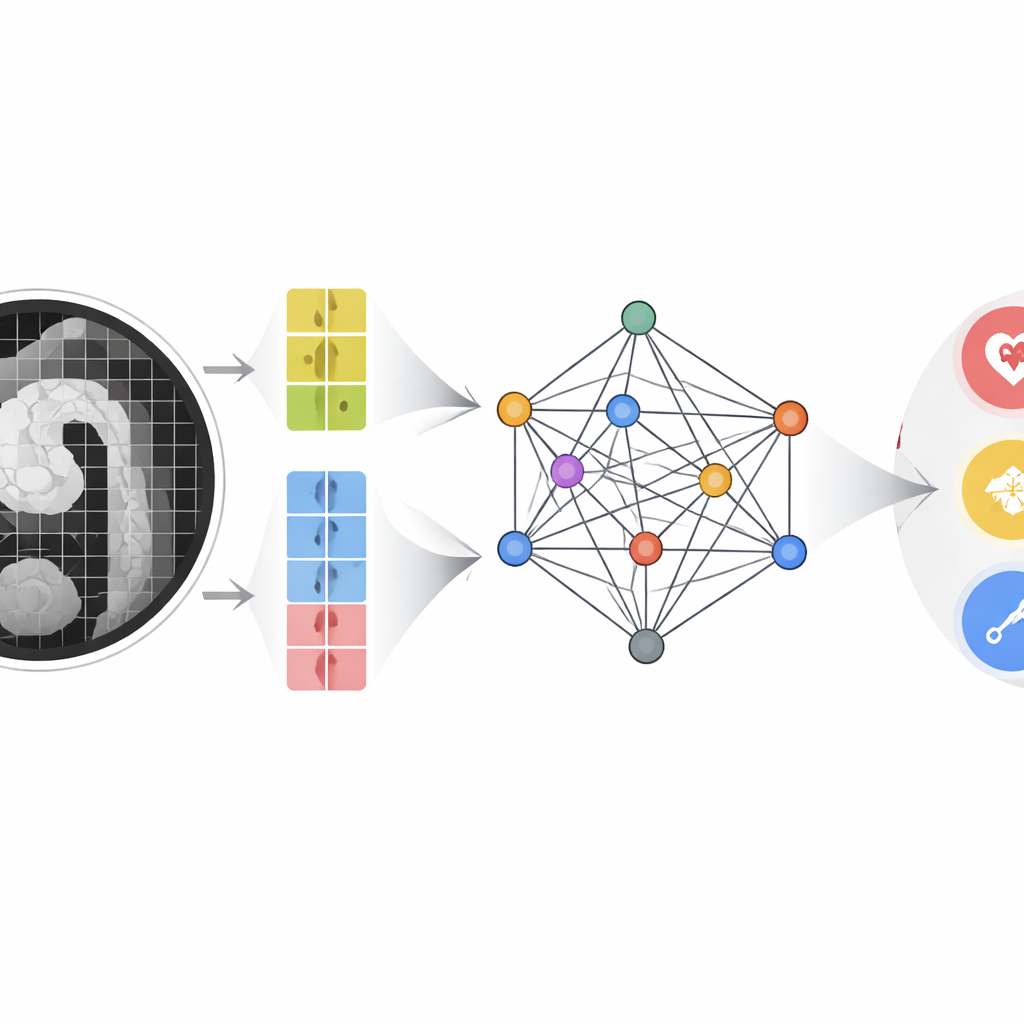
Насколько хорошо работает система
Команда обучала и тестировала модель MMMF на КТ‑сканах и сопутствующих анализах крови 493 пациентов, обследованных в период с 2019 по 2024 год; в выборке были подтверждённые случаи разных типов ОСА и контрольные пациенты без ОСА. Их подход сравнивали с известными моделями, работающими только с изображениями, моделями, использующими лишь лабораторные данные, и несколькими современными мультимодальными системами, изначально созданными для синхронизации изображений с текстом. По показателям точности, precision, recall и F1 модель MMMF оказалась лучшей. Полезная площадь под ROC‑кривой превысила 0,9, что указывает на высокую способность различать нормальные аорты, классические расслаивания восходящей и нисходящей аорты и нетипичные формы. Изображения оставались самым сильным одиночным источником информации, но аккуратно структурированное слияние с лабораторными данными давало заметный прирост, особенно в сложных или пограничных случаях. Абляционные эксперименты показали, что решающими элементами были двухмасштабный путь обработки изображений и трансформер‑основанный граф для моделирования дальнодействующих связей между признаками.
К партнерству врачей и машин
Помимо громких цифр по точности, ключевой вклад этого исследования — акцент на сотрудничестве, а не на замене. Система особенно хорошо очищает ясные нормальные сканы и явно патологические нетипичные случаи, выступая в роли интеллектуального первичного скрининг‑инструмента. Не менее важно, что она может распознавать, когда её собственная уверенность низка — часто в тех случаях, которые и человеческим экспертам кажутся сложными, например при ранних или более мягких формах расслаивания — и помечать таких пациентов для срочного повторного рассмотрения, дополнительной визуализации или консультации старшего специалиста. По сути, исследование показывает: если детали изображений и подсказки из анализов крови переплетены в структурированном, клинически обоснованном виде, ИИ может улучшить раннюю диагностику острого синдрома аорты и служить страховкой против пропущенных неотложных состояний, оставляя финальное решение за врачом.
Цитирование: Yang, Z., Xu, S., Wang, B. et al. AI-driven diagnosis of acute aortic syndrome based on multi-modal information fusion. Sci Rep 16, 8332 (2026). https://doi.org/10.1038/s41598-026-39111-4
Ключевые слова: острый синдром аорты, расслоение аорты, медицинский ИИ, мультимодальная диагностика, графовая нейронная сеть