Clear Sky Science · ru
Дефицит Dlgap2 нарушает синаптический гомеостаз, способствуя убиквитин‑опосредованному разрушению Itsn1 в модели, имитирующей аутизм, вызванную вальпроевой кислотой
Почему важно обычное лекарство и проводка мозга
Вальпроевая кислота — давно используемый препарат при эпилепсии и расстройствах настроения, но при приеме во время беременности он связан с повышенным риском аутизма у детей. В этом исследовании поставлен актуальный для семей и врачей вопрос: что именно делает этот препарат с развивающейся «проводкой» мозга? Трассируя изменения до отдельных молекул в синапсах — точках связи нейронов — исследователи раскрывают новую цепочку событий, которая может помочь объяснить поведение, похожее на аутистическое, и указать пути для будущих терапевтических стратегий. 
Ищем общие уязвимые места в разных видах
Чтобы найти надежные подсказки, команда не ограничилась одной моделью животных. Они сравнили мозги или мозгоподобные ткани из человеческих кортикальных органоидов, обезьян, крыс и мышей, подвергшихся внутриутробному воздействию вальпроевой кислоты. С помощью масштабных обследований генов и белков они выделили небольшой набор генов, изменившихся во всех этих системах и связанных с синапсами и миелинизацией аксонов. Среди них выделялся один: Dlgap2, белок‑каркас, который помогает организовывать постсинаптическую часть возбуждающих синапсов. У мышей, получавших вальпроевую кислоту пренатально, уровень Dlgap2 снизился в коре и, более того, внутри крошечных синаптических компартментов, что указывает на то, что этот структурный белок является ключевой жертвой воздействия препарата.
От молекулярных сдвигов к поведенческим изменениям
Затем авторы поинтересовались, достаточно ли одного лишь падения Dlgap2, чтобы нарушить работу мозга. Они использовали вирусы, несущие короткие шпильковидные РНК, чтобы понизить экспрессию Dlgap2 в культуре нейронов мыши и у новорожденных мышей. В культуре нейроны с пониженным Dlgap2 образовывали более короткие ветви и имели меньше постсинаптических пунктов — признаки ослабления связей. В живых животных прицельное понижение Dlgap2 в мозге вызывало поведение, похожее на аутистическое: молодые самцы мышей испытывали затруднения при запоминании расположения скрытой платформы в водном лабиринте и проявляли уменьшенный интерес к социальным партнерам и социальной новизне в тесте с тремя камерами. Эти изменения имитируют нарушения обучения и социального поведения, наблюдаемые у животных, подвергшихся воздействию вальпроевой кислоты, что усиливает аргумент в пользу того, что потеря Dlgap2 — не просто побочный эффект, а фактор, приводящий к изменению поведения.
Поиск уязвимого партнёра в синапсе
Чтобы понять, как потеря Dlgap2 распространяется по синапсу, исследователи внимательнее рассмотрели белки, закрепленные в постсинаптической плотности — плотной молекулярной «подушке», принимающей химические сигналы. С помощью протеомики они выяснили, что снижение Dlgap2 меняет количество сотен синаптических белков, особенно тех, что участвуют в организации синапсов и рециклинге везикул через эндоцитоз. Один белок, Intersectin‑1 (Itsn1), особенно резко снижался. Дальнейшие биохимические исследования показали, что Dlgap2 и Itsn1 физически сосуществуют в одних и тех же белковых комплексах в синапсо‑обогащенных фракциях и что оба входят в число генов, связанных с аутизмом. Это указывало на целенаправленное регуляторное партнерство между двумя молекулами в плотной синаптической среде. 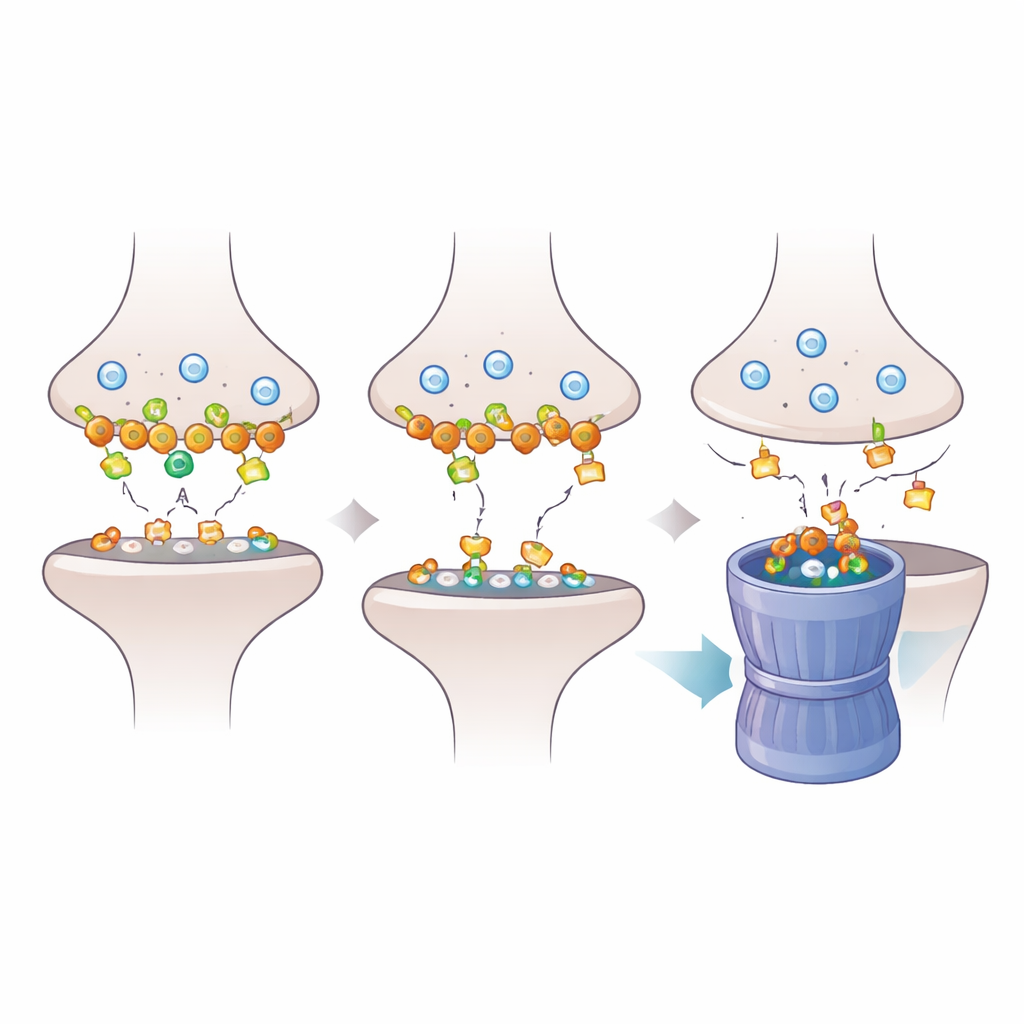
Важный путь утилизации выходит на свет
Команда затем поинтересовалась, почему уровень Itsn1 падает при отсутствии Dlgap2. Они обнаружили, что в синаптических компартментах при нокдауне Dlgap2 усиливается форма убиквитинирования, связанная через лизин‑48 (K48), которая маркирует белки для разрушения протеасомой — клеточным «шредером». Блокирование этой системы утилизации препаратом MG132 предотвращало потерю Itsn1, что указывает на то, что Dlgap2 обычно защищает Itsn1 от пометки и разрушения. При отсутствии Dlgap2 Itsn1 все чаще помечается, направляется в протеасому и истощается в синапсах, нарушая эндоцитарный рециклинг и баланс синаптической активности. Работа показывает, что даже тонкие сдвиги в скорости оборота ключевых белков могут дестабилизировать синапсы в ходе развития мозга.
Что это значит для аутизма и будущих лечений
В сумме исследование предлагает простую, но содержательную идею для неспециалистов: пренатальное воздействие вальпроевой кислоты может ослабить структурный «распорный» белок (Dlgap2) в синапсах. Когда этот упор теряется, его партнер — белок Itsn1 — становится чрезмерно помеченным для клеточной утилизации, что приводит к неправильному рециклингу синаптических компонентов и, в конечном счете, к нарушению проводки и поведению, похожему на аутистическое, у мышей. Хотя в аутизме участвуют многие гены и факторы окружения, ось Dlgap2–Itsn1 предлагает конкретную молекулярную цепочку от пренатального воздействия препарата к изменению функции мозга. В долгосрочной перспективе стратегии, сохраняющие это партнерство или тонко регулирующие машину утилизации белков в синапсах, могут помочь защитить развивающийся мозг от сходных нарушений.
Цитирование: Guo, X., Zhang, L. & Zhuang, K. Dlgap2 deficiency disrupts synaptic homeostasis by promoting ubiquitin-mediated Itsn1 degradation in a valproic acid-induced autism-like model. Sci Rep 16, 8305 (2026). https://doi.org/10.1038/s41598-026-39099-x
Ключевые слова: вальпроевая кислота и беременность, синаптические белки‑каркасы, механизмы расстройств аутистического спектра, путь убиквитин‑протеасома, мышиные модели аутизма