Clear Sky Science · ru
Передача тяговых сил через биоактивный матричный гидрогель способствует коллекторной миграции эпителиальных клеток, опосредованной интегринами
Как клетки тянут вместе, чтобы зажить
Когда вы порезали кожу или повредили орган, пласты клеток должны скоординированно переместиться, чтобы закрыть рану. В этом исследовании ставится на вид простая, но вводящая в заблуждение вопрос: когда клетки ползут вместе, они просто тянут друг друга или также «общаются» через мягкий материал под ними? Воссоздав в лаборатории реалистичную желеобразную среду, авторы показывают, что клетки могут передавать механические силы через этот мягкий матрикс, направляя групповое движение, раскрывая скрытый уровень коммуникации, который может играть ключевую роль в заживлении ран, восстановлении тканей и даже в распространении рака.
Мягкое основание, которое несет силу
В нашем организме многие клетки располагаются не на твердой поверхности вроде стекла или пластика, а на мягком белковом каркасе. Чтобы смоделировать это, исследователи выращивали клетки эпителия почки в виде непрерывного пласта на биоактивном гидрогеле из Matrigel и коллагена — двух распространенных компонентов натуральной ткани. Затем они создали небольшую пустую зону в середине геля, подобную маленькой ране, и наблюдали, как пласт клеток шаг за шагом заполняет зазор. Для отслеживания активности ключевого сигнального пути внутри клеток использовали флуоресцентный биосенсор, сообщающий об активности ERK — белка, часто реагирующего на механические сигналы. Такая установка позволяла в реальном времени видеть, как механические силы в мягком геле соотносятся и с движением клеток, и с внутриклеточной сигнализацией. 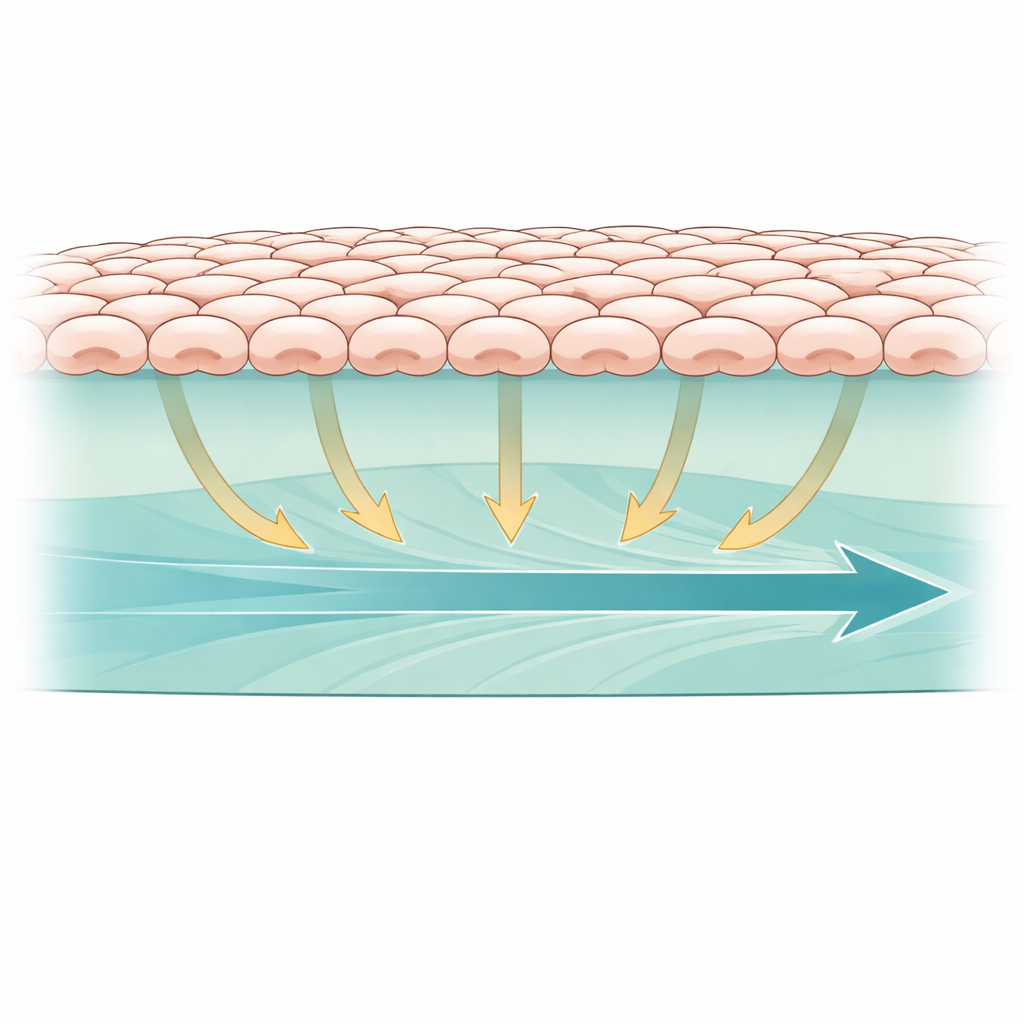
Наблюдая за тем, как земля движется под клетками
Чтобы понять, несет ли гель действительно нагрузку и передает ли силу, команда смешала в материале крошечные магнитные шарики и отслеживала их движение во время миграции клеток. На обычном геле, содержащем и Matrigel, и коллаген, шарики медленно скользили вперед в том же направлении, что и продвигающийся пласт клеток, что указывает на то, что клетки захватывают и тянут за собой матрикс. На гелях, состоящих только из Matrigel, шарики двигались медленнее, что свидетельствует о слабой передаче сил. Когда гель химически сшивали глаутаровым альдегидом, чтобы его упрочнить и «запереть» сеть, шарики почти не смещались. В этих «заблокированных» условиях клетки по-прежнему прикреплялись, но их коллективное продвижение резко замедлялось, а сигнал ERK становился слабее и менее сосредоточенным на переднем крае, связывая сильное сцепление с матриксом с более быстрым и направленным групповым движением.
Внутренние моторы и ионные ворота приводят движение
Авторы далее исследовали, что внутри клеток генерирует эти тянущие силы и как эта активность воспринимается. Они применяли препараты, блокирующие миозин-опосредованную контрактильность — тот же тип молекулярной машины, что приводит в движение мышцы. При ингибировании сокращения активность ERK падала, а пласт клеток продвигался медленнее, что согласуется с идеей, что внутреннее натяжение необходимо для передачи напряжения в матрикс. Они также вмешивались в работу нескольких типов кальциевых каналов в клеточной мембране и внутреннем кальциевом депо. Блокирование этих ионных путей ослабляло активность ERK и замедляло коллективную миграцию, указывая на цепочку событий, в которой механическое натяжение матрикса преобразуется в кальциевые и ERK-сигналы, помогающие группе двигаться единой силой.
Направление с помощью поверхностных захватов
Особенно заметный результат получилcя при нацеливании на интегрины — молекулы на поверхности, действующие как крошечные якоря, связывающие клетки с окружением. Когда исследователи блокировали один из основных подтипов интегринов, пласт перестал продвигаться вперед как целостный фронт, хотя отдельные клетки все еще могли локально шевелиться с почти нормальной скоростью. Одновременно движение шариков в геле почти остановилось, показывая, что интегрины необходимы для передачи силы от сокращающихся клеток к матриксу. В отличие от этого, блокирование механочувствительных каналов, связанных с Piezo1, которые помогают клеткам ощущать физическое давление, снижало и темп миграции, и сцепление, наблюдаемое в геле. В совокупности эти результаты рисуют картину, при которой сокращение генерирует силу, интегрины передают ее матриксу, а механочувствительные каналы и ERK-сигнализация интерпретируют эту силу, координируя направление и эффективность коллективного движения. 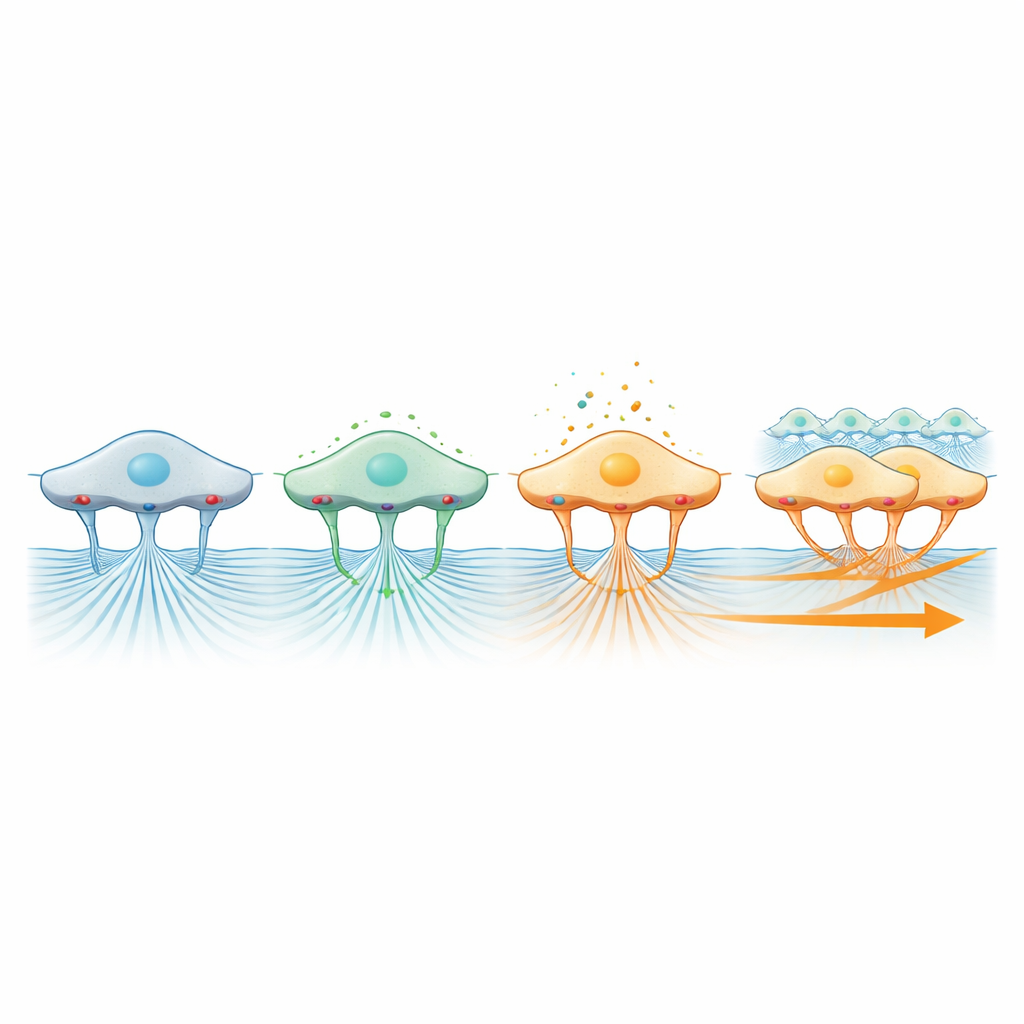
Почему это важно для заживления и болезней
Проще говоря, работа показывает, что пласты клеток не просто тянут друг друга; они также тянут и через мягкий материал под ними, используя его как некую механическую телефонную линию. Сокращения слоя клеток посылают напряжение через матрикс, и это напряжение, воспринимаемое через интегрины и ионные каналы и считываемое по активности ERK, помогает группе двигаться быстро и в едином направлении. Когда матрикс химически «заперт», так что силы не могут распространяться, или когда блокируются ключевые поверхностные «захваты» и датчики, коллективное продвижение слабеет. Эти наблюдения углубляют наше понимание того, как закрываются раны, как ткани поддерживают свою структуру и как инвазивные группы клеток, например при раке и фиброзе, могут использовать механические пути в окружении для распространения.
Цитирование: Ouyang, M., Cao, Y., Sheng, H. et al. Traction force transmission via bioactive matrix hydrogel promotes epithelial collective migration mediated by integrin. Sci Rep 16, 8923 (2026). https://doi.org/10.1038/s41598-026-39048-8
Ключевые слова: коллективная миграция клеток, механическая сигнализация, внеклеточный матрикс, интегрин, заживление ран