Clear Sky Science · ru
In Silico-идентификация мелкомолекулярных ингаляционных антагонистов IL-33/ST2 для эндотипов тяжелой астмы с высоким уровнем типа‑2
Почему это важно для дыхания
Для миллионов людей с тяжелой астмой даже современные ингаляторы и продвинутые инъекции не всегда устраняют одышку и риск опасных приступов. В этом исследовании рассматривают, можно ли переработать известные, таблеткоподобные препараты так, чтобы они работали как ингаляционные средства, блокирующие один из «тревожных» сигналов в легких при астме. Используя только компьютерное моделирование, исследователи искали мелкие молекулы, которые могли бы присоединяться к ключевому рецептору, участвующему в тяжелой аллергической астме, закладывая основу для последующих лабораторных испытаний, а не предлагая готовое лекарство.
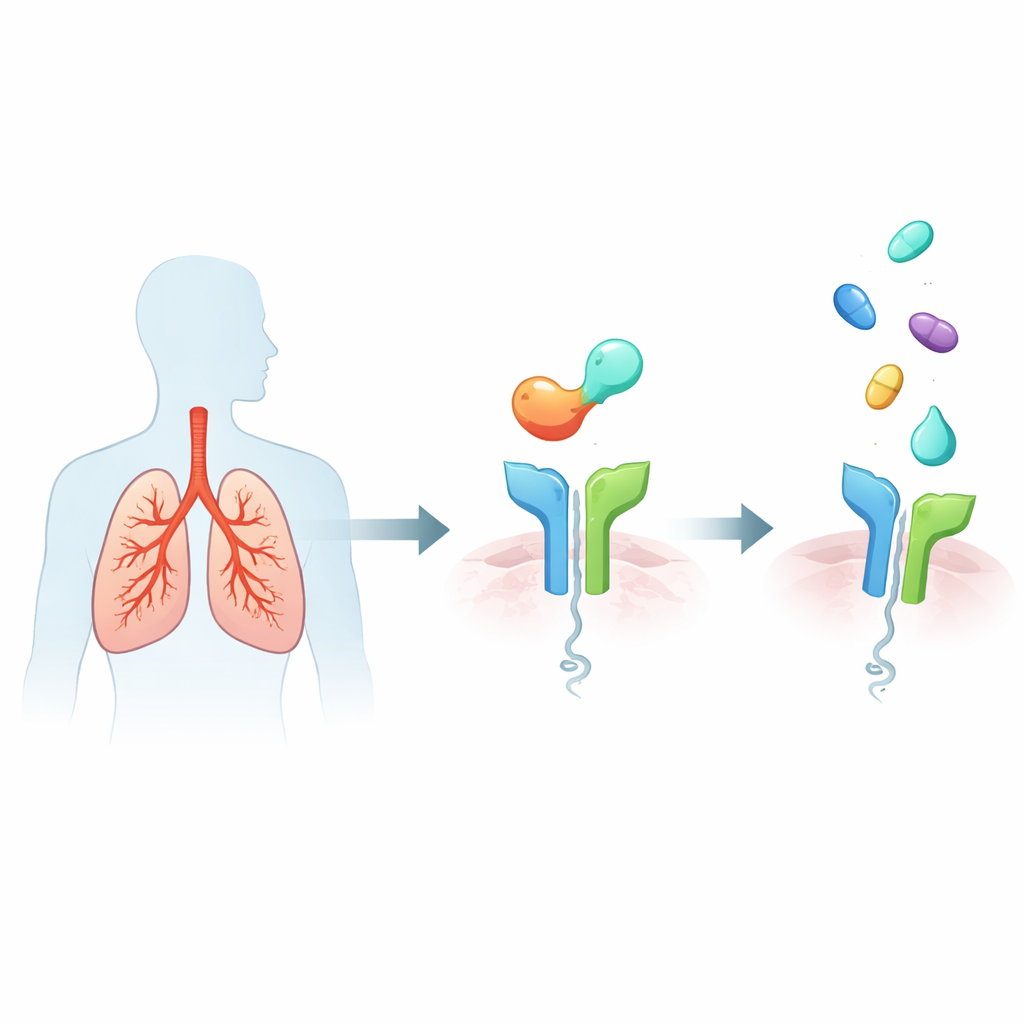
Система тревоги внутри астматических легких
Тяжелая астма с высоким типом‑2 характеризуется гиперактивным иммунным ответом, который заполняет дыхательные пути слизью и воспалительными клетками, сужает бронхи и со временем повреждает структуру легких. Основным триггером является белок IL‑33, выделяемый поврежденными клетками эпителия дыхательных путей. IL‑33 присоединяется к рецептору ST2 на различных иммунных клетках, которые затем выбрасывают мощные сигнальные молекулы, вызывающие типичные симптомы астмы, такие как хрипы, обострения и долгосрочное ремоделирование дыхательных путей. Поскольку повышенная активность IL‑33/ST2 связана с более тяжелыми симптомами и частыми приступами, ST2 стал привлекательной «вверхпо течению» мишенью: заблокируйте ST2 — и можно одновременно подавить многие последующие воспалительные сигналы.
От антител к привычным препаратам
Несколько существующих терапий для тяжелой астмы используют вводимые инъекционно антитела, которые нейтрализуют воспалительные белки в крови или блокируют их рецепторы. Хотя они эффективны у некоторых пациентов, такие биопрепараты дороги, требуют введения инъекций и нацелены в основном на сигналы, расположенные дальше по цепочке. Напротив, мелкомолекулярные препараты — ближе к традиционным таблеткам или ингаляторам — могут производиться в масштабах, удобно храниться и потенциально доставляться прямо в легкие. Проблема в том, что ST2 связывается с IL‑33 через широкую белок‑белковую поверхность, которую труднее нарушить мелкой молекулой, чем аккуратно оформленную глубокую полость фермента. Поэтому авторы обратились к высокоточной структурной информации о комплексе ST2–IL‑33 и современным in silico инструментам, чтобы выяснить, не найдется ли среди известных противовоспалительных препаратов тех, кто неожиданно «схватит» часть этого интерфейса.
Поиск по поверхности рецептора с помощью компьютера
Используя кристаллическую структуру человеческого ST2, связанного с IL‑33, команда сначала удалила IL‑33, чтобы обнажить связывающую поверхность рецептора, и применила программу поиска карманов, чтобы указать наиболее перспективный регион для размещения мелкомолекулы. Затем они выбрали десять клинически значимых мелкомолекул, уже используемых при астме или родственных иммунных заболеваниях — такие как блокаторы лейкотриенов монтелукаст и зафирлукаст, родственники талидомида с иммуномодулирующим действием и ингибиторы JAK — а также ранее описанную молекулу, ориентированную на ST2, в качестве эталона. С помощью виртуального докинга каждое соединение позиционировали тысячи раз на поверхности ST2, а лучшие позы оценивались по предполагаемой силе связывания. Зафирлукаст оказался лидером по ранжированию, немного опережая монтелукаст и известный ST2‑ориентированный компаратор.
Настройка лидирующей молекулы на экране
Поскольку зафирлукаст демонстрировал наиболее перспективное сочетание предсказанного связывания и общих лекарственно‑похожих свойств, авторы использовали инструмент проектирования на базе ИИ для создания модифицированной версии этой молекулы. Цель состояла в том, чтобы сохранить её сцепление со ST2 и одновременно улучшить предсказанный профиль безопасности. Переработанный аналог имел очень похожую оценку докинга и в in silico оценках предполагался как менее токсичный. Подробные карты контактов показали, что и исходное, и модифицированное соединения касаются нескольких тех же аминокислот ST2, которые обычно контактируют с IL‑33, что предполагает, что они занимают функционально важные участки интерфейса. Продолжительные молекулярно‑динамические симуляции — полмикросекунды виртуального движения в воде и соли — показали, что и рецептор, и лиганд остаются гибкими, при этом мелкая молекула перемещается по поверхности, а не жестко фиксируется в одной позе. Вычисления энергий взаимодействия во времени указывали на значимую, но динамическую ассоциацию, согласующуюся с молекулой, исследующей относительно плоскую белок‑белковую поверхность.
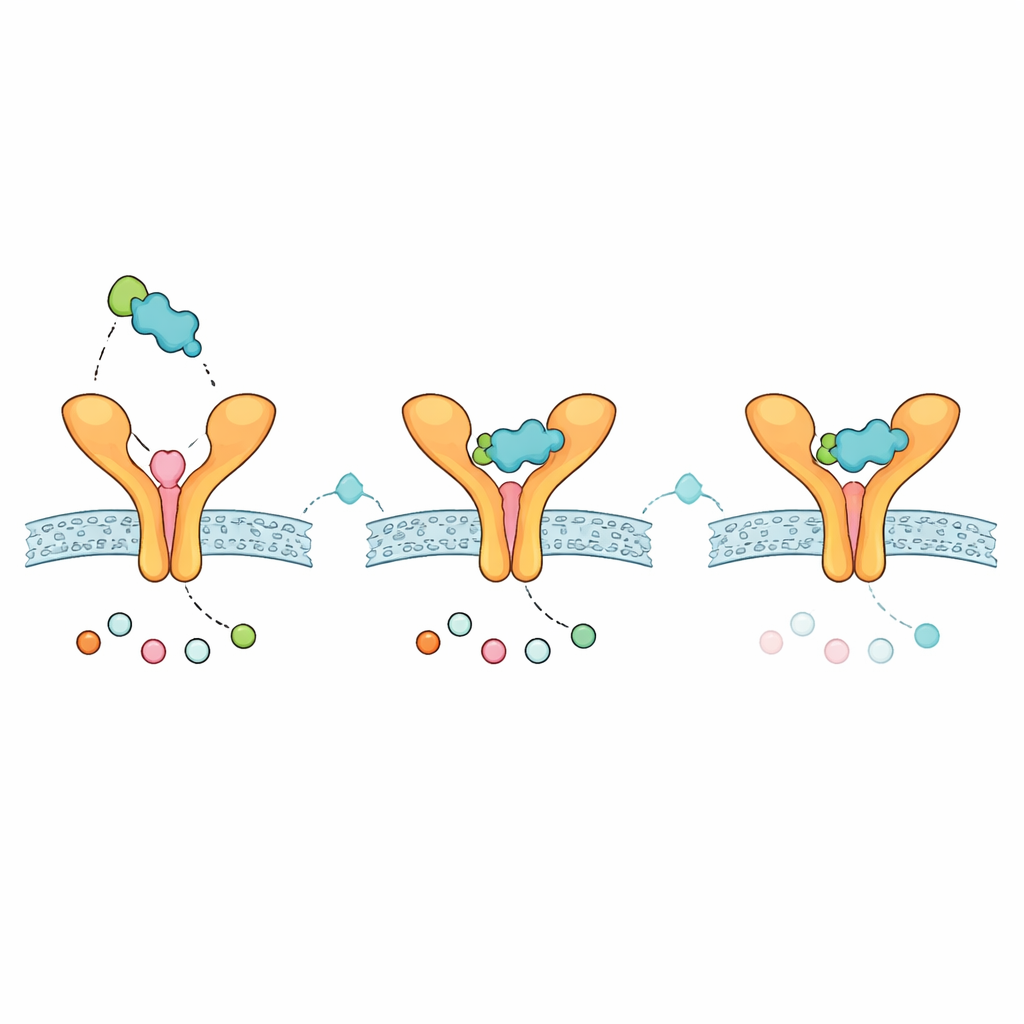
Подсказки о том, как может вести себя будущий ингалятор
Чтобы оценить, может ли модифицированный зафирлукаст правдоподобно функционировать как лекарство, команда провела стандартные вычислительные проверки абсорбции, распределения, метаболизма, выведения и токсичности. Аналог удовлетворял общим правилам лекарственно‑похожести для пероральных препаратов, имел умеренные размеры и жирорастворимость и, по предсказаниям, не проникает в мозг — характеристики, которые могут быть благоприятны для лечения, направленного на легкие с ограниченными системными побочными эффектами. Оценки растворимости варьировались в разных моделях, что указывает на необходимость тщательной разработки формуляции, особенно для неоральных путей введения, таких как ингаляция. Также предсказывалось взаимодействие соединения с определенными печеночными ферментами, что означает, что потенциальные лекарственно‑лекарственные взаимодействия потребуют внимания, если препарат когда‑нибудь будет использоваться одновременно с другими медикаментами.
Что действительно показывает эта работа
Это исследование не представляет собой готового противоастматического препарата, а демонстрирует пошаговую вычислительную стратегию поиска и оптимизации мелкомолекул, которые могут вмешиваться в систему тревоги IL‑33/ST2 на поверхности клеток дыхательных путей. В нем выделены зафирлукаст и оптимизированный ИИ аналог как правдоподобные отправные точки для лабораторных экспериментов, показано, что они способны занимать ключевые участки интерфейса ST2 и обладают в целом приемлемыми предсказанными безопасностными и лекарственно‑похожими свойствами. Однако все доказательства исключительно виртуальные: работа не доказывает, что эти молекулы реально блокируют связывание IL‑33 с ST2, подавляют воспалительную сигнализацию или облегчают дыхание пациентов. Эти вопросы потребуют биохимических тестов, клеточных исследований, моделей на животных и, в конечном счете, клинических испытаний. На данный момент исследование предлагает вычислительную дорожную карту и короткий список кандидатных скелетов для ученых, стремящихся превратить собственный «тревожный переключатель» при астме в практическую, ингаляционную лекарственную мишень.
Цитирование: Sun, G., Liu, Q., Yu, M. et al. In Silico identification of inhalable small-molecule IL-33/ST2 antagonists for severe type-2-high asthma endotypes. Sci Rep 16, 7996 (2026). https://doi.org/10.1038/s41598-026-39027-z
Ключевые слова: тяжелая астма, путь IL-33 ST2, мелкомолекулярные антагонисты, in silico дизайн лекарств, ингаляционные терапевтические средства