Clear Sky Science · ru
Пептид из пчелиной пыльцы с двойным действием: ингибирование DPP‑IV и модуляция транспорта глюкозы
Почему пчелиная пыльца может иметь значение для уровня сахара в крови
Сахарный диабет 2 типа часто сводят к избытку сахара и нехватке инсулина, но за этим стоит сеть ферментов и транспортеров, которые тонко регулируют переработку глюкозы в организме. В этом исследовании рассматривается любопытная гипотеза: пчелиная пыльца, природный «суперфуд», может быть источником коротких белковых фрагментов (пептидов), которые одновременно защищают гормональные сигналы, контролирующие уровень сахара, и умеренно меняют всасывание сахара из кишечника. Работа сосредоточена на одном таком пептиде, названном AA‑7, и спрашивает, может ли он когда‑нибудь вдохновить более безопасные пищевые стратегии для помощи в контроле диабета.
От улья до лаборатории
Пчелиная пыльца — это смесь растительной пыльцы и материалов пчел, богатая белками, витаминами и другими питательными веществами. Чтобы имитировать пищеварение у человека, исследователи обработали белки пчелиной пыльцы двумя пищеварительными ферментами — пепсином и панкреатином, аналогичными тем, что действуют в желудке и тонком кишечнике. Этот процесс расщепил большие белки на множество меньших фрагментов, некоторые длиной всего в несколько аминокислот. Затем фракции разделяли по размеру и химическим свойствам и тестировали каждую на способность блокировать фермент DPP‑IV, который обычно расщепляет и инактивирует гормоны, стимулирующие выделение инсулина. Одна фракция очень маленьких, относительно маслянистых (гидрофобных) пептидов выделялась благодаря сильной активности по блокированию DPP‑IV. 
Поиск выдающегося пептида
С помощью высокоразрешающей масс‑спектрометрии команда идентифицировала семиаминокислотный пептид с последовательностью Ala‑Thr‑His‑Ala‑Leu‑Leu‑Ala, который назвали AA‑7. Его синтезировали, чтобы протестировать в чистом виде. В ферментных тестах AA‑7 ингибировал DPP‑IV в микромолярном диапазоне, что несколько слабее по сравнению со стандартным лабораторным препаратом, но сопоставимо или лучше, чем многие пептиды из пищевых источников, описанные в литературе. Анализ зависимости скорости реакции от концентраций пептида и субстрата показал, что AA‑7 действует как конкурентный ингибитор: он занимает тот же активный карман DPP‑IV, что и природные субстраты, препятствуя их доступу, но не разрушает фермент.
Взаимодействия пептида и фермента на атомном уровне
Чтобы понять, почему AA‑7 эффективен, исследователи использовали компьютерное докинг‑моделирование, чтобы разместить пептид в трёхмерной модели DPP‑IV, а затем провели молекулярно‑динамические симуляции во времени. Модели показали, что AA‑7 располагается в каталитическом кармане фермента, контактируя с ключевыми аминокислотами, уже известными как критичные для активности DPP‑IV. Прогнозируемая прочность связывания была как минимум сопоставима со связыванием референтного ингибитора. Дальнейшие компьютерные оценки абсорбции, распределения, метаболизма и токсичности (ADMET) дали реалистичное предостережение: AA‑7, скорее всего, безопасен, но плохо всасывается через стенку кишечника в неизменённом виде — распространённое ограничение для малых пептидов. Это указывает на необходимость разработать способы доставки или структурные модификации, если AA‑7 или молекулы на его основе предполагается применять у людей.
Модуляция того, как кишечник обрабатывает сахар
Исследование не ограничилось экспериментами в пробирке. Команда обрабатывала культивируемые человеческие кишечные клетки (линия Caco‑2) AA‑7 и измеряла как захват глюкозы, так и активность генов, кодирующих два основных кишечных транспортёра глюкозы — SGLT1 и GLUT2. При нетоксичных дозах AA‑7 изменял скорость проникновения флуоресцентного аналога глюкозы в клетки; эффект зависел от дозы и времени. Также наблюдались изменения уровня экспрессии генов SGLT1 и GLUT2, причём эти изменения различались при краткосрочном (30 минут) и длительном (24 часа) воздействии. Компьютерный докинг показал, что AA‑7 может взаимодействовать со структурными участками этих транспортеров, хотя такие модели служат гипотезой, а не окончательным доказательством. В совокупности клеточные и модельные данные указывают, что AA‑7 делает больше, чем просто блокирует DPP‑IV — он также влияет на механизмы переноса сахара из кишечника в кровоток. 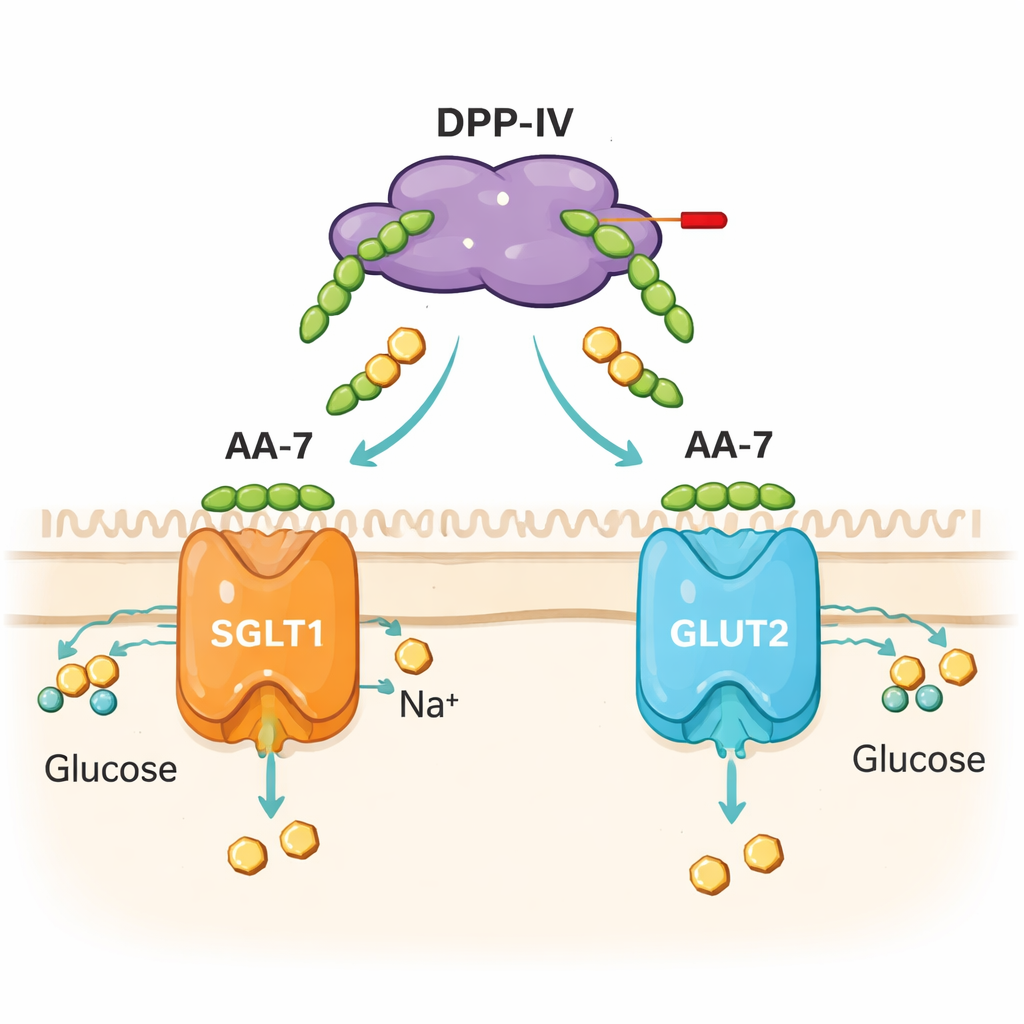
Что это может значить для будущих продуктов питания
Для неспециалиста основной вывод таков: пептид AA‑7 из пчелиной пыльцы, по‑видимому, действует по двум направлениям, важным для сахарного диабета 2‑го типа — он замедляет ключевой фермент, разрушающий гормоны, стимулирующие инсулин, и влияет на то, как кишечные клетки усваивают глюкозу. Сам по себе AA‑7 пока не готов стать лекарством или добавкой, отчасти потому, что может плохо всасываться. Тем не менее он указывает на пчелиную пыльцу — и, возможно, другие богатые белком продукты — как на резервуар коротких многофункциональных пептидов, которые могут вдохновить создание новых функциональных продуктов или пептидных терапий. При дальнейших исследованиях на животных и людях и с улучшенными способами доставки такие молекулы с двойным действием могут стать частью более тонкого, основанного на пище подхода к поддержанию нормального уровня сахара в крови.
Цитирование: Mongkolnkrajang, U., Kuptawach, K., Sangtanoo, P. et al. Bee pollen-derived peptide with dual DPP-IV Inhibition and glucose transport modulation. Sci Rep 16, 7616 (2026). https://doi.org/10.1038/s41598-026-39009-1
Ключевые слова: пептиды из пчелиной пыльцы, ингибирование DPP‑IV, транспорт глюкозы, сахарный диабет 2 типа, функциональные продукты питания